
Wetenschap
Een draagbare, vrijstaand elektrochemisch detectiesysteem
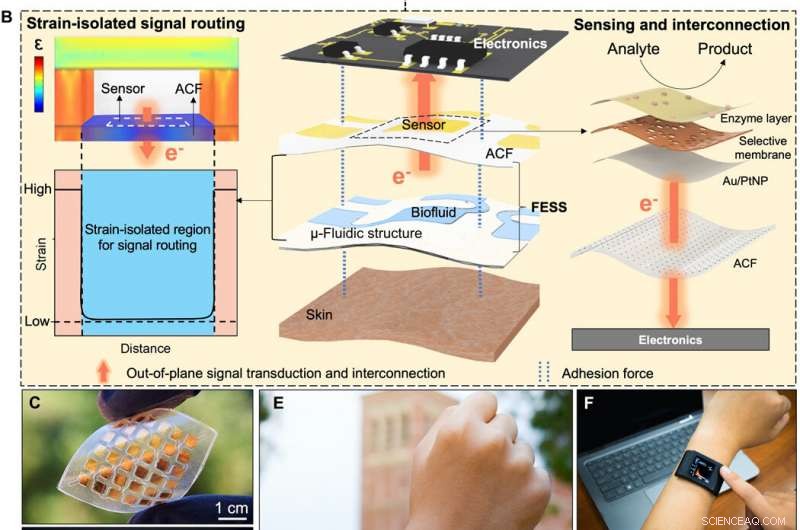
FESS ontwerpgrond, implementatie, en toepassing. (A) Schema van de biomarker-informatie-afleveringsroute mogelijk gemaakt door de FESS, ter illustratie van steekproeven, voelen, en routering van epidermaal opgehaalde biomarkerinformatie naar uitleeselektronica via een enkele entiteit. (B) Ontwerpgrondslag van de FESS. (C) Representatieve uitvoering van het FESS, het demonstreren van flexibiliteit en geen in-plan interconnectie. (D) Representatieve familie van FESS-apparaten, bevattende 1 × 2, 3 × 3, en 6 × 6 elektrode-arrays. (E) Op maat ontwikkelde en FESS-enabled smartwatch voor biomarker monitoring. (F en G) Inzet van de FESS-enabled smartwatch in stationaire (F) en hoge intensiteit oefening (G) instellingen. (Fotocredit:Peterson Nguyen, Kaili Chiu, Yichao Zhao, Universiteit van Californië, Los Angeles.) Krediet: wetenschappelijke vooruitgang , doi:10.1126/sciadv.aaz0007
In een nieuwe studie gepubliceerd op wetenschappelijke vooruitgang , Yichao Zhao en een onderzoeksteam in geïntegreerde bio-elektronica en materialen en engineering in de VS hebben een wegwerp-, vrijstaand elektrochemisch detectiesysteem (FESS). Dankzij de FESS konden ze een ontwerpstrategie op systeemniveau realiseren om de uitdagingen van draagbare biosensoren in aanwezigheid van beweging aan te pakken en naadloze integratie met consumentenelektronica mogelijk te maken. Het team ontwikkelde een FESS-compatibele smartwatch, met zweetmonsters, elektrochemische detectie en gegevensweergave of -overdracht, binnen een op zichzelf staand draagbaar platform. Het team gebruikte de FESS-smartwatch om de profielen van zweetmetabolieten bij individuen in sedentaire en zeer intensieve trainingsomgevingen te volgen.
De internet-of-things-infrastructuur (IOT) kan worden gebruikt in draagbare consumentenelektronica om gepersonaliseerde en precisiegeneeskunde te transformeren door fysiologisch relevante gegevens te verzamelen met minimale tussenkomst van de gebruiker. Wetenschappers hebben meestal fysieke sensoren gebruikt in commerciële draagbare platforms om de fysieke activiteit en vitale functies van een gebruiker te volgen. Echter, inzicht krijgen in de dynamische chemie van het lichaam, onderzoekers hebben elektrochemische detectieoppervlakken nodig om zich te richten op de biomarkermoleculen in niet-invasief opgehaalde lichaamsvloeistoffen zoals zweet. Om dit te bereiken, het is van cruciaal belang om de informatieoverdrachtroute van de skin naar een uitleeseenheid nauwkeurig te ontwerpen. Voor elektrochemische detectie, de informatieafgifteroute moet de biomarkerrijke biovloeistof bemonsteren en afleveren aan het sensoroppervlak in een microfluïdische structuur, gevolgd door signaaltransductie via onderling verbonden elementen naar de uitleeselektronica. Het signaal moet langs deze route worden gehandhaafd in de aanwezigheid van door beweging geïnduceerde spanning.
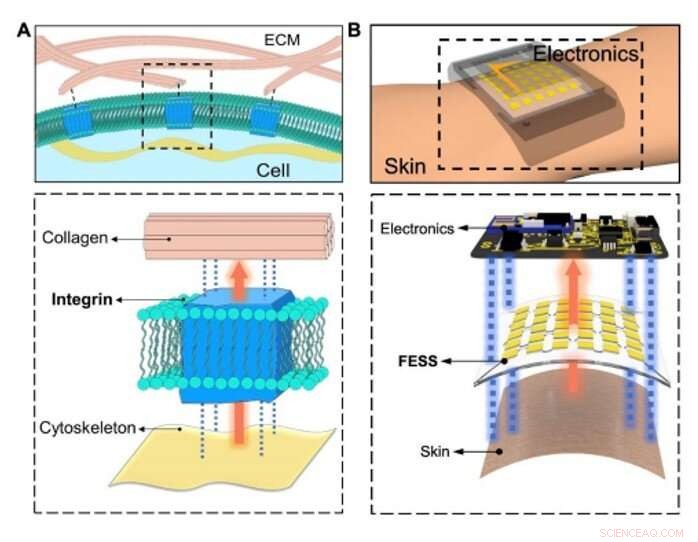
Bio-geïnspireerde in situ detectie en signaalinterconnectie. (A) Conceptuele illustratie van de fysiologische informatie-uitwisseling tussen intracellulaire/extracellulaire matrices gefaciliteerd door celadhesiemoleculen (integrine) via sensing, out-of-plane signaalinterconnectie, en dubbelzijdige hechting. (B) In-situ detectie, out-of-plane signaalinterconnectie, en dubbelzijdige hechting mogelijk gemaakt door FESS, als een enkele entiteit, geplaatst tussen huid en elektronica. Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aaz0007
In dit werk, Zhao et al. ontwikkelde het vrijstaande elektrochemische detectiesysteem (FESS) en hechtte het tegelijkertijd aan de huid en aan de elektronica met behulp van dubbelzijdige hechtkrachten zonder stijve connectoren. De FESS bemonsterde en regisseerde epidermaal biovloeistoffen voor elektrochemische detectie, gevolgd door routering naar uitleeselektronica via een spanningsgeïsoleerd pad. Ze integreerden de FESS in een op maat gemaakte smartwatch voor zweetinductie, bemonstering, elektrochemische detectie, signaalverwerking en gegevensweergave of -overdracht. De resultaten toonden high-fidelity signaaltransductie en robuust mechanisch contact met de menselijke huid zonder de beweging van de gebruiker te beperken. Het vrijstaande sensorsysteem kan worden gekoppeld aan toekomstige draagbare elektronica om high-fidelity gezondheids- en welzijnsgerelateerde datasets te genereren op basis van de dagelijkse activiteiten van gebruikers.
Om een efficiënte biologische route te creëren, Zhao et al. geselecteerde integrine - een celadhesiemolecuul dat op efficiënte wijze fysiologische informatie-uitwisseling tussen intracellulaire en extracellulaire matrices mogelijk maakte. Het FESS-apparaat implementeerde integrine-achtige functionaliteiten via een spanningsgeïsoleerd gebied in een microfluïdische structuur. Ze ontwikkelden FESS als een verticaal geleidend, dubbelzijdig klevend en flexibel microfluïdisch bioanalytisch dunne-filmsysteem bestaande uit meerdere verticaal gestapelde films. Deze films omvatten een zelfklevende anisotrope geleidende film (ACF), een edele metalen elektrode-arrayfilm, een biochemische film, een microfluïdische film en een huidklevende film. Ze plakten het complete dunne-filmsysteem op de uitleeselektronica zonder connectoren en met minimale contactweerstand om elk elektrisch contact mogelijk om te zetten in een chemische of biologische sensor. Het team ontwikkelde een proof-of-principle, zelfstandige biomarker-sensing smartwatch met FESS om de zweetmetabolietprofielen van individuen in sedentaire versus intensieve omgevingen te volgen.

FESS-reksimulatie en karakterisering van spanningsgeïsoleerde signaalinterconnectie. (A) Illustratie van de FESS 'out-of-plane signaalinterconnectie versus conventionele in-plane signaalinterconnectie. Conventionele implementaties zijn beperkt tot signaalroutering door zeer gespannen regio's, terwijl de bedachte FESS routering mogelijk maakt via bijna-nul spanningsgebieden. (B) COMSOL-gesimuleerde stam (ε) profiel van een representatieve FESS in aanwezigheid van een extern toegepaste schuifkracht, ter illustratie van bijna nul spanning aan de onderkant van het microkanaal (d.w.z. substraat-biovloeistof-interface). (C) Overeenkomstige ingezoomde weergave van het stamprofiel voor één "pixel". (D) Stamverdeling langs de stippellijn in (C). (E) Out-of-plane interconnectie elektrische karakterisering van FESS uitgevoerd onder verschillende gelokaliseerde buighoeken (voor een reeks van 6 × 6 Au-elektroden). (F) Interconnectieweerstanden van de gebogen FESS-FPCB (RFESS + RFPCB), voor verschillende gelokaliseerde buighoeken (genormaliseerd met betrekking tot RFPCB zonder buiging, offerteaanvraag, 0). Foutbalken geven de standaardfout van metingen over de zes elektroden in elke kolom aan. (G) Weerstandsmetingen van de FESS-elektroden onder verschillende buighoeken (n =36), met betrekking tot de weerstand van het FPCB-contactvlak (RFPCB, 0). (H tot J) 180° afpeltesten die de onderlinge hechting tussen de PCB en FESS karakteriseren met verschillende rugstructuren:microfluïdische basis–ACF (H), microfluïdisch kanaal-ACF (I), en een representatieve microfluïdische kanaalarray-ACF (J). (Fotocredit:Peterson Nguyen, Universiteit van Californië, Los Angeles.) Krediet: wetenschappelijke vooruitgang , doi:10.1126/sciadv.aaz0007
In deze opstelling, de verticale geleidbaarheid van ACF vergemakkelijkte out-of-plane signaalinterconnecties om ongewenste door lichaamsbewegingen veroorzaakte spanningseffecten op de signaalroutes te voorkomen. Het team karakteriseerde de mechanische adhesie-eigenschap van FESS om ervoor te zorgen dat de adhesiekrachten tussen de FESS en elektronica hoger waren dan die tussen FESS en een droge of actief zwetende huid. Het team testte de kracht die nodig was om de ACF-laag van de FESS af te pellen op een printplaat en de resultaten toonden een sterke FESS-gebaseerde verbinding met elektronica, geschikt voor toepassingen op het lichaam.
Zhao et al. testte vervolgens het signaaltransductievermogen van de FESS. Ze vormden edelmetaalelektroden op de ACF om biochemische-naar-elektrische signaaltransductie te bereiken, gevolgd door afzetting van biochemische films om biomoleculaire doelen van belang te analyseren. Ze testten de elektrochemische activiteit van ACF met metaalpatroon voor twee veelgebruikte elektrode-oppervlakken op ongewijzigd goud (Au) en platina (Pt) nanodeeltjes-gemodificeerd Au. De elektroanalytische methoden die in het werk werden onderzocht, leverden biomarker-uitlezingen van monster tot antwoord om realtime inzicht te krijgen in de veranderingen in de biocompositie van zweet.

Testen van de weerstandsmeting van de op ACF gebaseerde onderlinge verbindingen na mechanische vervorming. Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aaz0007
In de volgende paar experimenten, het onderzoeksteam toonde het vermogen van FESS om biomarkers te monitoren tijdens de dagelijkse activiteiten van de gebruiker. Om dit te bereiken, ze integreerden FESS in een op maat ontwikkelde smartwatch als een model IOT-apparaat met een analoog/digitaal circuit, Bluetooth-transceiver en een LCD-scherm (liquid crystal display) voor functionaliteiten op systeemniveau, inclusief signaal- en gebruikersopdrachtverwerking, display en draadloze datacommunicatie. De op FESS gebaseerde smartwatch presteerde op dezelfde manier als een potentiostaat. De wetenschappers plakten de complete smartwatch op de huid zonder externe omhulsels of armaturen voor draadloze biomarkerdetectie als een op zichzelf staande eenheid. Het LCD-scherm toonde realtime metingen en het tijdelijke profiel van de biomarkermetingen, terwijl de Bluetooth-ontvanger de metingen doorstuurde naar een op maat ontwikkelde mobiele applicatie om de gegevens naar een cloudserver te uploaden voor verdere analyse.
Het team plakte de op FESS gebaseerde smartwatch op de onderarm van een proefpersoon om zijn functie als een draagbaar systeem voor het bewaken van biomarkers weer te geven. De proefpersoon kan het apparaat draadloos bedienen om real-time, op zweet gebaseerde biomarkermetingen ten opzichte van de dagelijkse routine van de gebruiker. De gebruiker controleerde hun zweetglucosewaarden voor of na het nuttigen van een gemengde reeks maaltijden en de uitlezing van de smartwatch gaf verhoogde zweetglucosewaarden aan na voedselinname, in lijn met eerdere trends. De smartwatch gaf bovendien gebruikersinformatie over zweetlactaatmetingen tijdens het hardlopen in een veld, de resultaten waren consistent ondanks de betrokkenheid van hoogfrequente en op hoge versnelling gebaseerde lichaamsbewegingen.
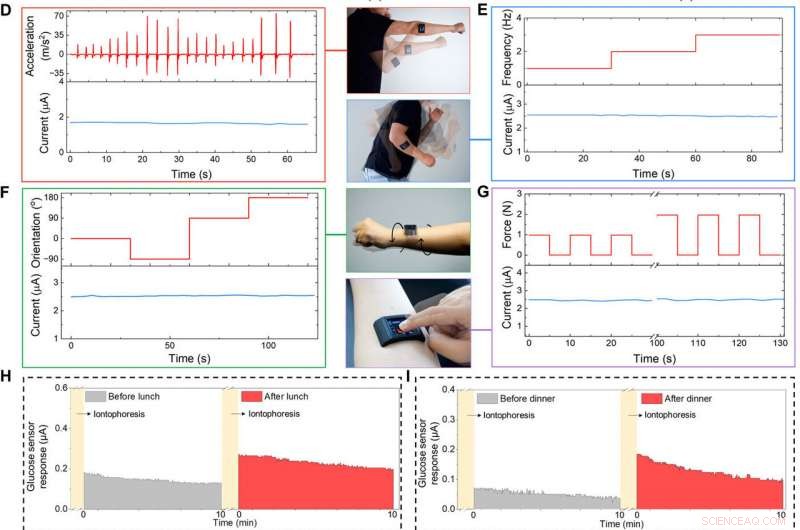
Op maat ontwikkelde FESS-geïntegreerde smartwatch voor toepassing op het lichaam. (A) Illustratie van de FESS-enabled smartwatch (met FESS, LCD scherm, printplaat, en batterijeenheden in een 3D-geprinte behuizing). (B en C) Ex situ karakterisering van de respons van het FESS-PCB glucosedetectiesysteem op vorticale trillingen (FESS-elektrode:6 mm2, hoogte microfluïdische kanaal:170 m, en volume:4 l). De trillingsversnellingsprofielen worden weergegeven in de bovenste helft, en de sensorreacties worden vastgelegd in de onderste helft wanneer getest in PBS (B) en 100 M glucose in PBS (C). (D tot G) Karakterisering van signaalgetrouwheid op het lichaam van een FESS-PCB lactaatdetectiesysteem met een onderwerp dat schaduwboksen uitvoert (D), arm zwaaien (E), pols draaien (F), en apparaat indrukken (G). De versnelling, frequentie, oriëntatie, en krachtprofielen worden weergegeven in de bovenste helft, en sensorreacties worden vastgelegd in de onderste helft. (H tot J) Monitoring van de metabolietprofielen van de proefpersonen door middel van verschillende dagelijkse gebeurtenissen en in verschillende instellingen. Iontoforetisch geïnduceerde zweetglucose werd gemeten voor en na de lunch (H) en het avondeten (I). (J) Zweetlactaatmetingen tijdens inspanning (een representatief bewegingsgeïnduceerd versnellingsprofiel wordt rechts weergegeven). (Fotocredit:Peterson Nguyen, Kaili Chiu, en Yichao Zhao, Universiteit van Californië, Los Angeles.) Krediet: wetenschappelijke vooruitgang , doi:10.1126/sciadv.aaz0007
Op deze manier, Yichao Zhao en collega's onderzochten de biomarker-informatieafgifteroute en herkenden bijna nul gespannen gebieden in een microfluïdische detectiemodule om een spanningsgeïsoleerd pad te ontwikkelen om de betrouwbaarheid van biomarkergegevens te behouden. Het dunnefilmsysteem dat de vrijstaande FESS-entiteit vormde, was bio-geïnspireerd door integrine-achtige functionaliteiten voor signaaltransductie en signaalinterconnectie via dubbelzijdige hechting. De FESS overbrugde op efficiënte wijze de huid en uitleeselektronica om informatie over biomarkers te verzamelen. Het team koppelde het FESS-systeem naadloos aan een op maat ontwikkelde smartwatch als draagbare biosensor om real-time biomarker-uitlezingen te bewaken tijdens de dagelijkse routine van een gebruiker. Om het in dit werk ontwikkelde prototype te commercialiseren, Zhao et al. toekomstige klinische onderzoeken voorstellen om op zweet gebaseerde biomarkermetingen in kaart te brengen en informatie te verkrijgen over de fysiologische status van de gebruikers. De voordelen van dit werk, inclusief hun gemakkelijke integratie met draagbare elektronica en high-fidelity-metingen kunnen worden gebruikt om grootschalige klinische onderzoeken uit te voeren.
© 2020 Wetenschap X Netwerk
 Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's Eiwitmoleculen in cellen functioneren als miniatuurantennes
Eiwitmoleculen in cellen functioneren als miniatuurantennes Wetenschappers bestuderen optische biopsietool die ziekte in seconden detecteert
Wetenschappers bestuderen optische biopsietool die ziekte in seconden detecteert Slim water kan helpen bij het terugwinnen van olie
Slim water kan helpen bij het terugwinnen van olie Wetenschappers maken eetbaar servies voor eenmalig gebruik gemaakt van appels
Wetenschappers maken eetbaar servies voor eenmalig gebruik gemaakt van appels
 10 geweldige groene steden
10 geweldige groene steden  Aanpassingen van de Emu
Aanpassingen van de Emu  Onderzoek onthult het verband tussen klimaatverandering, El Niño en de mogelijkheid voor meer extreme bosbranden
Onderzoek onthult het verband tussen klimaatverandering, El Niño en de mogelijkheid voor meer extreme bosbranden Barrièrerif financiering boost om roofzuchtige zeester aan te pakken
Barrièrerif financiering boost om roofzuchtige zeester aan te pakken Nederlanders sluiten EU's grootste gasveld vanwege aardbevingsgevaar
Nederlanders sluiten EU's grootste gasveld vanwege aardbevingsgevaar
Hoofdlijnen
- Wat is een Micel in Biochemie?
- Video:De aanval van invasieve soorten overleven
- Voors en tegens van Forensic Science
- Kluizenaar of niet? Wetenschappers gebruiken Twitter om spidervragen aan te pakken
- Waarom bevatten de testen veel glad ER?
- Onderzoekers krijgen voor het eerst een volledig beeld van eiwit achter tastzin
- Het verschil tussen Anaphase, Interphase, Metaphase en Prophase
- Nieuwe studie laat zien hoe mierenkolonies zich anders gedragen in verschillende omgevingen
- Neanderthalers waren eigenlijk prehistorische Picasso's
- Onderzoek toont aan hoe elektriciteitsetende microben elektronen gebruiken om koolstofdioxide te fixeren

- Een wetenschappelijk datingspel - biologen spelen RNA-eiwit matchmakers
- Een nieuwe manier om opeenvolgingen van chemische reacties te automatiseren
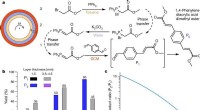
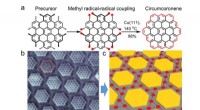
- Synthese op het oppervlak van grafeenmoleculen en hun superroosters
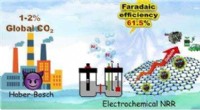
- Vooruitgang in de goedkope elektrochemische synthese van ammoniak
 Hoe een hoek te meten met een hoekmeter
Hoe een hoek te meten met een hoekmeter Een nieuwe dimensie in chemische nano-imaging
Een nieuwe dimensie in chemische nano-imaging Een achtbaan maken voor een schoolproject
Een achtbaan maken voor een schoolproject  bossen, koolstofputten, kan vertragingen bij het koolstofarm maken van de economie niet goedmaken:studie
bossen, koolstofputten, kan vertragingen bij het koolstofarm maken van de economie niet goedmaken:studie Studie helpt om het verband tussen binnen- en buitenluchtkwaliteit beter te begrijpen
Studie helpt om het verband tussen binnen- en buitenluchtkwaliteit beter te begrijpen Nummers afronden tot drie decimale plaatsen
Nummers afronden tot drie decimale plaatsen  Nanosensoren kunnen helpen bij het bepalen van het vermogen van tumoren om weefsel te hermodelleren
Nanosensoren kunnen helpen bij het bepalen van het vermogen van tumoren om weefsel te hermodelleren Hoe psychologisch eigenaarschap het rentmeesterschap voor publieke goederen kan verbeteren
Hoe psychologisch eigenaarschap het rentmeesterschap voor publieke goederen kan verbeteren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

