
Wetenschap
Polymeren te hulp! Cellen beschermen tegen beschadiging van ijs
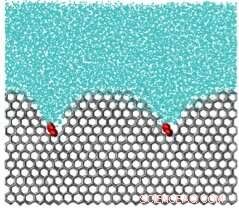
Een simulatie van een ijsremmend molecuul. het molecuul, in het rood, is als een gewicht op het oppervlak van het ijskristal, buigen en verdere groei van ijskristallen voorkomen. Krediet:Universiteit van Utah
Celtherapieën zijn veelbelovend voor een revolutie in de behandeling van kankers en auto-immuunziekten. Maar deze miljardenindustrie vereist langdurige opslag van cellen onder superkoude cryogene omstandigheden, terwijl ze ervoor zorgen dat ze blijven functioneren na ontdooien. Echter, deze koude temperaturen veroorzaken de vorming en groei van ijs, die cellen kunnen doorboren en verscheuren. Onderzoek gepubliceerd in de Tijdschrift van de American Chemical Society door de chemici van de Universiteit van Utah, Pavithra Naullage en Valeria Molinero, vormt de basis voor het ontwerpen van efficiënte polymeren die de groei van ijs kunnen voorkomen dat cellen beschadigt.
Antivries van de natuur
Huidige strategieën om cellen en organen te cryopreserveren, omvatten het baden ervan met grote hoeveelheden dimethylsulfoxide, een giftige chemische stof die de ijsvorming verpest, maar de cellen belast, waardoor hun overlevingskansen afnemen.
Natuur, echter, heeft een manier gevonden om organismen onder extreem koude omstandigheden in leven te houden:antivries-eiwitten. Vis, insecten en andere koudbloedige organismen hebben krachtige antivries-glycoproteïnen ontwikkeld die zich binden aan ijskristallieten en deze verhinderen te groeien en cellen te beschadigen.
Het groeiende gebied van op cellen gebaseerde therapieën vereist de ontwikkeling van krachtige remmers van ijsherkristallisatie die in activiteit kunnen concurreren met natuurlijke antivries-glycoproteïnen, maar die niet de kosten en toxiciteit hebben van dimethylsulfoxide. Deze vraag heeft de synthese van polymeren gestimuleerd die de werking van antivries-glycoproteïnen nabootsen. Maar de meest krachtige synthetische rekristallisatieremmer die tot nu toe is gevonden, polyvinylalcohol (PVA), is orden van grootte minder krachtig dan natuurlijke glycoproteïnen.
"Inspanningen om sterkere remmers voor ijsgroei te identificeren lijken tot stilstand te zijn gekomen, aangezien er nog geen moleculair begrip is van de factoren die de remmingsefficiëntie van ijsherkristallisatie van polymeren beperken, ' zegt Molinero.
Een verborgen ontwerpvariabele van polymeer
Hoe voorkomen moleculen dat ijskristallen groter worden? Moleculen die sterk aan ijs binden, spelden het oppervlak ervan, zoals stenen op een kussen, waardoor het ijsfront een gebogen oppervlak rond de moleculen ontwikkelt. Deze kromming destabiliseert het ijskristal, haar groei stoppen. Moleculen die langer aan ijs gebonden blijven dan de tijd die nodig is om ijskristallen te laten groeien, slagen erin om verdere groei en herkristallisatie te voorkomen.
Molinero en Naullage gebruikten grootschalige moleculaire simulaties om de moleculaire onderbouwing van hoe flexibiliteit, lengte en functionalisering van polymeren regelen hun binding aan ijs en hun efficiëntie om ijsgroei te voorkomen. Hun studie toont aan dat de gebonden tijd van de moleculen aan het ijsoppervlak wordt bepaald door de sterkte van hun ijsbinding in combinatie met de lengte van het polymeer en hoe snel ze zich voortplanten op het ijsoppervlak.
"We ontdekten dat de efficiëntie van flexibele polymeren bij het stoppen van de ijsgroei wordt beperkt door de langzame voortplanting van hun binding aan ijs, ' zegt Molinero.
De studie ontleedt de verschillende factoren die de binding van flexibele polymeren aan ijs regelen en die de kloof in potentie van PVA en natuurlijke antivries-glycoproteïnen verklaren. In een notendop, elk blok antivries-glycoproteïnen bindt sterker aan ijs dan PVA, en worden ook begunstigd door hun secundaire moleculaire structuur die de bindende en niet-bindende blokken scheidt, zodat ze sneller aan ijs kunnen hechten om de groei te stoppen.
"Voor zover we weten, dit werk is de eerste om de voortplantingstijd van binding te identificeren als een sleutelvariabele in het ontwerp van efficiënte ijsbindende flexibele polymeren, " zegt Naullage. "Onze studie vormt de basis voor het de novo ontwerp van flexibele polymeren die de efficiëntie van antivries-glycoproteïnen kunnen evenaren of zelfs overtreffen en een impact kunnen hebben op biomedisch onderzoek."
 Er is een grot in de vorm van een neushoorn in de staat Washington
Er is een grot in de vorm van een neushoorn in de staat Washington  Verwaterde biodiversiteit:het type monster is van cruciaal belang in milieu-DNA-onderzoeken voor biomonitoring
Verwaterde biodiversiteit:het type monster is van cruciaal belang in milieu-DNA-onderzoeken voor biomonitoring Bugs die eruit zien als sesamzaden
Bugs die eruit zien als sesamzaden  Onderzoek:impact van beleid ter beheersing van kwik neemt af met elke vijf jaar vertraging
Onderzoek:impact van beleid ter beheersing van kwik neemt af met elke vijf jaar vertraging Grote aardbeving 7.3 treft afgelegen Malukus in Oost-Indonesië
Grote aardbeving 7.3 treft afgelegen Malukus in Oost-Indonesië
Hoofdlijnen
- Hoe de wet van Sines
- Hoe een moleculaire schaar op de juiste plaats knipt
- Wat doen onze lichaamscellen met zuurstof?
- Wat zijn de kleine delen van het DNA die Code for a Trait?
- CRISPR-octrooioorlogen benadrukken het probleem van het verlenen van brede intellectuele eigendomsrechten voor technologie die publieke voordelen biedt
- Wetenschappers werken aan een omkeerbare vorm van genbewerking
- Stropers richten zich op Afrikaanse leeuwen, gieren met vergif
- Wetenschappers ontwikkelen aardnoot die resistent is tegen aflatoxine
- Wat gebeurt er met plantaardige en dierlijke cellen wanneer ze worden geplaatst in hypertone, hypotone en isotone omgevingen?
- Wetenschappers zetten stap richting efficiëntere brandstofraffinageprocessen
- Onderzoekers zien in realtime scheurvorming in 3D-geprint wolfraam

- de dodelijke, levengevende en voorbijgaande elementen die deel uitmaken van groep 15 van het periodiek systeem

- Onderzoekers gebruiken hele levende cellen als sjablonen om naar bioactieve moleculen te zoeken
- Nieuwe tool om polymeereigenschappen te voorspellen

 Zwaartekrachtkristallen:een nieuwe methode om de fysica van witte dwergsterren te onderzoeken
Zwaartekrachtkristallen:een nieuwe methode om de fysica van witte dwergsterren te onderzoeken Engineered microbe kan de sleutel zijn tot het produceren van plastic uit planten
Engineered microbe kan de sleutel zijn tot het produceren van plastic uit planten EPA dwingt VW om benzineverbruik op 98 te corrigeren, 000 voertuigen
EPA dwingt VW om benzineverbruik op 98 te corrigeren, 000 voertuigen Een nieuwe familiesuperrechtbank zal misschien geen tijd besparen of leiden tot betere oordelen
Een nieuwe familiesuperrechtbank zal misschien geen tijd besparen of leiden tot betere oordelen Flip-flop qubits:radicaal nieuw ontwerp voor kwantumcomputers uitgevonden
Flip-flop qubits:radicaal nieuw ontwerp voor kwantumcomputers uitgevonden Orkaan Isaias raast aan wal aan Amerikaanse oostkust
Orkaan Isaias raast aan wal aan Amerikaanse oostkust IBM-wetenschappers maken de kleinste 3D-kaart van planeet Aarde
IBM-wetenschappers maken de kleinste 3D-kaart van planeet Aarde Ongerept Lake Tahoe gehuld in rook van dreigend vuur
Ongerept Lake Tahoe gehuld in rook van dreigend vuur
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Norway | Spanish | Danish |

-
Wetenschap © https://nl.scienceaq.com

