
Wetenschap
enzymen nabootsen, scheikundigen produceren grote, nuttige koolstofringen
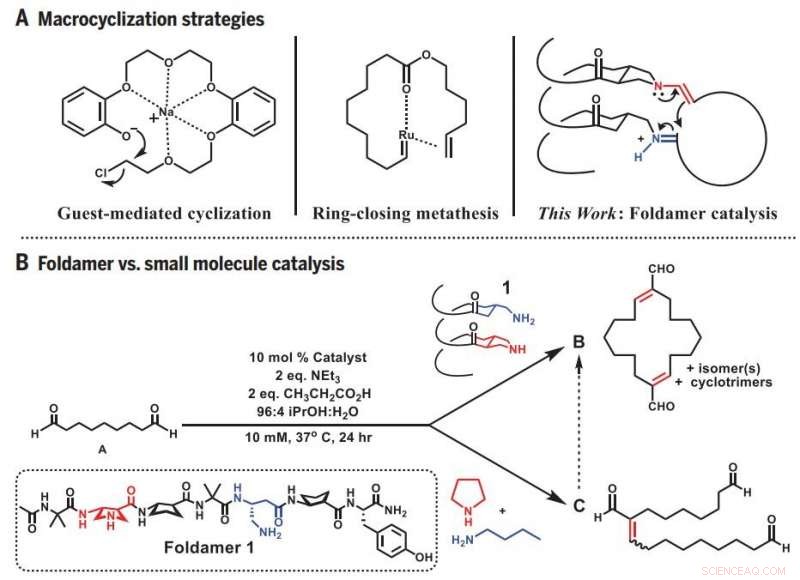
Macrocycliseringsstrategieën. (A) Voorafgaande benaderingen en foldameerbenadering van macrocyclisatie. (B) Uiteenlopende reactiviteit:Foldameer versus katalyse met kleine moleculen. vgl., equivalent(en). Credit: Wetenschap (2019).DOI:10.1126/science.aax7344
Inspiratie halen uit de natuur, Chemici van de University of Wisconsin-Madison hebben een efficiënte manier ontdekt om lang, kronkelende moleculen om grote ringen te vormen - ringen die de ruggengraat vormen van veel geneesmiddelen, maar die moeilijk te produceren zijn in het laboratorium.
Het werk kan een voorlopige vooruitgang betekenen in de richting van het ontcijferen van hoe enzymen, geperfectioneerd door evolutie, zo efficiënt natuurlijke verbindingen produceren. Meer onmiddellijk, de nieuwe methode kan onderzoekers helpen bij het synthetiseren van medicijnen met grote ringruggengraat, zoals die voor hepatitis. Het onderzoek is op 19 december gepubliceerd in het tijdschrift Wetenschap .
De natuur geeft de voorkeur aan de wanorde van een lange, flexibel molecuul in de orde van een stijve ring, waardoor het voor chemici notoir moeilijk is om grote ringen te laten vormen in het laboratorium. "Als de lineaire moleculen lang genoeg worden, het is alsof de uiteinden niet meer weten dat ze met elkaar verbonden zijn, en ze zullen net zo goed een binding aangaan met andere moleculen als dat ze samenkomen, " zegt UW-Madison hoogleraar chemie Sam Gellman, de hoofdauteur van het rapport.
Toch kunnen biologische enzymen deze uiteinden gemakkelijk bij elkaar brengen en ringen van alle groottes vormen. Ze bereiken deze prestatie dankzij hun complexe, driedimensionale vormen die fungeren als een gespecialiseerd slot - het lineaire molecuul past precies op zijn plaats als een sleutel op de juiste manier om een georganiseerde reactie te laten plaatsvinden.
Om zowel te bestuderen hoe enzymen werken als hun capaciteiten na te bootsen, Gellmans team werd veel kleiner, driedimensionale eiwitachtige moleculen, foldamers genaamd, die hun laboratorium heeft helpen ontwikkelen.
Omdat de foldameer een driedimensionale vorm heeft die zich aan de uiteinden van het flexibele precursormolecuul kan vastgrijpen, het vergroot de kans dat de uiteinden elkaar vinden enorm. Tegelijkertijd, de foldameer katalyseert de juiste reactie die de uiteinden in een gesloten ring verbindt. Het resultaat is een rechttoe rechtaan en voorspelbare synthese van een uitdagende, en nuttig, moleculaire vorm.
"Als chemici, we zien hoe buitengewoon effectieve enzymen zijn in het uitvoeren van reacties die moeilijk te bereiken zijn in een fles, maar we begrijpen niet echt hoe ze werken, ", zegt Gellman. "Als we leren hoe deze kleine foldameerkatalysatoren werken, we kunnen misschien katalysatoren bouwen die effectief zijn voor veel verschillende reacties. uiteindelijk, misschien kunnen we ons een weg banen naar Foldamers die echt enzym-achtige activiteit hebben."
Afgestudeerd student en hoofdauteur Zebediah Girvin begon het onderzoek door de mogelijkheden van een korte, spiraalvormige maper. Girvin probeerde de foldameer te gebruiken om een lineair molecuul met negen koolstofatomen te buigen, zodat het een ring zou vormen. Maar in plaats van een ring van de verwachte maat, Girvin kreeg er een die twee keer zo groot was - het resultaat van twee voorlopermoleculen die eerst samenkwamen en vervolgens de cirkel sloten.
"Dit is een veel voorkomende situatie in de wetenschap. Je probeert iets en het werkt niet zoals je had verwacht, ", zegt Gellman. "De uitdaging is om te herkennen wanneer het verrassende resultaat net zo interessant is als het oorspronkelijke doel, of nog interessanter."
Geleid door deze serendipiteit, Girvin begon te testen hoe goed de foldameer de grotere ringen kon produceren die hij het liefste maakte. Hij ontdekte dat hij gemakkelijk ringen kon maken die bestonden uit 12 tot 22 koolstofatomen wanneer de reactieve plaatsen van de foldameer, waar de ringsluiting plaatsvindt, stonden aan één kant naast elkaar. Deze oriëntatie bracht de twee uiteinden van diverse lineaire moleculen dicht genoeg bij elkaar om te fuseren.
Als proof-of-concept voor de nieuwe techniek, Girvin synthetiseerde het natuurlijke product robustol helemaal opnieuw. Afgeleid van de bladeren van de Australische zijde-eik, robustol weegt met een forse 22-atoom ring.
Het team van Gellman is zeer enthousiast over het potentieel voor Foldamers om andere nuttige reacties te katalyseren en mogelijk te helpen bij het ontrafelen van al lang bestaande mysteries over hoe enzymen, de chemische virtuozen van de natuur, produceer de moleculen die nodig zijn voor het leven door simpelweg aminozuurbouwstenen in de juiste vorm te ordenen. Hoewel die antwoorden jaren weg zijn, de ringsluitingstechniek die ze hebben ontdekt, zou meer onmiddellijk kunnen worden gebruikt om kandidaat-geneesmiddelen te synthetiseren. Het hepatitis C-medicijn vaniprevir, die wordt gebruikt in Japan en in latere proeven in de VS, bevat precies dit soort grote ring.
Het echte potentieel van foldermakers komt voort uit hun diversiteit. Chemici kunnen in het lab een bijna oneindige verscheidenheid aan foldameren maken, omdat ze toegang hebben tot meer bouwstenen dan in natuurlijke eiwitten voorkomen. Dit zou scheikundigen in staat kunnen stellen meer bruikbare katalysatoren te bouwen, wat ertoe leidde dat Gellman bepaalde foldamers patenteerde en het bedrijf Longevity Biotech oprichtte om hun therapeutische toepassingen te onderzoeken.
Vooruit gaan, die rijkdom aan opties stelt onderzoekers in staat om deze katalysatoren in vormen te rangschikken die op onverwachte manieren nuttig kunnen zijn. Alleen meer onderzoek zal het uitwijzen.
"We weten nog niet echt waartoe deze katalysatoren in staat zijn, ", zegt Girvin. "Het zal jaren duren om hun potentieel te ontdekken, en het is belangrijk dat we een breed net werpen en een open geest houden over wat we kunnen bereiken met deze nieuwe tools."
 Wat zijn enkele interessante feiten over Stratus Clouds?
Wat zijn enkele interessante feiten over Stratus Clouds?  Groot sequoiabos in particulier bezit wordt bewaard in een deal van $ 24,7 miljoen
Groot sequoiabos in particulier bezit wordt bewaard in een deal van $ 24,7 miljoen Mammoetveld wakkert Noorse olie-industrie aan
Mammoetveld wakkert Noorse olie-industrie aan Studie lokaliseert de oorsprong van gletsjerroetvervuiling in Noord-India
Studie lokaliseert de oorsprong van gletsjerroetvervuiling in Noord-India Voorgestelde grensmuur zal planten en dieren in Texas schaden, wetenschappers zeggen:
Voorgestelde grensmuur zal planten en dieren in Texas schaden, wetenschappers zeggen:
Hoofdlijnen
- Wanneer dupliceren chromosomen tijdens een levenscyclus van cellen?
- Genoomonderzoek daagt eerder begrip van de oorsprong van fotosynthese uit
- Studie suggereert nieuwe doelen voor het verbeteren van het sojaoliegehalte
- Wetenschappers rapporteren chemische basis van de celdelingstimer, een mogelijk doelwit tegen kanker
- Wanneer werden DNA-testen het eerst gebruikt?
- Wetenschappers ontdekken dat schorpioenen zich richten op hun gif
- Opnieuw geïntroduceerde buideldieren kunnen een nieuwe bedreiging vormen voor op de grond levende vogels
- Verschil tussen recombinant DNA en genetische manipulatie
- Bij-nabootsende kaalvleugelmot zoemt na 130 jaar weer tot leven
- Huidvaccinatie met micronaaldpleister, influenzafusie-eiwit verbetert de werkzaamheid van griepvaccins

- MiNT-eiwit een nieuw doelwit om ziekte aan te vallen
- Probes werpen nieuw licht op de oorzaak van Alzheimer

- Nieuwe biochemische route die meer veerkrachtige gewasvariëteiten kan ontwikkelen

- Nieuw voorgestelde strategie biedt slimme flexibele neurale elektrode met hoge efficiëntie
 China, Europa neemt het voortouw op het gebied van klimaat terwijl de wereld op Trump wacht
China, Europa neemt het voortouw op het gebied van klimaat terwijl de wereld op Trump wacht Hoe leeftijd berekenen in maanjaren
Hoe leeftijd berekenen in maanjaren Kwadratische vergelijkingen schrijven Gegeven een Vertex & Point
Kwadratische vergelijkingen schrijven Gegeven een Vertex & Point Schuurpapier vijgen maken voedsel, vuur, medicijn en een knus huis voor wespen
Schuurpapier vijgen maken voedsel, vuur, medicijn en een knus huis voor wespen Pas op hoe je de huidige AI behandelt:het kan in de toekomst wraak nemen
Pas op hoe je de huidige AI behandelt:het kan in de toekomst wraak nemen Onderzoek toont aan dat milieuvriendelijk servies schadelijk is voor zeedieren
Onderzoek toont aan dat milieuvriendelijk servies schadelijk is voor zeedieren Grootste moleculaire spin gevonden in de buurt van een kwantumfaseovergang
Grootste moleculaire spin gevonden in de buurt van een kwantumfaseovergang Onder de oppervlakte kijken - steden leefbaarder maken
Onder de oppervlakte kijken - steden leefbaarder maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

