Wetenschap
Huidvaccinatie met micronaaldpleister, influenzafusie-eiwit verbetert de werkzaamheid van griepvaccins
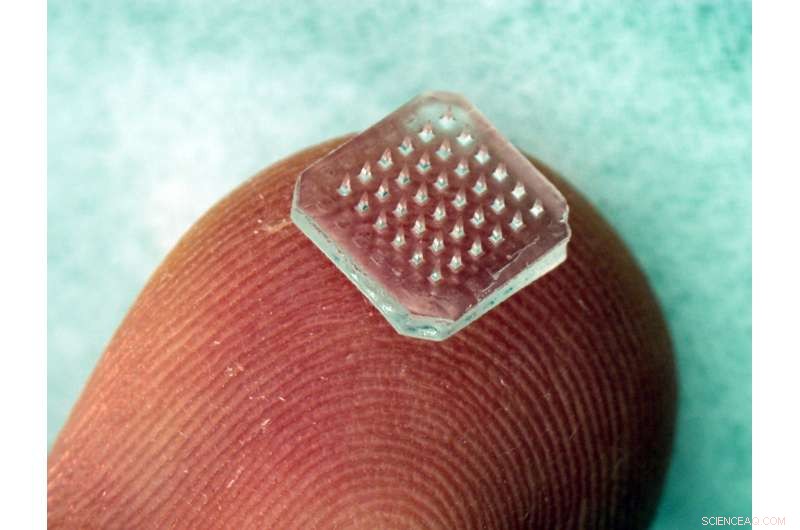
Krediet:Georgia State University
Een stimulerende huidvaccinatie met een biologisch afbreekbare micronaaldpleister en eiwit opgebouwd uit sequenties van subtypes van het influenzavirus zou de effectiviteit van conventionele influenzavaccins kunnen verbeteren, Dat blijkt uit een onderzoek onder leiding van de Georgia State University.
Om de bescherming van standaard griepvaccins te vergroten, De groep van Dr. Baozhong Wang maakte een fusie-eiwit (4M2e-tFliC) met vier verschillende sequenties van M2e van vier verschillende subtypes van influenza. M2e is een peptide, een verbinding van twee of meer aminozuren die in een keten zijn verbonden, gevonden bij alle griepstammen. Het fusie-eiwit bevat ook flagelline (FliC), een peptide dat in bijna alle bacteriën met flagella (wimperachtige aanhangsels) wordt aangetroffen en dat als een sterke katalysator werkt wanneer het samen met andere antigenen wordt toegediend, of vreemde stoffen die een immuunrespons in het lichaam opwekken.
De onderzoekers condenseerden het eiwit in de micronaaldpleister door een samenwerking met Dr. Mark R. Prausnitz van het Georgia Institute of Technology. De micronaaldpleister is gemaakt van een biocompatibel polymeer, en de kleine naalden die op de pleister zijn aangebracht, lossen op en geven het vaccin snel af in de huid.
Uit de studie bleek dat muizen een conventioneel geïnactiveerd vaccin kregen, een vaccin dat bestaat uit ziekteverwekkers die in cultuur zijn gekweekt en vervolgens worden gedood, gevolgd door een op de huid aangebrachte, oplossende 4M2e-tFliC-micronaaldpleister-boost kon de humorale immuniteitsantilichaamrespons tegen influenzavirusinfectie beter handhaven in vergelijking met wanneer ze alleen het conventionele vaccin kregen. De bevindingen, gepubliceerd in de Tijdschrift voor gecontroleerde afgifte , bieden een nieuw perspectief voor universele griepvaccins.
"Onze studie toont aan dat op M2e gebaseerde vaccins de immuunrespons aanzienlijk verbeteren en de beschermende functies tegen influenzavirusinfectie versterken, " zei Wang, universitair hoofddocent aan het Instituut voor Biomedische Wetenschappen van de staat Georgia. "We ontdekten dat een op de huid aangebrachte 4M2e-tFliC-micronaaldpleister de immunisatie van ontvangers van seizoensvaccins verhoogde en een snelle benadering kan zijn om de beschermende werkzaamheid van seizoensvaccins te verhogen als reactie op uitdagingen met het griepvirus. het M2e-antigeen is een veelbelovende kandidaat voor de ontwikkeling van universele griepvaccins."
Het griepvirus is een van de ernstigste respiratoire pathogenen die mensen treft en veroorzaakt ongeveer vijf miljoen ziekten en 250, 000 tot 500, 000 doden per jaar wereldwijd. Geschat wordt dat een plotselinge opkomst van een grieppandemie wereldwijd ongeveer 60 miljoen mensen kan doden.
Vaccinatie is een effectieve methode om infectie met het influenzavirus te voorkomen, maar circulerende virussen kunnen snel antigene veranderingen ondergaan, of kleine veranderingen in de genen van influenzavirussen die in de loop van de tijd optreden als het virus zich vermenigvuldigt, die de werkzaamheid van seizoensgriepvaccins kunnen verminderen of elimineren. Om een grieppandemie veroorzaakt door antigene drift te bestrijden, een snelle, een kostenefficiënte vaccinatiemethode is vereist om een bredere kruisbescherming te bieden tegen seizoens- en pandemische influenzavirusinfecties en om de immuniteit op lange termijn te bevorderen.
De biologisch afbreekbare micronaaldpleister, die is ontworpen om vaccins af te geven in de epidermis en dermis van de huid, is een nieuwe technologie voor de toediening van vaccins en zou het vermogen van het vaccin om een immuunrespons in het lichaam uit te lokken, kunnen verbeteren. De huid is een krachtige plek voor vaccinatie omdat ze een overvloed aan bloedvaten en lymfevaten heeft, evenals veel verschillende soorten immuuncellen. Ook, veel cellen in de huid brengen TLR5 tot expressie, een receptor voor FliC die het aangeboren immuunsysteem activeert. Door de huidafgifte van het M2e-antigeen te combineren met tFliC als katalysator, ontstaat een sterke synergie.
In dit onderzoek, muizen werden geïmmuniseerd met geïnactiveerde griepvaccins, en vier weken later kregen ze een van de volgende stimulerende immunisaties:intramusculaire injectie van 4M2e-tFliC-fusie-eiwit, micronaaldpleister huidvaccinatie van 4M2e-tFliC of een placebo micronaaldpleister zonder het antigeen.
De onderzoekers testten of een 4M2e-tFliC-verhogende immunisatie de immuunresponsen zou kunnen beïnvloeden die worden veroorzaakt door geïnactiveerde griepvaccins. De muizen werden uitgedaagd met H1N1- en H3N2-influenzavirussen en werden gedurende 14 dagen dagelijks gecontroleerd op veranderingen in lichaamsgewicht en overleving. De niveaus van influenzavirustiters in de longen van dieren waarvan het lichaam antistoffen tegen het influenzavirus had opgebouwd, werden gemeten, en bloedmonsters, longen, milten en beenmerg werden verzameld en verwerkt.
Muizen die de micronaaldpleister-boost kregen, vertoonden een significant verbeterde overleving en cellulaire immuunresponsen. De resultaten gaven ook aan dat huidvaccinatie met 4M2e-tFliC een langdurige antilichaam-gemedieerde immuniteit bevorderde.
 Zout smelt geen ijs - zo maakt het de winterse straten echt veilig
Zout smelt geen ijs - zo maakt het de winterse straten echt veilig Wetenschappers suggereren een milieuvriendelijke manier om zeer actieve katalysatoren te verkrijgen
Wetenschappers suggereren een milieuvriendelijke manier om zeer actieve katalysatoren te verkrijgen Onderzoekers regenereren gedeactiveerde katalysator in het proces van methanol tot olefinen
Onderzoekers regenereren gedeactiveerde katalysator in het proces van methanol tot olefinen Onderzoekers ontwikkelen nieuwe manier om verontreinigende stoffen uit water te verwijderen
Onderzoekers ontwikkelen nieuwe manier om verontreinigende stoffen uit water te verwijderen Methanolsynthese:inzicht in de structuur van een raadselachtige katalysator
Methanolsynthese:inzicht in de structuur van een raadselachtige katalysator
Hoofdlijnen
- Hoe zal klimaatverandering de arctische kariboes en rendieren beïnvloeden?
- Goudvinken blijven jarenlang bij elkaar
- Nieuwe technologie verlicht microben die niet in een laboratorium kunnen worden gekweekt
- Wat zijn de rollen van chlorofyl A & B?
- Wat is een prehistorische toolkit en hoe zou het de menselijke geschiedenis kunnen herschrijven?
- Wit vlees of donker vlees? Big data serveren om het Thanksgiving-diner te ontcijferen
- Burgerwetenschap kan de betrokkenheid en het begrip bij niet-gegradueerde biologielessen vergroten
- Hoe antidepressiva werken
- De zoektocht naar de zuidelijke rubberboa
 Dierencollectieven zoals mieren zouden zich als slimme gokkers door hun omgeving moeten bewegen
Dierencollectieven zoals mieren zouden zich als slimme gokkers door hun omgeving moeten bewegen NASA-ruimtevaartuig arriveert bij oude asteroïde, zijn eerste bezoeker
NASA-ruimtevaartuig arriveert bij oude asteroïde, zijn eerste bezoeker Onderzoekers bestuderen muggenplaag in afvalwaterzuiveringsinstallaties in Ohio
Onderzoekers bestuderen muggenplaag in afvalwaterzuiveringsinstallaties in Ohio Wetenschappers ontwikkelen eerste kwantumalgoritme om ruis in grote systemen te karakteriseren
Wetenschappers ontwikkelen eerste kwantumalgoritme om ruis in grote systemen te karakteriseren Hier is een tip die banken fenomenaal succesvol kan maken:radicale eerlijkheid
Hier is een tip die banken fenomenaal succesvol kan maken:radicale eerlijkheid Lanceervenster versmalt voor SpaceXs monsterraket (update)
Lanceervenster versmalt voor SpaceXs monsterraket (update) Hoe zal de bevolkingsgroei van invloed zijn op energie?
Hoe zal de bevolkingsgroei van invloed zijn op energie?  Hoe bomen te redden:het draait allemaal om conflictoplossing
Hoe bomen te redden:het draait allemaal om conflictoplossing
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com