
Wetenschap
Nieuwe technologie voor eiwitbioconjugatie en structurele proteomics
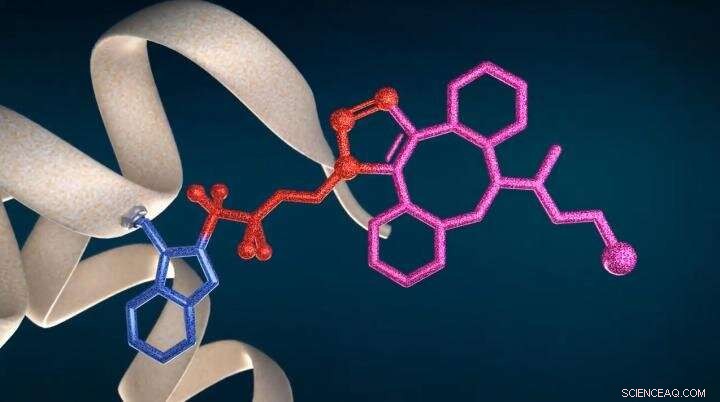
Nieuwe technologie CF LINK voor eiwitbioconjugatie en structurele proteomics Credit:IOCB Prague (Bron:youtu.be/a9IMvKv0UQU)
Onderzoekers van de Tsjechische Academie van Wetenschappen en de in Brno gevestigde start-up CF Plus Chemicals, een spin-off van ETH Zürich, heeft een nieuwe technologie gemeld, CF LINK genaamd, voor plaatsselectieve bioconjugatie van eiwitten en hun structurele karakterisering. De technologie kan selectief eiwitconjugaten bereiden via hun tryptofaanresiduen en post-translationele modificatie van aromatische aminozuren uitvoeren. Verder, het kan ook worden gebruikt als een hulpmiddel voor het in kaart brengen van eiwitoppervlakken en studies van eiwit-eiwitinteracties.
Het bedrijf CF Plus Chemicals, een spin-off van ETH Zürich, opgericht in 2014, is gebaseerd op bijna 10 jaar samenwerking van de groep van Dr. Petr Beier aan het Instituut voor Organische Chemie en Biochemie van de Tsjechische Academie van Wetenschappen (IOCB Praag) en Dr. Václav Matoušek, een doctoraat alumnus van Prof. Dr. Antonio Togni aan de ETH Zürich.
Reagentia op basis van cyclische hypervalente jodium-perfluoralkylverbindingen, ook wel Togni-reagentia genoemd, zijn veelgebruikte en populaire hulpmiddelen geworden in de organische synthese, vooral in medicinale chemie voor de bereiding van nieuwe gefluoreerde kandidaat-geneesmiddelen, in lijn met de groeiende vraag naar gefluoreerde steigers bij het ontwerpen van geneesmiddelen. In het begin van de jaren negentig, gefluoreerde moleculen waren goed voor 5 procent van het totale aantal goedgekeurde geneesmiddelen; ze omvatten nu 15 procent, en ongeveer 30 procent voor nieuw goedgekeurde therapieën.
Deze familie van chemische verbindingen werd vervolgens in 2013 uitgebreid in samenwerking met ETH Zürich en Dr. Petr Beier van IOCB tot een nieuwe generatie gepatenteerde Togni-reagentia die een complexere RCF2CF2-groep dragen in plaats van een eenvoudige CF3-groep. De nieuwe familie van deze chemicaliën deelt niet alleen de rijke reactiviteit van de eerste generatie Togni-reagentia, maar vertonen ook vrijwel onbeperkte structurele variabiliteit van de β-gesubstitueerde tetrafluorethylgroep, die ze kunnen overbrengen naar een verscheidenheid aan substraten die relevant zijn voor de medische chemie van kleine moleculen.
in 2017, het toepassingspotentieel van de tweede generatie Togni-reagentia werd uitgebreid tot eiwitten. Hun hoge affiniteit voor de thiolgroep maakt selectieve bioconjugatie door cysteïnen mogelijk om stabiele conjugaten te vormen die, in tegenstelling tot maleïmideconjugaten, zijn niet onderhevig aan langzame deconjugatie en thioluitwisseling.
De onderhavige uitvinding bouwt voort op de eerdere kennis van de radicale aard van Togni-reagens-gemedieerde reacties. In het MKB Instrument Horizon 2020-project, ondersteund door de stad Brno en in samenwerking met IOCB en Dr. Petr Novák van het Instituut voor Microbiologie van de Tsjechische Academie van Wetenschappen (IMIC), er werd aangetoond dat Togni-reagentia, wanneer gemengd met natriumascorbaat, een goedkope, niet-toxisch en biocompatibel reductiemiddel, genereren onmiddellijk ß-gesubstitueerde tetrafluorethylradicalen die selectief hechten aan sterisch toegankelijke tryptofaanresten van het eiwit onder overgangsmetaalvrije omstandigheden.
Zodra azidofluoralkylgroepen aan het eiwit zijn gehecht, verschillende functionele groepen, zoals fluorescerende kleurstoffen, radionucliden of ADC-toxinen voor gerichte oncotherapie kunnen vervolgens via klikreactie worden gekoppeld om de overeenkomstige eiwitconjugaten te verkrijgen. De beschreven tryptofaan-selectieve bioconjugatiemethode verstoort de eiwitdisulfidebruggen niet en biedt een alternatieve oplossing waar conventionele cysteïneconjugatie niet mogelijk is, bijvoorbeeld, als gevolg van een ongewenste disulfide-scramblering.
Deze bioconjugatiemethode kan ook worden uitgebreid naar andere aromatische aminozuren en dus naar eiwitten zonder tryptofaan. Dus, het was mogelijk om humane recombinante insuline met succes te modificeren en tot zeven modificaties aan zijn aromatische aminozuren te koppelen, het aantonen van het potentieel voor post-translationele modificatie van eiwitten.
De extreem snelle aard van deze reactie, gericht op voor oplosmiddel toegankelijke aromatische aminozuren, maakt het een handig hulpmiddel voor het in kaart brengen van eiwitoppervlakken en het bestuderen van eiwit-eiwit-interacties. Gebruikmakend van het voorbeeld van menselijk koolstofanhydrase, de onderzoekers toonden aan dat de resultaten van het in kaart brengen van het oppervlak in uitstekende overeenstemming zijn met de gepubliceerde oorspronkelijke structuur.
Prof. Dr. Martin Fusek, CEO van IOCB Tech, zegt, "De basis van succesvolle commerciële resultaten van basisonderzoeksresultaten is uitstekend wetenschappelijk werk. Dit is een belangrijk resultaat dat niet alleen nuttig is als hulpmiddel voor fundamenteel onderzoek, maar ook als middel voor de ontwikkeling van nieuwe op eiwitten gebaseerde medicijnen. Het unieke, wat eerder de regel zou moeten zijn, is dat het project tot stand is gekomen door de samenwerking van twee academische instellingen en een commercieel bedrijf. Ik ben erg blij dat we deel hadden kunnen uitmaken van het proces."
Dr. Petr Beier, hoofd van een onderzoeksgroep bij IOCB Praag, zegt, "Ik ben blij dat we een succesvolle interdisciplinaire samenwerking van organische synthese en biochemie hebben kunnen ontwikkelen. Het blijkt dat de specifieke eigenschappen van gefluoreerde verbindingen niet alleen traditioneel kunnen worden gebruikt in de medische chemie van kleine moleculen, maar zoals onlangs ook aangetoond voor bioconjugatie van eiwitten en studies van hun structuur. Ik geloof dat we in de toekomst andere aantrekkelijke toepassingen van Togni-reagentia in de biochemie zullen kunnen identificeren."
Dr. Petr Novák, hoofd van een onderzoeksgroep bij IMIC, zegt, "Dankzij Togni-reagentia zijn we in staat geweest om binnen enkele seconden een gefluoreerde sonde in de eiwitstructuur in een waterige omgeving te introduceren. We zijn nu in staat om deze technologie te gebruiken om eiwitten selectief te labelen voor klinische diagnostiek of om deze te gebruiken om te identificeren de interactie-interface van eiwitten met hun liganden."
Dr. Václav Matousek, CEO van CF Plus Chemicals, zegt, "Ik ben verheugd om te zien dat de reactiviteit van Togni-reagentia kan worden uitgebreid tot aromatische aminozuren en aromaten in het algemeen, waardoor een overvloed aan potentiële toepassingen wordt geopend, vooral in eiwitwetenschap en op eiwit gebaseerde therapieën. We zijn nu actief op zoek naar gevestigde industriële partners die onze technologie kunnen toepassen om hun uitdagingen op te lossen."
 Techniek om medicijnen te maken zonder bijwerkingen
Techniek om medicijnen te maken zonder bijwerkingen Wat is de chemische formule van ozon en hoe wordt ozon gevormd in de atmosfeer?
Wat is de chemische formule van ozon en hoe wordt ozon gevormd in de atmosfeer?  Waarom poppen ballonnen wanneer ze in een hete auto worden achtergelaten?
Waarom poppen ballonnen wanneer ze in een hete auto worden achtergelaten?  Schone waterstof maken is moeilijk, maar onderzoekers hebben zojuist een grote hindernis opgelost
Schone waterstof maken is moeilijk, maar onderzoekers hebben zojuist een grote hindernis opgelost Onderzoekers hebben een nieuwe draai aan asymmetrische katalyse
Onderzoekers hebben een nieuwe draai aan asymmetrische katalyse
 A-68A ijsberg dunner met 2,5 cm per dag
A-68A ijsberg dunner met 2,5 cm per dag Sprankelende bronnen helpen bij zoektocht naar ondergrondse warmte-energiebronnen
Sprankelende bronnen helpen bij zoektocht naar ondergrondse warmte-energiebronnen Door thuisblijvende bestellingen wordt de blootstelling aan lawaai bijna gehalveerd
Door thuisblijvende bestellingen wordt de blootstelling aan lawaai bijna gehalveerd Wat eet Minnows?
Wat eet Minnows?  Wat de grootteverdeling van organismen ons vertelt over de energetische efficiëntie van een meer
Wat de grootteverdeling van organismen ons vertelt over de energetische efficiëntie van een meer
Hoofdlijnen
- Combinatie van warmer water, blootstelling aan chemicaliën versterkt schadelijke effecten bij een kustvis
- Studie vindt variatie binnen soorten een cruciaal aspect van biodiversiteit
- Chili vecht om een favoriete mossel te redden
- Onderzoekers creëren nieuwe letters om DNA-functies te verbeteren
- Wat zijn de twee hoofdfasen van de celcyclus?
- Waarom gifkikkers zichzelf niet vergiftigen?
- Ontdekking van een potentieel therapeutisch doelwit om trypanosomen te bestrijden
- Onderzoek toont aan dat walvissen, al een bedreigde diersoort, kan een vage toekomst tegemoet gaan
- Maïsplaag maakt gebruik van plantafweerstoffen om zichzelf te beschermen
- Een nieuwe katalysator voor energierijke aluminium-luchtstroombatterijen

- Wearables en apparaten voor schimmels:biomaterialen maken de weg vrij voor de toekomst van sciencefiction

- Vijf kenmerken van een chemische verandering

- Video:De toevallige ontdekking van LSD

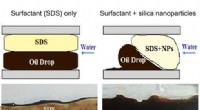
- Nieuwe materialen met belangrijke toepassingen in verbeterde oliewinning
 Onderzoek onthult belemmeringen voor het vergroten van diversiteit in vrijwilligersorganisaties
Onderzoek onthult belemmeringen voor het vergroten van diversiteit in vrijwilligersorganisaties Zeldzaam ijzermineraal uit rotsen gevonden in weekdiertanden
Zeldzaam ijzermineraal uit rotsen gevonden in weekdiertanden Remedie tegen superbacteriën gevonden in kraaiheide
Remedie tegen superbacteriën gevonden in kraaiheide Wetenschappers stellen mogelijke mechanismen voor om coronale mini-jets in geactiveerde tornado-achtige prominentie te verklaren
Wetenschappers stellen mogelijke mechanismen voor om coronale mini-jets in geactiveerde tornado-achtige prominentie te verklaren Levenscyclus van de Okapi
Levenscyclus van de Okapi  Detectie van 5-MeV-protonen met behulp van een flexibel organisch dunnefilmapparaat
Detectie van 5-MeV-protonen met behulp van een flexibel organisch dunnefilmapparaat Hogere frequentie van financiële rapportage belemmert bedrijfsinnovatie
Hogere frequentie van financiële rapportage belemmert bedrijfsinnovatie Wetenschappers lossen een halve eeuw oud magnesiumdimeermysterie op
Wetenschappers lossen een halve eeuw oud magnesiumdimeermysterie op
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Swedish | German | Dutch | Norway | Portuguese | Danish |

-
Wetenschap © https://nl.scienceaq.com

