
Wetenschap
Genenschaar gebruiken om ziekten op te sporen

In een onderzoek, onderzoekers van de Universiteit van Freiburg introduceren de eerste elektrochemische CRISPR-biosensor die de diagnose van ziekten zoals kanker moet helpen verbeteren. Krediet:Richard Bruch
CRISPR/Cas-technologie kan meer doen dan genen veranderen. Een onderzoeksteam van de Universiteit van Freiburg gebruikt de zogenaamde genenschaar - waarmee wetenschappers genetisch materiaal kunnen bewerken - om ziekten zoals kanker beter te diagnosticeren. In een onderzoek, introduceren de onderzoekers een microfluïdische chip die kleine stukjes RNA herkent, sneller en nauwkeuriger een specifiek type kanker aan te duiden dan de tot nu toe beschikbare technieken. De resultaten zijn onlangs gepubliceerd in het wetenschappelijke tijdschrift Geavanceerde materialen .
Ze testten de CRISPR-biosensor ook op bloedmonsters van vier kinderen bij wie hersentumoren waren vastgesteld. "Onze elektrochemische biosensor is vijf tot tien keer gevoeliger dan andere toepassingen die CRISPR/Cas gebruiken voor RNA-analyse, " legt Freiburg microsysteemingenieur Dr. Can Dincer uit. Hij leidt het onderzoeksteam samen met bioloog Prof. Dr. Wilfried Weber, van de Universiteit van Freiburg. "We doen pionierswerk in Duitsland en Europa voor deze nieuwe toepassing van genenschaar, ’ benadrukt Dincer.
Korte moleculen bekend als microRNA (miRNA) worden gecodeerd in het genoom, maar in tegenstelling tot andere RNA-sequenties, ze worden niet vertaald in eiwitten. Bij sommige ziekten, zoals kanker of de neurodegeneratieve ziekte, Alzheimer, verhoogde niveaus van miRNA kunnen worden gedetecteerd in het bloed. Artsen gebruiken miRNA's al als biomarker voor bepaalde soorten kanker. Alleen de detectie van een groot aantal van dergelijke signaalmoleculen maakt een geschikte diagnose mogelijk. De onderzoekers werken nu aan een versie van de biosensor die tot acht verschillende RNA-markers tegelijk herkent.
De CRISPR-biosensor werkt als volgt:Een druppel serum wordt gemengd met reactieoplossing en op de sensor gedruppeld. Als het het doel-RNA bevat, dit molecuul bindt zich met een eiwitcomplex in de oplossing en activeert de genenschaar - op een manier die vergelijkbaar is met een sleutel die een deurslot opent. Zo geactiveerd, het CRISPR-eiwit valt af, of klieft, de reporter-RNA's die zijn gehecht aan signaalmoleculen, het opwekken van een elektrische stroom. De splitsing resulteert in een vermindering van de stroomsignalen die elektrochemisch kunnen worden gemeten en geeft aan of het gezochte miRNA in het monster aanwezig is.
"Het bijzondere aan ons systeem is dat het werkt zonder de replicatie van miRNA, want in dat geval gespecialiseerde apparaten en chemicaliën nodig zouden zijn. Dat maakt ons systeem goedkoop en aanzienlijk sneller dan andere technieken of methoden, " legt Dincer uit. Hij werkt aan nieuwe sensortechnologieën bij het Freiburg Center for Interactive Materials and Bioinspired Technologies (FIT) en samen met Prof. Dr. Gerald Urban bij de afdeling Microsystems Engineering (IMTEK).
Weber, een professor in synthetische biologie aan het excellentiecluster CIBSS - het Centre for Integrative Biological Signalling Studies van de Universiteit van Freiburg - benadrukt hoe belangrijk de interdisciplinaire omgeving bij CIBSS is voor een dergelijke ontwikkeling:"De biologen van Freiburg werken samen aan deze technologieën met hun collega's uit de ingenieurs- en materiaalwetenschappen. Dat opent nieuwe, spannende routes naar oplossingen."
De onderzoekers streven ernaar het systeem in ongeveer vijf tot tien jaar verder te ontwikkelen om de eerste snelle test voor ziekten te worden met gevestigde microRNA-markers die direct bij de dokter kunnen worden gebruikt. "De laboratoriumapparatuur moet toch hanteerbaarder worden, ' zegt Weber.
 Lijst met insecten met onvolledige metamorfose
Lijst met insecten met onvolledige metamorfose  Pesticiden kunnen gewassen beschermen tegen hydrofobe verontreinigende stoffen
Pesticiden kunnen gewassen beschermen tegen hydrofobe verontreinigende stoffen Vluchten geannuleerd tijdens de ergste zandstorm in China in tien jaar
Vluchten geannuleerd tijdens de ergste zandstorm in China in tien jaar Waarom sommige mensen niet evacueren:FEMA-onderzoek
Waarom sommige mensen niet evacueren:FEMA-onderzoek NASA's aquasatelliet vindt een zwakkere Chantal, nu een depressie
NASA's aquasatelliet vindt een zwakkere Chantal, nu een depressie
Hoofdlijnen
- Genezing van verbrande poten met vissenhuid
- Onderzoek toont aan dat honden slimmer zijn dan katten
- Wat zijn de chemische zintuigen?
- Explosie van ratten, klaverblaadjes, bedmijt, muggen onbedoeld evolutionair gevolg van verstedelijking
- Deze 8 foto's van puppy's kunnen je helpen focussen,
- Walvissen en dolfijnen hebben rijke mensachtige culturen en samenlevingen
- Hebben vogelgezang en menselijke spraak biologische wortels?
- Is de behoefte aan privacy evolutionair?
- Verschil tussen bacteriële en plantencelwand
- Techniek versnelt chemische screening om prioriteit te geven aan toxiciteitstesten

- Cementvrij beton verslaat corrosie en geeft fatbergs de flush

- Wetenschappers stellen nieuwe strategie voor elektrochemische reductie van kooldioxide voor
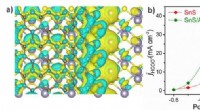
- Kleurveranderingstest om kankeronderzoek vooruit te helpen
- Onderzoekers lossen 60 jaar oude puzzel op over superhard materiaal
 Wat is de pH van natriumcarbonaat in water?
Wat is de pH van natriumcarbonaat in water?  Ja, mensen putten de hulpbronnen van de aarde uit, maar schattingen van de voetafdruk vertellen niet het volledige verhaal
Ja, mensen putten de hulpbronnen van de aarde uit, maar schattingen van de voetafdruk vertellen niet het volledige verhaal Minder duur produceren, groenere waterstofperoxide
Minder duur produceren, groenere waterstofperoxide Onderzoekers vinden dat molybdeniet mogelijk beter geschikt is voor geïntegreerde logische circuits dan grafeen
Onderzoekers vinden dat molybdeniet mogelijk beter geschikt is voor geïntegreerde logische circuits dan grafeen Inside YouTube's jaar van verantwoordelijkheid
Inside YouTube's jaar van verantwoordelijkheid Nieuwe kwantumfenomenen in superroosters van grafeen
Nieuwe kwantumfenomenen in superroosters van grafeen Onderzoekers brengen kristallen in kaart om behandelingen voor beroerte te bevorderen, suikerziekte, Dementie
Onderzoekers brengen kristallen in kaart om behandelingen voor beroerte te bevorderen, suikerziekte, Dementie Een vijfde van de koolstof die de kustwateren van Oost-Noord-Amerika binnendringt, is begraven
Een vijfde van de koolstof die de kustwateren van Oost-Noord-Amerika binnendringt, is begraven
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

