
Wetenschap
Oplosbaarheidsmysterie van veelgebruikt plastic opgelost
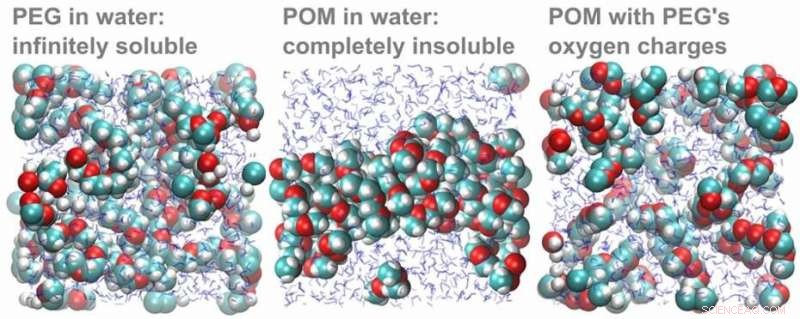
Computersimulaties van PEG- en POM-moleculen in water. Links:PEG-moleculen lossen op in water. Midden:POM-moleculen lossen niet op in water, maar blijf bij elkaar in een klontje. Rechts:Wanneer de lading van de zuurstofatomen wordt veranderd in de waarde in PEG, de POM-moleculen lossen snel op. Krediet:HIMS
Polyethermoleculen hebben de neiging om beter in water op te lossen omdat ze meer zuurstof en minder koolstofatomen bevatten. Maar er zijn zeer contra-intuïtieve uitzonderingen op deze trend, de meest bekende is de veelgebruikte plastic POM. Het heeft de hoogst mogelijke zuurstof/koolstofverhouding maar is volledig onoplosbaar. In het huidige nummer van Natuurcommunicatie , onderzoekers van de Universiteit van Amsterdam en het Max Planck Instituut voor Polymeeronderzoek in Mainz komen nu met een definitieve verklaring.
De onderzoekers werpen met name licht op de oplosbaarheidsverschillen tussen de polyethers PEG (polyethyleenglycol) en POM (polyoxymethyleen) die overal in ons dagelijks leven voorkomen. PEG heeft vele toepassingen in waterige oplossingen voor farmaceutische en cosmetische doeleinden, bijvoorbeeld in crèmes voor scheren en huidverzorging. POM is een alomtegenwoordig plastic materiaal:veel voorwerpen in het dagelijks leven zijn gemaakt van POM, evenals de felgekleurde Keck-clips voor het aansluiten van glaswerk, bekend bij elke chemicus.
Hoewel deze twee polyethers op moleculair niveau veel op elkaar lijken, ze hebben een zeer contra-intuïtieve oplosbaarheid in water. PEG (herhalende eenheid -CH 2 -CH 2 -O-) is perfect oplosbaar, en elke scheikundestudent kan je vertellen waarom:de zuurstofatomen in PEG zijn licht negatief geladen, waardoor ze hydrofiel zijn. Deze verklaring lijkt te worden bevestigd door het vergelijkbare polymeer PPG (polypropyleenglycol, herhalende eenheid-CH 2 -CH 2 -CH 2 -O-):het bevat relatief minder zuurstofatomen dan PEG, en is minder oplosbaar, wat volkomen logisch is.
Maar wacht:POM (herhalende eenheid -CH 2 -O-) bevat relatief meer zuurstofatomen dan PEG, dus de verklaring zou een verhoogde oplosbaarheid suggereren. Echter, POM is volledig onoplosbaar!
Inductie als verklarend principe
Om het mysterie te ontrafelen, gebruikten de onderzoekers uit Amsterdam en Mainz een combinatie van femtoseconde-infraroodspectroscopie, diëlektrische ontspanningsexperimenten, kwantumberekeningen en computersimulaties.
De experimenten toonden aan dat de water-polymeer interactie, die de oplosbaarheid bepaalt, hangt sterk af van de koolstof/zuurstofverhouding van het polymeer. interessant, kwantumberekeningen toonden aan dat deze afhankelijkheid niet te wijten is aan de afstand tussen de zuurstofatomen in de polymeerketen. Dit is vaak voorgesteld - het idee is dat de zuurstof-zuurstofafstand in PEG beter past in het waterstofbrugnetwerk van water.
In Nature Communications laten de onderzoekers nu zien dat de relatie tussen koolstof/zuurstofverhouding en oplosbaarheid inductie is:de zuurstofatomen zijn negatief geladen omdat ze elektronendichtheid onttrekken aan de naburige koolstofatomen in de polymeerketen. in PEG, elk zuurstofatoom heeft twee aangrenzende koolstofatomen volledig tot zijn beschikking om de elektronendichtheid aan te onttrekken. in POM, echter, de zuurstofatomen moeten de koolstofatomen onderling "delen", en kan daarom minder elektronendichtheid onttrekken. Als resultaat, de gedeeltelijke negatieve lading op de zuurstofatomen in POM is ongeveer twee keer zo laag als in PEG. Het concept van inductie zou dus perfect verklaren waarom POM veel minder hydrofiel is, en daardoor onoplosbaar.
Elegante bevestiging
Om te bevestigen dat het verschil in partiële zuurstoflading inderdaad het oplosbaarheidsverschil verklaart, de theoretische onderzoekers in het team voerden een elegant computerexperiment uit. Eerst, ze simuleerden een oplossing van POM-moleculen, die neerkwam zoals verwacht. Toen ze vervolgens de zuurstofladingen van POM veranderden in die berekend voor PEG, de POM-met-PEG-kosten losten onmiddellijk op.
Naast het oplossen van een al lang bestaand mysterie met betrekking tot alledaagse materialen, de resultaten laten zien dat inductie-effecten een grote invloed kunnen hebben op de oplosbaarheid. Rekening houden met dit effect zou het gemakkelijker moeten maken om oplosbaarheden in de toekomst te voorspellen.
 Onderzoekers bedenken kleine, hersluitbare pakketten om materialen op tijd af te leveren
Onderzoekers bedenken kleine, hersluitbare pakketten om materialen op tijd af te leveren Spaghetti, vensterbank, en LEGO:on-the-fly composieten modellering
Spaghetti, vensterbank, en LEGO:on-the-fly composieten modellering Wat is een thermoplastisch polymeer?
Wat is een thermoplastisch polymeer?  Domino-effect in farmaceutische synthese
Domino-effect in farmaceutische synthese Onderzoek naar biomimicry - het bouwen van de volgende generatie aanpasbare materialen uit de natuur
Onderzoek naar biomimicry - het bouwen van de volgende generatie aanpasbare materialen uit de natuur
 Filippijnse luchtlandingscampagne richt zich op weer, klimaatwetenschap
Filippijnse luchtlandingscampagne richt zich op weer, klimaatwetenschap Drijvende parken gemaakt van plastic afval kunnen gemeenschappen verenigen om vervuiling aan te pakken
Drijvende parken gemaakt van plastic afval kunnen gemeenschappen verenigen om vervuiling aan te pakken AI gebruiken, burgerwetenschap en rampenbestrijding om slachtoffers van orkaan Irma . te helpen
AI gebruiken, burgerwetenschap en rampenbestrijding om slachtoffers van orkaan Irma . te helpen Langzamer smelten van sneeuw in een opwarmende wereld
Langzamer smelten van sneeuw in een opwarmende wereld Watersporters en vissers moesten helpen bij het opnieuw in kaart brengen van door orkaan Irma . gewijzigde waterwegen
Watersporters en vissers moesten helpen bij het opnieuw in kaart brengen van door orkaan Irma . gewijzigde waterwegen
Hoofdlijnen
- Hoe beïnvloedt de temperatuur het metabolisme?
- Genetische studie onthult evolutionaire geschiedenis van dingo's
- Is de behoefte aan privacy evolutionair?
- VN schotelt vijgcactus voor als antwoord op voedselzekerheid
- Hoe succesvol te zijn in Microbiology
- Waarom zijn mensen hun staart kwijtgeraakt?
- Dominant Allele: wat is het? & Waarom gebeurt het? "(with Traits Chart)
- Waar vindt glucoserosorbtie plaats?
- Live 3D-beeldvorming benadrukt cellulaire activiteit tijdens embryonale hartontwikkeling
- Methanol

- Compressief scheren kan het leven op andere planeten doen ontstaan

- Onderzoekers ontwikkelen technologie voor het malen van cryogene koffie

- Supercomputers en het Archimedes-principe maken het mogelijk om de diffusie van nanobellen in nucleaire brandstoffen te berekenen

- Onderzoeksgroep heeft een defectbestendige superlegering gemaakt die 3D-geprint kan worden

 Studie verbindt grondwater met oppervlaktewater in Devils River
Studie verbindt grondwater met oppervlaktewater in Devils River Licht van zeldzame aarde:nieuwe kansen voor organische light-emitting diodes
Licht van zeldzame aarde:nieuwe kansen voor organische light-emitting diodes De beste met radiokoolstof gedateerde vindplaats in de hele recente Iberische prehistorie
De beste met radiokoolstof gedateerde vindplaats in de hele recente Iberische prehistorie Technische banen stijgen naar recordhoogten in Bay Area
Technische banen stijgen naar recordhoogten in Bay Area Een fononisch kristal gekoppeld aan een transmissielijn via een kunstmatig atoom
Een fononisch kristal gekoppeld aan een transmissielijn via een kunstmatig atoom Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen
Uitlaatgas is de schuldige:ozon op leefniveau is schadelijk voor gewassen Wetenschappers bedenken een benadering met een Trojaans paard om kankercellen te doden zonder medicijnen te gebruiken
Wetenschappers bedenken een benadering met een Trojaans paard om kankercellen te doden zonder medicijnen te gebruiken Het bevorderen van antiracisme in de ecologie, evolutie en conservatiebiologie
Het bevorderen van antiracisme in de ecologie, evolutie en conservatiebiologie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

