
Wetenschap
Gerichte evolutie opent deur naar nieuwe antibiotica
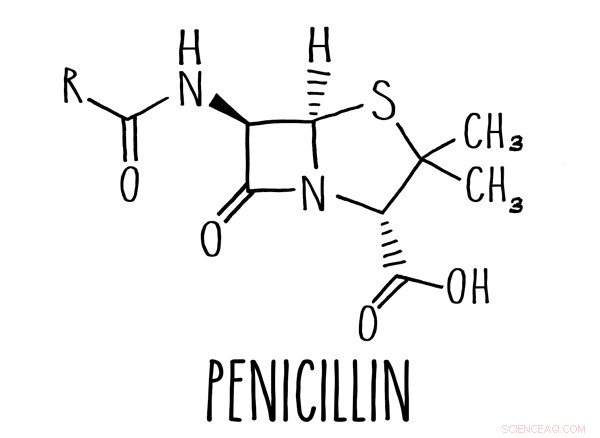
Een bètalactamring vormt de kern van veel antibiotica, inclusief penicilline. Krediet:Caltech
In de voortdurende wapenwedloop met mensen en hun antibiotica aan de ene kant, en bacteriën met hun vermogen om afweer tegen antibiotica te ontwikkelen aan de andere kant, mensen hebben een nieuwe bondgenoot ingelijfd:andere bacteriën.
Veel voorkomende antibiotica, waaronder het meest bekende antibioticum, penicilline, zijn gebaseerd op een moleculaire structuur die bekend staat als een bètalactamring. Deze medicijnen, toepasselijk genaamde bètalactamantibiotica, interfereren met het vermogen van een bacterie om zijn celwand te bouwen.
Naarmate bacteriën resistent worden tegen bestaande antibiotica, onderzoekers en farmaceutische bedrijven werken aan nieuwe. Dat betekent dat er hard gewerkt wordt aan het creëren van nieuwe soorten bètalactams, en dat is waar het lab van Frances Arnold in beeld komt.
Bèta-lactams worden gemaakt door een kettingachtig molecuul te nemen en het in een lus te plaatsen, zoiets als het ene uiteinde van een touwtje nemen en het in een knoop in het midden van het touwtje binden.
De grootste uitdaging is om precies te controleren waar langs het molecuul de reactie plaatsvindt. Met traditionele synthetische chemie, scheikundigen moeten extra stukjes op moleculen plakken die ze willen omzetten in bètalactams. Zonder die extra stukken, de knopen zullen eindigen op inconsistente plekken, wat resulteert in sommige lussen die groot zijn en sommige die klein zijn. Dat is onwenselijk voor iemand die een consistente batch antibiotica probeert te maken. Maar de toevoeging van die extra stukken maakt de synthese ingewikkelder omdat er extra stappen nodig zijn om ze toe te voegen en nog meer stappen om ze te verwijderen nadat de looping is voltooid.

Een lactamring wordt gemaakt door een molecuul op zichzelf te lussen, net als het binden van een lus in een touwtje. Krediet:Caltech
Afgestudeerde student Inha Cho en postdoctoraal onderzoeker Zhi-Jun Jia, beide uit Arnolds lab, iets eenvoudiger hebben ontwikkeld door gerichte evolutie te gebruiken, een techniek ontwikkeld door Arnold, de Linus Pauling hoogleraar chemische technologie, Bio-engineering en biochemie, en directeur van het Donna en Benjamin M. Rosen Bioengineering Center. In gerichte evolutie, die Arnold in de jaren negentig ontwikkelde en waarvoor ze in 2018 de Nobelprijs voor de Scheikunde ontving, enzymen worden in een laboratorium ontwikkeld totdat ze zich op de gewenste manier gedragen. De genetische code van een bruikbaar enzym wordt overgebracht naar bacteriën zoals Escherichia coli. Naarmate de bacteriën groeien, verdeling, en hun leven leiden, ze produceren het enzym.
In dit geval, Cho en Jia namen een enzym dat bekend staat als cytochroom P450, dat een veelzijdig werkpaard is geweest in het Arnold-lab, en evolueerde het om bètalactams te produceren. Er werden ook twee andere versies van enzymen gemaakt om andere ringgroottes van lactamen te construeren. Eén versie creëert een gamma-lactam, een lus van vier koolstofatomen en één stikstofatoom. En de andere versie creëert een delta-lactam, een lus van vijf koolstofatomen en één stikstofatoom.
"We ontwikkelen nieuwe enzymen met een activiteit die in de natuur niet te vinden is, " zegt Cho. "Lactams kunnen in veel verschillende medicijnen worden gevonden, maar vooral in antibiotica, en we hebben altijd nieuwe nodig."
Jia wijst erop dat de enzymen die ze hebben gemaakt ook ongelooflijk efficiënt zijn, waarbij elk enzymmolecuul in staat is tot een miljoen bètalactammoleculen te produceren. "Ze vertegenwoordigen de meest efficiënte enzymen die in ons laboratorium zijn gemaakt, en zijn klaar voor industriële toepassingen, "zegt Jia.
De krant, getiteld "Site-selectieve enzymatische CH-amidering voor de synthese van diverse lactamen" en co-auteur van Arnold, verschijnt in het nummer van 10 mei van Wetenschap .
Hoofdlijnen
- Nieuw onderzoek dat kankerremmende eiwitten koppelt aan celantennes
- Maken regenachtige dagen je echt down?
- Hoeveel zintuigen heeft een mens?
- Een flitsende gele keelzanger? Daar zijn genen voor
- Vliegtuigbrandstof uit suikerriet een realistisch vooruitzicht
- Beschrijving van de basisfuncties van enzymen in cellen
- Hoeveel mogelijke combinaties van eiwitten zijn mogelijk met 20 verschillende aminozuren?
- Regenboogkleuren onthullen celgeschiedenis
- Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
- Banden die binden, en kan worden losgemaakt
- Nieuwe biosyntheseroute die uniek is voor pathogene micro-organismen
- Waarom moeten een buret en pipet worden gespoeld met de juiste oplossing voor een titratie?

- Teamdetails plasmonisch effect waardoor de katalysator met lagere energie kan werken

- Berekening van het aantal mol van een verbinding

 Verdient kunstmatige intelligentie dezelfde ethische bescherming die we aan dieren geven?
Verdient kunstmatige intelligentie dezelfde ethische bescherming die we aan dieren geven? Ruimtewet is een belangrijk onderdeel van de strijd tegen ruimteschroot
Ruimtewet is een belangrijk onderdeel van de strijd tegen ruimteschroot Archeologen onthullen nieuwe vondsten van legendarisch Zweeds oorlogsschip
Archeologen onthullen nieuwe vondsten van legendarisch Zweeds oorlogsschip Waarom priemgetallen wiskundigen nog steeds fascineren, 2, 300 jaar later
Waarom priemgetallen wiskundigen nog steeds fascineren, 2, 300 jaar later Wat eet planten in de woestijn?
Wat eet planten in de woestijn?  Een gnu-manier om de kamertemperatuur te regelen
Een gnu-manier om de kamertemperatuur te regelen Fractale patronen in groeiende bacteriekolonies
Fractale patronen in groeiende bacteriekolonies Techleiders dringen aan op meer focus van het Witte Huis op AI
Techleiders dringen aan op meer focus van het Witte Huis op AI
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


