
Wetenschap
Engineered smart cells verbeteren de productie van farmaceutische grondstoffen

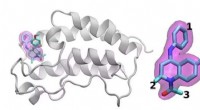
Figuur 1 - Een ontwerp, Bouwen, Toets, Leer workflow maakte verbetering van de productie van alkaloïden mogelijk. Krediet:Universiteit van Kobe
Onderzoekers in Japan hebben een geïntegreerd synthetisch biologiesysteem ontwikkeld om nieuwe metabole routes en enzymen in microben te construeren. Door een "Ontwerp, Bouwen, Toets, Leren" (DBTL)-workflow, de productie van farmaceutische grondstoffen zou systematisch kunnen worden geoptimaliseerd. Deze applicatie ondersteunt het concept van de DBTL-workflow als een duurzame methode voor de productie van complexe en waardevolle materialen. De resultaten zijn op 1 mei gepubliceerd in het open access tijdschrift Natuurcommunicatie .
Deze studie maakt deel uit van een project van de New Energy and Industrial Technology Development Organization (NEDO), en werd uitgevoerd door een onderzoeksteam van de Universiteit van Kobe onder leiding van assistent-professor Christopher Vavricka, Een bezoek aan professor Michihiro Araki, Professor Tomohisa Hasunuma en Professor Akihiko Kondo. Nauwe samenwerking met een onderzoeksteam onder leiding van universitair hoofddocent Hiromichi Minami (Research Institute for Bioresources and Biotechnology, Ishikawa Prefectural University) stond ook centraal in dit project.
Het collaboratieve onderzoeksteam neemt deel aan een NEDO onderzoeks- en ontwikkelingsproject onder het thema "Ontwikkeling van productietechnieken voor zeer functionele biomaterialen met behulp van slimme cellen van planten en andere organismen (Smart Cell Project)". Het doel van het Smart Cell Project is om massaproductie van zeer gewaardeerde doelmaterialen te bereiken door genen te introduceren die coderen voor verbeterde routes in gastheermicroben. Dit proces is sterk afhankelijk van informatie-analysetechnologie om metabolische systemen en routes opnieuw te ontwerpen die de productiehoeveelheden en de productie-efficiëntie kunnen verhogen.
De productie van alkaloïden werd gekozen als een goed voorbeeld voor optimalisatie, omdat alkaloïden belangrijke tussenproducten zijn bij de productie van geneesmiddelen, waaronder opioïde pijnstillers. Onlangs, de productie van alkaloïde afgeleide pijnmedicatie is bereikt met behulp van microben, maar om dit commercieel levensvatbaar te maken, moeten de productieopbrengsten worden verbeterd. Het belangrijkste alkaloïde tussenproduct tetrahydropapaveroline (THP) werd eerder geproduceerd met een combinatie van twee enzymen:aromatisch L-aminozuurdecarboxylase (AAAD) en monoamineoxidase (MAO). Echter, de ontspannen specificiteit MAO is een barrière geweest voor efficiënte THP-productie.
Om dit proces te verbeteren, een metabool ontwerpprogramma genaamd M-path werd op de proef gesteld. Deze voorspellingssoftware is ontwikkeld door professor Araki aan de Kobe University, en toegepast om nieuwe enzymen te identificeren die MAO kunnen omzeilen voor verbeterde routes naar het belangrijkste alkaloïde intermediaire THP. De M-path-analyse leidde tot de ontdekking van een veelbelovend natuurlijk enzym gevonden in zijderupsen genaamd 3, 4-dihydroxyfenylacetaldehyde synthase (DHPAAS) als alternatief voor MAO. DHPAAS is nieuw omdat het een amineoxiderend vermogen bezit naast de conventionele decarboxyleringsactiviteit. Het team ontwikkelde vervolgens op structuur gebaseerde enzymengineeringmethoden om de belangrijkste aminozuren te identificeren die betrokken zijn bij het bepalen van de DHPAAS-enzymactiviteit. Hierdoor konden ze kunstmatige DHPAAS-enzymen maken die de verhouding van decarboxylase- en amine-oxidase-activiteiten kunnen afstemmen, wat leidt tot een betere productie van het belangrijkste tussenproduct THP.
Toen het team de nieuw ontworpen metabolische route introduceerde, inclusief gemanipuleerde enzymen, in de conventionele laboratoriumbacterie Escherichia coli, ze waren in staat om de verhouding van de belangrijkste tussenproducten dopamine (productie van decarboxylering) en DHPAA (oxidatieproduct) nauwkeurig te regelen. Het balanceren van dopamine- en DHPAA-niveaus leidde tot een verbeterde alkaloïdeproductie in de opnieuw ontworpen "slimme cellen". Om het microbiële productiesysteem verder te optimaliseren, meer dan 100 metabolieten werden geanalyseerd met Shimadzu-massaanalysesystemen, waardoor het team knelpunten en nevenreacties kan identificeren. Door de metabolietinformatie op te nemen als leergegevens om een nieuwe DBTL-cyclus vooruit te helpen, productie van stroomafwaartse alkaloïde tussenproducten werd verder verbeterd.
Deze bevindingen tonen aan dat het combineren van geavanceerde biotechnologie en computerwetenschap een effectieve strategie is om snel celfabrieken te ontwikkelen die veel verschillende soorten waardevolle materialen kunnen produceren. In aanvulling, het vermogen om kunstmatige enzymfuncties te ontwikkelen, kan helpen om het scala aan mogelijke productiedoelen uit te breiden. Ergens naar uitkijken, de auteurs zijn van mening dat de DBTL-workflow een efficiëntere productie van verschillende nuttige materialen mogelijk zal maken, inclusief geneesmiddelen, fijne chemicaliën, biologische chemicaliën en biobrandstoffen. Deze workflow voor synthetische biologie zal naar verwachting een belangrijke bijdrage leveren aan de slimme celindustrie van de volgende generatie voor de productie van complexe geneesmiddelen en chemicaliën, evenals nieuw ontdekte materialen.
 Drugsjagers bewapenen, scheikundigen ontwerpen nieuwe reactie voor medicijnontdekking
Drugsjagers bewapenen, scheikundigen ontwerpen nieuwe reactie voor medicijnontdekking Het veelzijdige ontwerp van de bidsprinkhaangarnalenclub inspireert geavanceerde composietmaterialen voor vliegtuigen, voetbal helmen
Het veelzijdige ontwerp van de bidsprinkhaangarnalenclub inspireert geavanceerde composietmaterialen voor vliegtuigen, voetbal helmen Chemische ingenieurs ontwikkelen nieuwe klasse multifunctioneel precisiepolymeer
Chemische ingenieurs ontwikkelen nieuwe klasse multifunctioneel precisiepolymeer Nauwe ruimtes tip aanwezigheid van petrochemicaliën
Nauwe ruimtes tip aanwezigheid van petrochemicaliën Video:Hoe werkt airconditioning?
Video:Hoe werkt airconditioning?
 De voedselsystemen van steden veranderen om de CO2-uitstoot te verminderen
De voedselsystemen van steden veranderen om de CO2-uitstoot te verminderen De Indiaanse spirituele betekenissen van dieren
De Indiaanse spirituele betekenissen van dieren Een opwarmend Californië vormt het toneel voor toekomstige overstromingen
Een opwarmend Californië vormt het toneel voor toekomstige overstromingen Experts waarschuwen voor dode zone in Chesapeake Bay tegen vervuiling
Experts waarschuwen voor dode zone in Chesapeake Bay tegen vervuiling Top 5 manieren waarop NASA het milieu helpt
Top 5 manieren waarop NASA het milieu helpt
Hoofdlijnen
- Onverwachte regulatie van transcriptiefactoren die cruciaal zijn voor ontwikkeling
- Thailand neemt grote slagtanden van olifanten in beslag ter waarde van meer dan $ 450, 000
- Welke soorten moleculen katalyseren RNA-splitsing?
- VS keuren herstelplan voor Mexicaanse wolven goed
- Wat zijn de verschillen tussen een oog van een koe en een menselijk oog?
- Dahls paddenkopschildpad bedreigd door versnipperd leefgebied, krimpende bevolking
- Hoe hoge bomen suikers verplaatsen
- Nieuwe database catalogiseert planten die verontreiniging opnemen
- Van Zuidoost-Azië tot de riolen:studie bepaalt nieuwe geografische oorsprong van bruine ratten
- Onderzoeksgroep gebruikt supercomputing om zich te richten op de meest veelbelovende kandidaat-geneesmiddelen uit een enorm aantal mogelijkheden
- De wetenschap van geur bevorderen - met een vleugje musk

- Onderzoekers ontdekken unieke multifibrillaire vezels

- Peptidepapieren wijzen op nieuwe manieren om bacteriën aan te pakken

- De groei van nanodeeltjes belichten met röntgenstralen

 Edgy blik op 2-D molybdeendisulfide
Edgy blik op 2-D molybdeendisulfide Onderzoekers ontwikkelen techniek om koolstofdioxide en methaan te hergebruiken
Onderzoekers ontwikkelen techniek om koolstofdioxide en methaan te hergebruiken Studie vindt dat aardvarkens lijden als het Afrikaanse klimaat warmer wordt
Studie vindt dat aardvarkens lijden als het Afrikaanse klimaat warmer wordt Meena is een toonbeeld van verstandige gesprekken, presteert beter dan andere chatbots
Meena is een toonbeeld van verstandige gesprekken, presteert beter dan andere chatbots Bouw diverse voedselsystemen voor de post-COVID-19 wereld
Bouw diverse voedselsystemen voor de post-COVID-19 wereld Hoe de omtrek van een parallellogram te vinden
Hoe de omtrek van een parallellogram te vinden  Onderzoek wijst op mogelijke verandering in watervingerafdruk van komeet
Onderzoek wijst op mogelijke verandering in watervingerafdruk van komeet Ecologische landroof:voedsel versus brandstof versus bossen
Ecologische landroof:voedsel versus brandstof versus bossen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

