
Wetenschap
Bewerkt plantaardig toxine bezit anti-tumor eigenschappen
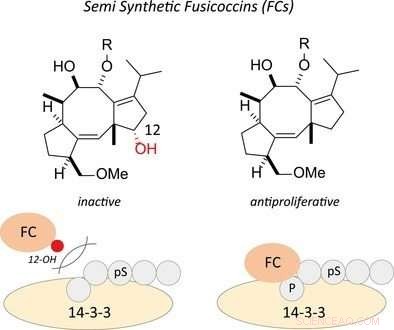
Fusicoccine, een fytotoxine, werd omgezet in een reeks antiproliferatieve middelen voor tumorcellen door de 12hydroxylgroep te verwijderen. Van deze verbindingen werd aangetoond dat ze de interactie van 1433 en een fosfoligand op een sequentiespecifieke manier opwaarts reguleren. Krediet:© 2018, John Wiley en zonen
Onderzoekers van de Shinshu University in Japan hebben ontdekt dat het bewerken van de chemische eigenschappen van fusicoccines, een soort giftige organische verbinding die door schimmels wordt geproduceerd om planten te vernietigen, kan ze omzetten in chemicaliën met anti-tumor eigenschappen in cellen. De resultaten van het onderzoek zijn gepubliceerd in Chemie — een Europees tijdschrift in september 2018.
Hoewel bekend is dat fusicoccinen betrokken zijn bij verschillende activiteiten in de zoogdiercel, hun exacte mechanismen zijn niet goed begrepen. bij planten, fusicoccins binden structureel aan een specifiek type eiwit, 14-3-3-eiwitten genoemd. Bij zoogdieren, dezelfde 14-3-3-eiwitten zijn verantwoordelijk voor het reguleren van verschillende cellulaire processen, waaronder celgroei en -dood, differentiatie en veroudering.
In deze context, de auteurs keken specifiek naar het effect van een model fusicoccine op de binding tussen 14-3-3-eiwitten en hun partnermoleculen in een proces van vorming van grotere functionele complexen. De onderzoekers hebben aangetoond dat een belangrijke chemische verandering in de structuur van een fusicoccine niet alleen het bindingsgedrag tussen een 14-3-3-eiwit en zijn partnermolecuul beïnvloedt tijdens complexvorming (ook wel eiwit-eiwitinteractie genoemd, PPI), maar deze verandering veranderde de fusicoccine ook in een giftige stof met het vermogen om cellen te vernietigen, de laatste is van bijzonder belang in kankercellen.
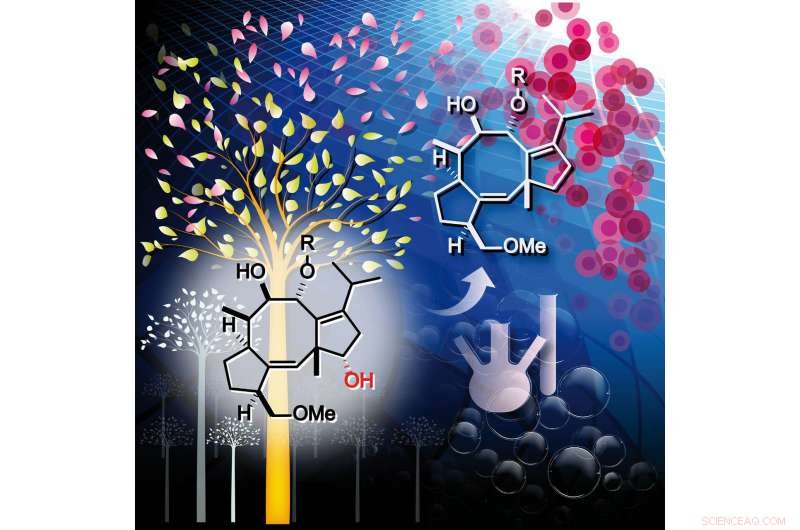
Fusicoccine, een fytotoxine, werd omgezet in een reeks antiproliferatieve middelen voor tumorcellen door de 12-hydroxylgroep te verwijderen. (staat op de omslag van) Chemie - Een Europees tijdschrift ) Krediet:© 2018, John Wiley en zonen
"Wat ons het meest intrigeert, is dat de eenvoudige structurele verandering van de fusicoccine, die anders geen toxiciteit bezit in menselijke cellen, kan leiden tot antikankermiddelen, " zegt Junko Ohkanda, doctoraat, corresponderende auteur van het onderzoekspaper en professor aan het Institute of Agriculture, Shinshu-universiteit. "Onze studie suggereert dat de verbinding werkt als een stabilisator voor eiwit-eiwit-interacties. Er zijn tot nu toe slechts enkele voorbeelden hiervan bekend."
De auteurs synthetiseerden eerst twee model fusicoccinen, een met een kritische hydroxylgroep, of een gebied dat een waterstofmolecuul bevat dat is gebonden aan een zuurstofmolecuul, en één zonder een hydroxylgroep. Dit gebeurde via een reeks chemische reacties. Om het effect van een fusicoccin op de eiwit-eiwit interacties te kunnen waarnemen, de onderzoekers gebruikten fluorescentie-etikettering. Dat stelde hen in staat om te differentiëren wanneer een eiwit aan een specifiek soort synthetisch fusicoccine bond en om de structurele effecten van eiwitten van de aan- of afwezigheid van de hydroxylgroep te begrijpen.
Hoewel verbindingen die interacties tussen eiwitten reguleren in het post-genoomtijdperk naar voren zijn gekomen als nieuwe veelbelovende doelwitten voor geneesmiddelen en de afgelopen twee decennia veel aandacht hebben gekregen, het ontwikkelen van een synthetisch molecuul met die functie blijft een uitdaging. "We hopen een nieuw klinisch relevant middel tegen kanker te kunnen ontwikkelen op basis van fusicoccines, die selectief eiwit-eiwit interacties controleren die cruciaal zijn voor celoverleving, " zegt professor Ohkanda.
Volgens Ohkanda, het onderzoeksteam is van mening dat "fusicoccinen een nieuwe moleculaire basis bieden voor de ontwikkeling van zowel antitumormiddelen als de PPI-inductoren, die zeer wenselijk zijn voor een beter begrip van cellulaire biologie." In hun toekomstig onderzoek, de auteurs willen zich concentreren op het werpen van licht op de werkingsmechanismen. Als zodanig, ze richten zich al op identificatie van de cellulaire doelen.
 Brandstoffen uit het niets:nieuwe weg naar het afvangen en opwaarderen van CO2
Brandstoffen uit het niets:nieuwe weg naar het afvangen en opwaarderen van CO2 Zout helpt eiwitten om verder te komen
Zout helpt eiwitten om verder te komen Snelle vloeistofverpakking:watersilhouetten insluiten in 3D-polymeermembranen voor lab-in-a-drop-experimenten
Snelle vloeistofverpakking:watersilhouetten insluiten in 3D-polymeermembranen voor lab-in-a-drop-experimenten Chemische eigenschappen van benzoëzuur
Chemische eigenschappen van benzoëzuur Ingebedde druppelafdruktechnologie print en verwerkt druppeltjes die op hun plaats zijn opgehangen, gecontroleerd en verwerkt
Ingebedde druppelafdruktechnologie print en verwerkt druppeltjes die op hun plaats zijn opgehangen, gecontroleerd en verwerkt
 Experts:Slecht ontwerp, gebouw veroorzaakte gevaren bij de hoogste dam
Experts:Slecht ontwerp, gebouw veroorzaakte gevaren bij de hoogste dam Wat betekent een natte lente voor het bosbrandseizoen?
Wat betekent een natte lente voor het bosbrandseizoen? Indonesische vulkaan spuwt enorme aswolk
Indonesische vulkaan spuwt enorme aswolk Olieramp in Orange County laat veel aanwijzingen achter, doodlopende wegen en mysteries, maar weinig antwoorden
Olieramp in Orange County laat veel aanwijzingen achter, doodlopende wegen en mysteries, maar weinig antwoorden Kleine aardbevingen rammelen Silicon Valley, landbouwgrond in Californië
Kleine aardbevingen rammelen Silicon Valley, landbouwgrond in Californië
Hoofdlijnen
- Een dierencel maken voor een wetenschapsproject
- Studie vindt hoe de overlevingstijd van stamcellen kan worden verlengd
- Draadtap op het dak is bedoeld om te leren waar kraaien over roddelen in de schemering
- Wat is Supplex Nylon?
- Hogere biodiversiteit door rivierverruimende maatregelen
- Wat zijn de functies van mRNA & tRNA?
- Nieuwe statistische methode voor het evalueren van reproduceerbaarheid in studies van genoomorganisatie
- Moet het houden van reptielen en amfibieën als huisdier worden beperkt?
- Stamboom van Homo Sapiens blijft evolueren
- Precious Metals Extract from Sulfides

- Volgmechanismen van kristallisatie in realtime
- Hoe houden Van der Waals-krachten moleculen bij elkaar?

- Onderzoekers ontwikkelen hoogwaardige perovskietoxide-katalysatoren met behulp van laat-overgangsmetaaloxidematerialen
- Nieuwe mogelijkheden voor lichtgevende kunststoffen met patroonlicht

 Hoe een spanningsdaling over weerstanden te berekenen
Hoe een spanningsdaling over weerstanden te berekenen  Klimaatsimulaties project natter, winderige orkanen
Klimaatsimulaties project natter, winderige orkanen Hoe AI kan leiden tot cursusontwerp en studiekeuzes om afgestudeerden te helpen de banen te krijgen die ze willen
Hoe AI kan leiden tot cursusontwerp en studiekeuzes om afgestudeerden te helpen de banen te krijgen die ze willen Onderzoekers onderzoeken enzymactiviteiten op basis van nanocomplexsensoren
Onderzoekers onderzoeken enzymactiviteiten op basis van nanocomplexsensoren Herziening van drukeffecten op op ijzer gebaseerde hogetemperatuursupergeleiders
Herziening van drukeffecten op op ijzer gebaseerde hogetemperatuursupergeleiders Wat als je in een lift zat en de kabel brak?
Wat als je in een lift zat en de kabel brak?  Waarom zenuwagent Novitsjok zo dodelijk is
Waarom zenuwagent Novitsjok zo dodelijk is  Hoe te weten wanneer een vergelijking geen oplossing heeft, of oneindig veel oplossingen
Hoe te weten wanneer een vergelijking geen oplossing heeft, of oneindig veel oplossingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

