
Wetenschap
Onderzoeksteam keert de manier waarop kaliumkanalen werken van bacterie naar mens om

Door hun onderzoek, Cuello, samen met D. Marien Cortes, bepaald hoe ongekende kennis en controle over kaliumkanalen te verkrijgen. Krediet:TTUHSC
Voor de eerste keer ooit, onderzoekers van het Texas Tech University Health Sciences Center (TTUHSC) hebben een specifiek aminozuurresidu geïdentificeerd dat verantwoordelijk is voor het omkeren van de communicatie tussen het openen van de activeringspoort en de inactivering van het selectiviteitsfilter van een kaliumkanaal. De studie werd gepubliceerd in de Proceedings van de National Academy of Sciences (PNAS) aprilnummer.
Luis G. Cuello, doctoraat, universitair hoofddocent bij de TTUHSC Afdeling Celfysiologie en Moleculaire Biofysica en directeur van het Core Facility Laboratory van het Center for Membrane Protein Research, zei dat zijn onderzoeksteam in staat was om de manier waarop kaliumkanalen van bacteriën naar mensen werken om te keren.
"Normaal gesproken, een kaliumkanaal opent de activeringspoort en beheert de ionengeleiding gedurende honderden milliseconden, dan omdat de activeringspoort en de filteroverspraak, het filter ondergaat een verandering in zijn conformatie die zijn ineenstorting opleverde, die de ionengeleiding stopt, het kanaal inactiveren, ' zei Cuello.
Kaliumkanalen zijn uiterst gespecialiseerde eiwitten die zijn ingebed in een membraan dat elke levende cel omgeeft. Door een nauwe vernauwing te sluiten en te openen die bekend staat als de activeringspoort, ze regelen het transport van kaliumionen in en uit de cel. Het selectiviteitsfilter van kaliumkanalen is het gebied binnen de eiwitstructuur dat verantwoordelijk is voor de selectieve discriminatie tussen kalium- en natriumionen, die ongeveer even groot zijn. Cuello zei dat dit deel van het eiwit een doorgang krijgt die perfect past bij kaliumionen, maar niet in staat is om natriumionen op te nemen. waardoor het "selectief" is voor kaliumionen. Het filter kan ook fungeren als een secundaire poort in serie met de activeringspoort.
"We hebben dit eerder vastgesteld door de kristalstructuur van een open kaliumkanaal op te lossen, " zei Cuello. "De opening van de activeringspoort veroorzaakt het instorten van het selectiviteitsfilter dat de stroom van ionen er doorheen verhindert, ondanks dat de activeringspoort open is. Het instorten van een kaliumkanaal is de onderliggende oorzaak van een proces dat bekend staat als C-type inactivatie, waardoor het selectiviteitsfilter de C-type inactiveringspoort is."
Kaliumkanalen zijn eiwitten die zijn gemaakt van aminozuurresten. EEN THREONINE is een van de 20 verschillende aminozuurresten die een cel gebruikt om een eiwitmolecuul te bouwen. Cuello's lab identificeerde een Threonine-residu (Threonine 75) als een cruciale speler die de opening van de activering doorgeeft aan het kanaalselectiviteitsfilter.
Allosterische koppeling verwijst naar de communicatie tussen twee regio's binnen een eiwitstructuur. Veel therapeutische geneesmiddelen binden aan een specifieke plaats binnen de eiwitstructuur (bindingsplaats) en produceren ergens anders een effect binnen het eiwit (effectorplaats). Het identificeren van het netwerk van de aminozuurresiduen die eiwitten gebruiken om twee verre locaties te koppelen, is een belangrijke stap om op atomair niveau te begrijpen hoe eiwitten alle fysiologische aspecten in het menselijk lichaam reguleren.
Cuello's onderzoek vond een manier om dit proces om te keren in een gemuteerd kanaal, de threonine-naar-alanine-mutatie in kanalen van bacteriën tot aan de mens keert het proces terug. Deze mutantkanalen hebben een selectiviteitsinactief filter wanneer de activeringspoort gesloten is en resetten naar een geleidende conformatie wanneer de activeringspoort open is.
"Met dit onderzoek we krijgen ongekende kennis en controle over dit soort kanalen, Cuello zei. "Door een beter begrip te ontwikkelen en een ongeëvenaarde controle uit te oefenen over dit soort moleculen, we effenen de weg naar het slimme ontwerp en de synthese van nieuwe en veiligere therapeutische medicijnen om ziekten te corrigeren die verband houden met de disfunctie van kaliumkanalen."
 Hoe Net Ionic vergelijkingen in de chemie te doen
Hoe Net Ionic vergelijkingen in de chemie te doen Easy Kids Science Fair Experimenten over Germs
Easy Kids Science Fair Experimenten over Germs Hoe beïnvloedt concentratie de reactiesnelheid?
Hoe beïnvloedt concentratie de reactiesnelheid?
Verhogen van de concentratie van reactanten verhoogt in het algemeen de reactiesnelheid omdat meer van de reagerende moleculen of ionen aanwezig zijn om de reactieproducten te vormen. Dit is vooral
 Apatietachtige materialen zonder interstitiële zuurstofverbindingen vertonen een hoge oxide-ionengeleiding door overbinding
Apatietachtige materialen zonder interstitiële zuurstofverbindingen vertonen een hoge oxide-ionengeleiding door overbinding Een robot en software maken het eenvoudiger om geavanceerde materialen te maken
Een robot en software maken het eenvoudiger om geavanceerde materialen te maken
Hoofdlijnen
- Activisten willen brug over snelweg bouwen om wilde dieren veilig over te steken
- Kleine opgerolde eiwitrollen die zichzelf in kooien assembleren
- Wat is het verschil tussen planten, schimmels en dieren?
- Gestratificeerd epitheelweefsel: definitie, structuur, typen
- Wat maakt een allel dominant, recessief of mede-dominant?
- Hoe werkt een automatische DNA-sequencer?
- Hoe de hormonen van de hypofyse te onthouden
- Hoe een onbekende bacterie te identificeren in de microbiologie
- Golgi-apparaat: functie, structuur (met analogie en diagram)
- Chemisch proces breekt lignine af en verandert berkenhout in bruikbare chemische producten

- Een nieuwe manier om lichtgevoelige medicijnen te leveren om het probleem van antibioticaresistentie te bestrijden

- Speekseltest voor cannabis kan ooit helpen bij het identificeren van gehandicapte bestuurders

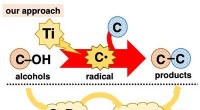
- Alcoholen als voorlopers van koolstofradicaal
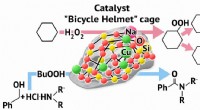
- Chemicus ontwikkelt nieuwe katalysator voor oxidatie en amidering
 NASA ziet Talim nu extra-tropisch
NASA ziet Talim nu extra-tropisch Cell on a chip onthult eiwitgedrag
Cell on a chip onthult eiwitgedrag Wetenschappers volgen elektronen in moleculen
Wetenschappers volgen elektronen in moleculen Eeuwenoude Japanse familiebedrijven maken geschiedenis relevant voor de zakenwereld van vandaag
Eeuwenoude Japanse familiebedrijven maken geschiedenis relevant voor de zakenwereld van vandaag De belangrijkste biotische en abiotische componenten van het ecosysteem van het Great Barrier Reef
De belangrijkste biotische en abiotische componenten van het ecosysteem van het Great Barrier Reef 10 Meest populaire vogels in Michigan
10 Meest populaire vogels in Michigan Je slimme huis afsluiten met blockchain
Je slimme huis afsluiten met blockchain Door het klimaat geteisterde jetstreams stimuleren droogte, overstroming:studeren
Door het klimaat geteisterde jetstreams stimuleren droogte, overstroming:studeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

