
Wetenschap
Cholesterol helpt het griepvirus te ontsnappen door het membraan van de gastheercel
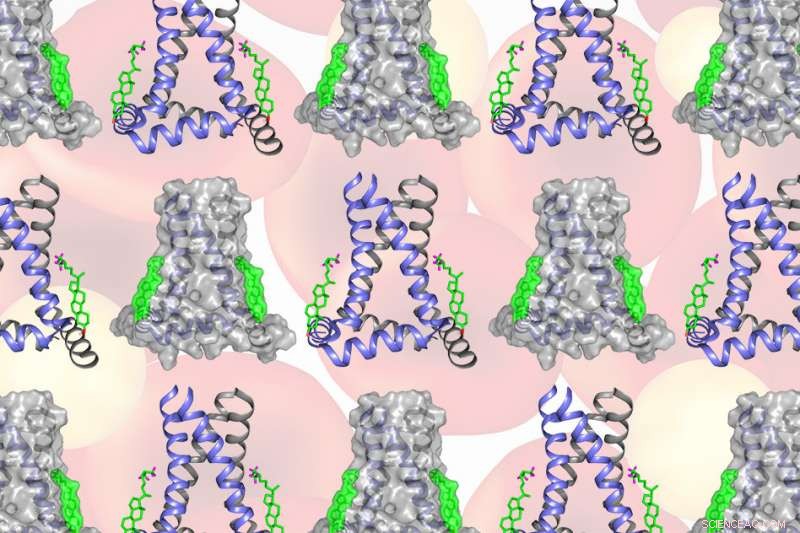
Met behulp van een techniek genaamd solid-state nucleaire magnetische resonantie (NMR) spectroscopie, een MIT-team ontdekte dat twee cholesterolmoleculen binden aan een griep-eiwit genaamd M2 om virale knoppen van hun gastheercel te scheiden. De moleculaire configuratie creëert een overdreven wigvorm in het celmembraan die de nek van het ontluikende virus buigt en vernauwt totdat de nek breekt. Krediet:Massachusetts Institute of Technology
Nadat een griepvirus een gastheercel infecteert en zijn innerlijke werking kaapt om kopieën van zichzelf te maken, deze kopieën verzamelen zich in virale knoppen die loskomen van de gastheercel om opnieuw te infecteren. Een nieuwe studie van MIT geeft nu het duidelijkste beeld tot nu toe van hoe de knoppen van het gastheercelmembraan worden afgeknepen.
Met behulp van een techniek genaamd solid-state nucleaire magnetische resonantie (NMR) spectroscopie, het MIT-team ontdekte dat twee cholesterolmoleculen binden aan een griep-eiwit genaamd M2 om de virale knoppen van hun gastheer te scheiden. De moleculaire configuratie creëert een overdreven wigvorm in het celmembraan die de nek van het ontluikende virus buigt en vernauwt totdat de nek breekt.
Terwijl eerder onderzoek had aangetoond dat de werking van M2 tijdens het ontluiken afhankelijk was van cholesterolconcentraties in het celmembraan, de nieuwe studie toont de exacte rol aan die cholesterol speelt bij het vrijgeven van het virus.
En hoewel het team zich in hun onderzoek richtte op een griepeiwit, "wij geloven dat we met deze aanpak hebben ontwikkeld, we kunnen deze techniek toepassen op veel membraaneiwitten, " zegt Mei Hong, een MIT-professor in de chemie en senior auteur van het artikel, die verschijnt in de Proceedings van de National Academy of Sciences de week van 20 november.
Het amyloïde voorlopereiwit en alfa-synucleïne, betrokken bij de ziekte van Alzheimer en de ziekte van Parkinson, respectievelijk, behoren tot de eiwitten die ten minste een deel van hun leven in celmembranen doorbrengen, die cholesterol bevatten in hun vetlagen, zegt Hong.
"Ongeveer 30 procent van de eiwitten die door het menselijk genoom worden gecodeerd, zijn geassocieerd met het celmembraan, dus je hebt het over veel directe en indirecte interacties met cholesterol, " merkt ze op. "En nu hebben we een hulpmiddel voor het bestuderen van de cholesterolbindende structuur van eiwitten."
Dynamische uitdagingen
Eerdere beeldvormings- en experimentele onderzoeken toonden aan dat het M2-eiwit van griep noodzakelijk was voor het ontluiken van virussen, en dat het ontluiken het beste werkte in celmembranen die een bepaalde concentratie cholesterol bevatten. "Maar we waren nieuwsgierig, "Hong zegt, "over de vraag of cholesterolmoleculen daadwerkelijk binden of interageren met M2. Dit is waar onze expertise met solid-state NMR van pas komt."
NMR gebruikt de magnetische eigenschappen van atoomkernen om de structuren te onthullen van de moleculen die die kernen bevatten. De techniek is bijzonder geschikt voor het bestuderen van cholesterol, "wat over het algemeen moeilijk te meten is op moleculair niveau omdat het zo klein en dynamisch is, interactie met veel eiwitten, en het celmembraan waar we het waarnemen is ook dynamisch en ongeordend, ', zegt Hong.
Dankzij de NMR-techniek konden Hong en haar collega's cholesterol vastpinnen "in zijn natuurlijke omgeving in het membraan, waar we ook het eiwit M2 in zijn natuurlijke omgeving hebben, " zegt ze. Het team was toen in staat om de afstand tussen cholesterolatomen en de atomen in het M2-eiwit te meten om te bepalen hoe cholesterolmoleculen binden aan M2, evenals de oriëntatie van cholesterol in de lagen van het celmembraan.
Cholesterol en membraankromming
Cholesterol is niet gelijkmatig over het celmembraan verdeeld - er zijn met cholesterol verrijkte "vlotten" samen met minder verrijkte gebieden. Het M2-eiwit heeft de neiging zichzelf te lokaliseren op de grens tussen de vlot- en niet-raftgebieden in het membraan, waar het ontluikende virus zichzelf kan verrijken met cholesterol om zijn virale envelop te bouwen.
De configuratie die Hong en haar collega's observeerden bij de ontluikende nek - twee cholesterolmoleculen gehecht aan M2 - creëert een significante wigvorm in de binnenste laag van het celmembraan. De wig produceert een zadelvormige kromming bij de ontluikende nek die nodig is om het membraan te verbreken en het virus vrij te geven.
De nieuwe bevindingen hebben geen directe implicaties voor het vaccineren of behandelen van griep, hoewel ze nieuw onderzoek zouden kunnen inspireren naar het voorkomen van virale ontluiking, zegt Hong.
 Moleculaire schatkaarten om nieuwe materialen te ontdekken
Moleculaire schatkaarten om nieuwe materialen te ontdekken Onderzoekers ontwerpen polymeer dat resistente bacteriën kan doden
Onderzoekers ontwerpen polymeer dat resistente bacteriën kan doden Niet-ontvlambare elektrolyt voor hoogwaardige kaliumbatterijen
Niet-ontvlambare elektrolyt voor hoogwaardige kaliumbatterijen Doorbraak in het bestuderen van het enzym dat uiteindelijk het visgeursyndroom veroorzaakt
Doorbraak in het bestuderen van het enzym dat uiteindelijk het visgeursyndroom veroorzaakt Waarom zit er een klein gaatje in een waterpomp?
Waarom zit er een klein gaatje in een waterpomp?
 Technische oplossingen ontdekken voor een koolstofarme toekomst:afvang en opslag van koolstof
Technische oplossingen ontdekken voor een koolstofarme toekomst:afvang en opslag van koolstof Limonade maken:toevalsobservatie leidt tot onderzoek naar microbiële bloeivorming
Limonade maken:toevalsobservatie leidt tot onderzoek naar microbiële bloeivorming Biodiversiteit van zoete aardappelen kan helpen om de klimaatbestendigheid van kleinschalige landbouw te vergroten
Biodiversiteit van zoete aardappelen kan helpen om de klimaatbestendigheid van kleinschalige landbouw te vergroten Deugdzame cyclus:CO2 in Gabons-bossen een prijskaartje geven
Deugdzame cyclus:CO2 in Gabons-bossen een prijskaartje geven Voor iedereen hetzelfde zeeniveau
Voor iedereen hetzelfde zeeniveau
Hoofdlijnen
- Wat doet ADP in de biologie?
- Wat zijn de functies van een levercel?
- Ontdekking van de Mitochondria
- Goed excuus,
- Nieuwe technologie verlicht microben die niet in een laboratorium kunnen worden gekweekt
- Het is goed om zeldzaam te zijn, voor sommige soorten
- Met extra suiker, bladeren worden ook dik
- nieuwe ontdekking, meer bijen markeren Michigans eerst, volledige bijentelling
- "DNA Model Project Ideas
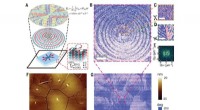
- Concentrische cirkelvormige polarisatiebanden gevonden in een ferro-elektrisch polymeer
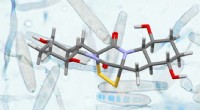
- Een nieuwe strategie voor de synthese van complexe natuurlijke producten
- De zuurtest doorstaan:nieuw systeem met lage pH recyclet meer koolstof in waardevolle producten

- De effecten van het wassen van de organische laag met natriumcarbonaat

- Bacteriële enzymen:de biologische rol van europium

 SPFCNN-Miner:een nieuwe classifier om klasse-ongebalanceerde gegevens aan te pakken
SPFCNN-Miner:een nieuwe classifier om klasse-ongebalanceerde gegevens aan te pakken Gunstige percepties van ruimte projecteren
Gunstige percepties van ruimte projecteren VS duurt langer om Sprint-fusie met T-Mobile te overwegen
VS duurt langer om Sprint-fusie met T-Mobile te overwegen IonQ kondigt ontwikkeling van volgende generatie kwantumcomputer aan
IonQ kondigt ontwikkeling van volgende generatie kwantumcomputer aan Koolstofopname door Amazonebossen komt overeen met uitstoot van regio's
Koolstofopname door Amazonebossen komt overeen met uitstoot van regio's Massale zeehondendoden in het Russische Baikalmeer
Massale zeehondendoden in het Russische Baikalmeer NASA's InSight-missie detecteert zijn eerste Marsbeving
NASA's InSight-missie detecteert zijn eerste Marsbeving  Student archeologie vindt uitzonderlijk zeldzaam fragment uit Romeinse fles
Student archeologie vindt uitzonderlijk zeldzaam fragment uit Romeinse fles
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

