
Wetenschap
Kleine veranderingen in de structuur van oppervlakteactieve stoffen beïnvloeden het vermogen om olieachtige moleculen in te kapselen

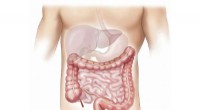
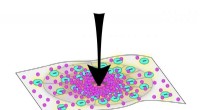
Een oppervlakteactieve stof (in rood weergegeven, geel en turkoois) met een 14-koolstof ‘staart’ vormt een golvende laag tussen water (kleurloos) en decaan (groen), die zich ontwikkelt tot knoppen (midden) en vervolgens vrije micellen (lager). Krediet:American Chemical Society
De eigenschappen van oppervlakteactieve stoffen, stoffen die de oppervlaktespanning van een vloeistof verlagen, kunnen worden verfijnd door hun moleculaire structuur aan te passen, volgens een recente A*STAR-studie. Deze methode kan onderzoekers helpen betere oppervlakteactieve stoffen te ontwikkelen voor een verscheidenheid aan toepassingen, van hulp bij het afleveren van medicijnen, of het verbeteren van de efficiëntie van olieboringen, om het reinigend vermogen van zeep te vergroten.
Oppervlakteactieve stoffen zijn moleculen met gespleten persoonlijkheden. Ze hebben meestal een hydrofiele 'kop' die water aantrekt, en een hydrofobe 'staart' die de voorkeur geeft aan olieachtige moleculen. Oppervlakteactieve stoffen kunnen kleine olieachtige druppeltjes omringen om een structuur te vormen die een micel wordt genoemd, waardoor de olieachtige moleculen kunnen worden gedispergeerd en stabiel in water.
Freda Lim en collega's van het A*STAR Institute of High Performance Computing hebben nu aangetoond dat het herschikken van de atomen in een gewone oppervlakteactieve stof een grote invloed kan hebben op het vermogen om micellen te vormen.
Het team voerde computersimulaties uit van een familie van zes verschillende alkylbenzeensulfonaatmoleculen, oppervlakteactieve stoffen die, vanwege hun kosteneffectiviteit en biologische afbreekbaarheid, worden veel gebruikt in de wasmiddelen en de aardolie-industrie. Deze moleculen bevatten alkyl-staarten met 12, 14 of 16 koolstofatomen, en sommige hebben korte alkylgroepen op verschillende posities op hun benzeensulfonaat-'koppen'.
De onderzoekers simuleerden eerst hoe de oppervlakteactieve stoffen zich gedroegen in een laag met één molecuul, gevangen tussen water en een kleurloos, olieachtige koolwaterstof genaamd decaan. Naarmate de concentratie van oppervlakteactieve moleculen toenam tot het punt waarop de laag vol was met oppervlakteactieve stoffen, die met compactere koppen en langere staarten bleven in een vlakke laag, terwijl degenen met grotere koppen en kortere staarten in golvende golven begonnen te knikken. In het algemeen, het gedrag van de oppervlakteactieve stof was ook afhankelijk van de positie van chemische groepen rond zijn kop.
De onderzoekers gingen vervolgens door met het verhogen van de concentraties oppervlakteactieve stoffen in de tussenlaag. Degenen met compactere koppen en langere staarten vormden knopachtige structuren gevuld met decaan, maar gaf geen vrije micellen vrij. In tegenstelling tot, die met de grotere koppen en kortere staarten vormden knoppen die uiteindelijk loskwamen van de oppervlakteactieve laag (zie afbeelding).
"De selectie van oppervlakteactieve stoffen hangt af van het doel waarvoor het wordt gebruikt, er is dus echt geen 'beste' oppervlakteactieve stof, " legt Lim uit. "Onze simulaties bieden een richtlijn voor het kiezen van de soorten oppervlakteactieve stoffen, afhankelijk van de specifieke toepassingen." Het team is nu van plan te onderzoeken hoe verschillende stimuli de breuk van de oppervlakteactieve micelstructuren veroorzaken, en hoe de stoffen die in deze structuren zijn gevangen, kunnen worden vrijgegeven voor toepassingen.
Hoofdlijnen
- Het belang van DNA in de menselijke cel
- Fun Biology Presentatie Onderwerpen
- Met extra suiker, bladeren worden ook dik
- Genetische veranderingen helpen muggen om aanvallen van pesticiden te overleven
- Beeldstabilisatie bij gewervelde dieren hangt af van contrast tussen objecten
- Virtuele kusten verbeteren het begrip van mogelijke uitkomsten van kustplanning
- Bestorming van het kasteel:nieuwe ontdekking in de strijd tegen bacteriën
- Ondanks de wet stijgt het aantal doden door loodvergiftiging in New Hampshire
- Philadelphia Zoo euthanaseert populaire Aziatische zwarte beer
- Grote moleculen uit voedingsvezels kunnen de darmomgeving veranderen door fysieke krachten
- Reparatie van kuilen milieuvriendelijk gemaakt met gruis van afvalwaterzuivering

- Bimetaalkatalysator helpt bij het synthetiseren van afstembare imines en secundaire aminen

- Op ijzer gebaseerde katalysatoren ontdekt in door licht aangedreven kooldioxidehydrogenering

- Onder druk:nieuw bio-geïnspireerd materiaal kan van vorm veranderen naar externe krachten
 Dichtbij omslagpunt, Amazon kan over 50 jaar instorten
Dichtbij omslagpunt, Amazon kan over 50 jaar instorten Jeetje! Enorme prehistorische krokodil duikt op uit Zuidoost-Queensland
Jeetje! Enorme prehistorische krokodil duikt op uit Zuidoost-Queensland Checkpointblokkade door een D-peptide voor kankerimmunotherapie
Checkpointblokkade door een D-peptide voor kankerimmunotherapie Groene erwten geven aanwijzingen voor de begindagen van het heelal
Groene erwten geven aanwijzingen voor de begindagen van het heelal Franse startup Plume probeert luchtkwaliteit te crowdsourcen
Franse startup Plume probeert luchtkwaliteit te crowdsourcen Verkeer bleek een belangrijke bron van atmosferische nanocluster-aerosolen
Verkeer bleek een belangrijke bron van atmosferische nanocluster-aerosolen Wiskunde gaat over verwondering, creativiteit en plezier, dus laten we het zo leren
Wiskunde gaat over verwondering, creativiteit en plezier, dus laten we het zo leren De Etna houdt zijn spectaculaire explosies vol; asregens op steden
De Etna houdt zijn spectaculaire explosies vol; asregens op steden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


