
Wetenschap
Onderzoekers ontdekken nieuwe klasse van chemische reacties
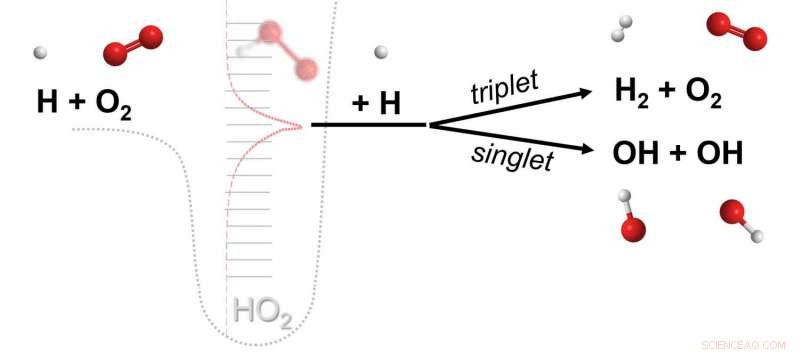
Een chemische reactie waarbij drie verschillende moleculen (bijv. H, O2, H) nemen elk deel aan het verbreken en vormen van chemische bindingen. De reactie wordt gemedieerd door een kortstondig botsingscomplex (HO2**) gevormd door de botsing van twee moleculen (H, O2) die vervolgens reageert bij een botsing met een derde molecuul (H). Gegevens van geavanceerde berekeningen laten zien dat reacties van deze klasse, bijna een eeuw geleden verondersteld en later als onbelangrijk beschouwd, zijn belangrijke chemische routes. Krediet:Michael P. Burke/Columbia Engineering
Een nieuwe studie onder leiding van Michael P. Burke, universitair docent werktuigbouwkunde aan Columbia Engineering, heeft de betekenis geïdentificeerd van een nieuwe klasse van chemische reacties waarbij drie moleculen betrokken zijn die elk deelnemen aan het verbreken en vormen van chemische bindingen. De reactie van drie verschillende moleculen wordt mogelijk gemaakt door een "kortstondig botsingscomplex, " gevormd door de botsing van twee moleculen, die lang genoeg leeft om te botsen met een derde molecuul.
Deze vierde klasse, die de onderzoekers "chemisch termoleculaire reacties, " werd voor het eerst verondersteld door Cyril Hinshelwood en Nikolay Semenov in hun studies van kettingreacties in de jaren 1920 en '30 (ze wonnen de Nobelprijs voor scheikunde van 1956 voor dit werk). Decennia lang, onderzoekers hebben deze reacties als onbelangrijk beschouwd - als ze al voorkwamen - en tot nu toe, niemand heeft ze bestudeerd. Burke, die een verscheidenheid aan problemen onderzoekt op het raakvlak tussen fundamentele fysische chemie en praktische technische apparaten, besloten om deze reacties te onderzoeken nadat ze zich realiseerden dat veelvoorkomende verbrandingssituaties, zoals die in veel motoren voorkomen, hebben voldoende hoge fracties van zeer reactieve moleculen die bekend staan als vrije radicalen om deze reacties mogelijk te maken. De nieuwe studie is vandaag gepubliceerd in Natuurchemie .
"Verbranding is altijd een startpunt geweest voor het begrijpen van allerlei andere chemische mechanismen, " zegt Burke, die ook lid is van het Data Science Institute. "Potentieel kunnen er ontelbare reacties zijn van deze nieuwe klasse die van invloed zijn op hoe we de gasfasechemie modelleren, van het ontwerpen van nieuwe soorten motoren tot het begrijpen van de planetaire chemie die verantwoordelijk is voor wolkenformaties, klimaatverandering, evolutie van verontreinigende stoffen, misschien zelfs de opeenvolging van reacties die van invloed kunnen zijn op de omstandigheden voor buitenaards leven. Onze ontdekking opent een hele nieuwe wereld van mogelijkheden."
Bijvoorbeeld, ruimtevoertuigen ervaren zeer hoge temperaturen en radicale fracties in hun afdaling terug naar de aarde. Burke speculeert dat deze vierde klasse van reacties de warmtestroom naar het voertuig kan beïnvloeden, met aanzienlijke gevolgen voor het ontwerp van thermische beveiligingssystemen om astronauten en/of ladingen veilig te houden wanneer ze naar de aarde komen.
Werken met Stephen J. Klippenstein, (Divisie Chemische Wetenschappen en Engineering, Argonne Nationaal Laboratorium), Burke gebruikte state-of-the-art computationele methoden, het combineren van kwantumchemische berekeningen die het verbreken en vormen van chemische bindingen tussen reagerende moleculen simuleren met kinetische transportberekeningen die de reacties en bewegingen van bulkgassen simuleren die de prestaties van technische apparaten bepalen.
"De kracht van deze state-of-the-art computationele methoden, " zegt Burke, "is dat ze een unieke lens kunnen bieden in ruwe chemische omgevingen die niet geschikt zijn voor experimentele technieken voor het bestuderen van individuele reactiedynamiek. Onze berekeningen zijn gebaseerd op computationele gegevens die zijn geproduceerd op basis van eerste principes:de Schrödinger-vergelijking, de fundamentele vergelijking van de kwantummechanica. Door deze gegevens te combineren met andere op fysica gebaseerde modellen, kunnen we de impact van slechts één enkele reactie uit vele, op een manier die in het lab heel moeilijk is."
Met behulp van theoretische methoden, inclusief degene die ze voor dit onderzoek hebben ontwikkeld, de onderzoekers toonden aan dat deze chemisch termoleculaire (d.w.z. drie-molecule) reacties niet alleen belangrijke chemische routes zijn, maar ook invloed hebben op de voortplantingssnelheid van vlammen, een maat voor de algehele brandstofreactiviteit die de prestaties bepaalt, stabiliteit, en efficiëntie van veel moderne motoren.
De chemie van veel systemen, inclusief verbranding en planetaire atmosferen, wordt beheerst door complexe chemische mechanismen, waarbij de algehele omzetting van een reeks initiële reactanten naar een reeks eindproducten door vele chemische intermediaire moleculen gaat, waarbij veel individuele chemische reacties op moleculair niveau plaatsvinden. Ons huidige begrip van de complexe mechanismen van verbranding en planetaire atmosferen is gebaseerd op de soorten reacties waarvan bekend is dat ze plaatsvinden. Tot nu toe, slechts drie klassen van reacties zijn overwogen:
- Unimoleculaire reacties, waarbij één reactant bindingsverbreking en/of vorming ondergaat om verschillende producten op te leveren
- Bimoleculaire reacties, waar twee reactanten botsen en vervolgens bindingen verbreken en/of vormen om verschillende producten op te leveren
- Termoleculaire associatiereacties, waar twee reactanten botsen om een moleculair complex te vormen met een nieuwe chemische binding tussen de twee reactanten en een derde molecuul, bekend als het badgas, verwijdert een deel van de interne kinetische energie van dat molecuul om het te stabiliseren
Het badgas wordt meestal beschouwd als een inert, of niet-reactief, molecuul dat niet deelneemt aan het verbreken of vormen van bindingen, maar neemt in plaats daarvan wat energie weg van het andere moleculaire complex (dat voldoende interne kinetische energie zou hebben om spontaan te ontbinden als er geen energie zou worden weggenomen).
Als in plaats daarvan het moleculaire complex botst met een reactief molecuul, dan kan het derde molecuul deelnemen aan het proces van het verbreken/vormen van bindingen, wat Burke en Klippenstein een "chemisch termoleculair reactieproduct" noemen. "In onze krant we toonden het belang aan van reacties met H + O2-complexen met andere radicale soorten, bijv. H + O2 + H, in verbrandingsomgevingen, " merkt hij op. "Echter, gezien het feit dat reactieve moleculen, zoals vrije radicalen en moleculaire zuurstof, zijn belangrijke bestanddelen bij verbranding en bepaalde planetaire omgevingen, er is een aanzienlijk potentieel voor het optreden van andere chemisch termoleculaire reacties en om een significante rol te spelen in andere omgevingen."
William H. Groen, hoogleraar chemische technologie aan het MIT, zegt over de studie, "Het is al lang bekend dat veel gasfase-associatiereacties zeer lage effectieve snelheden hebben, omdat het aanvankelijk geactiveerde adduct niet lang genoeg leeft om te worden gestabiliseerd door energieoverdracht door botsingen, en valt gewoon uit elkaar terug naar de reactanten. Dit heeft het veld ertoe gebracht te denken dat deze tijdelijke adducten volledig kunnen worden genegeerd. Dit artikel onthult dat zelfs als de unimoleculaire reacties van geactiveerde adducten verwaarloosbaar zijn, ze kunnen nog steeds deelnemen aan bimoleculaire reacties, met verrassend belangrijke gevolgen."
Burke is van plan deze theorieën en methoden voor het berekenen van chemisch termoleculaire reactiesnelheden te veralgemenen om vergelijkbare berekeningen in omgevingen met hogere druk mogelijk te maken, waar botsingen tussen moleculen nog frequenter zijn, belangrijk voor geavanceerde motorontwerpen. Hij zal ook de implicaties van de bevinding voor andere reacties en chemische omgevingen onderzoeken, zoals die welke betrokken zijn bij de vorming en reductie van verontreinigende stoffen of de chemie van planetaire atmosferen.
 Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer
Een eenstaps multikatalytische methode om racemische mengsels te verrijken tot een enkele enantiomeer Chemicus ontwikkelt apparaat om hondeneenheden te trainen in geurdetectie
Chemicus ontwikkelt apparaat om hondeneenheden te trainen in geurdetectie Wat is balpeninkt gemaakt van?
Wat is balpeninkt gemaakt van?  Nieuwe methode meet enkele moleculen uit nanoliter bloed in realtime
Nieuwe methode meet enkele moleculen uit nanoliter bloed in realtime Kristallisatie bij lage temperatuur van fasezuiver α-formamidiniumloodjodide mogelijk gemaakt door studie
Kristallisatie bij lage temperatuur van fasezuiver α-formamidiniumloodjodide mogelijk gemaakt door studie
 Onderzoek suggereert dat zware regenval van tropische cyclonen de grond eronder vervormt
Onderzoek suggereert dat zware regenval van tropische cyclonen de grond eronder vervormt Een diepe duik in de verdeling van organische koolstof in hadal-geulen
Een diepe duik in de verdeling van organische koolstof in hadal-geulen Hoe maak je een Minnow Farm
Hoe maak je een Minnow Farm Het leven op aarde is een groot deel van de geschiedenis in duisternis gehouden, studie vondsten
Het leven op aarde is een groot deel van de geschiedenis in duisternis gehouden, studie vondsten Bevroren in de tijd:gletsjerarcheologie op het dak van Noorwegen
Bevroren in de tijd:gletsjerarcheologie op het dak van Noorwegen
Hoofdlijnen
- Wat is de belangrijkste primaire producent in het mariene ecosysteem?
- Wat is het verschil in de cellen van een menselijke baby en een volwassen mens?
Nieuwe baby's zijn allebei erg op elkaar en lijken erg op volwassenen. De meeste celontwikkeling en -differentiatie vinden plaats voorafgaand aan de geboorte van een ba
- Aard-lucht warmtewisselaar beste manier om landbouwhuisdieren in stallen te beschermen tegen de gevolgen van klimaatverandering
- Moeders geven de voorkeur aan dochters,
- Zal er ooit een gelukkige pil zijn?
- Wanneer dupliceren chromosomen tijdens een cellevenscyclus?
- Mexico vangt zeldzame vaquita-bruinvis om soorten te redden
- Retrovirus versus DNA-virus
- Wat is het verschil tussen Ribosoom en Ribosomaal DNA?
- Hoe moleculaire riboswitches werken in bacteriën
- Chemische ingenieurs publiceren paper waarin theorieën over glasovergang worden uitgedaagd

- Waarom een knapperige korst essentieel is voor het aroma en de smaak van baguettes
- Model leert hoe individuele aminozuren de eiwitfunctie bepalen
- Biostasis heeft tot doel de dood na traumatisch letsel te voorkomen door biochemische reacties in cellen te vertragen

 Nieuw op genen gebaseerd model suggereert, voor microben, het is niet wie je bent, maar wat je doet
Nieuw op genen gebaseerd model suggereert, voor microben, het is niet wie je bent, maar wat je doet Wetenschappers hebben olie gevonden van de Deepwater Horizon-uitbarsting in vissenlevers en op de diepe oceaanbodem
Wetenschappers hebben olie gevonden van de Deepwater Horizon-uitbarsting in vissenlevers en op de diepe oceaanbodem Juli 2019 warmste maand ooit voor planeet:NOAA
Juli 2019 warmste maand ooit voor planeet:NOAA Hole metalen! Nieuwe metalens focust licht met ultradiepe gaten
Hole metalen! Nieuwe metalens focust licht met ultradiepe gaten Nieuwe katalytische benadering voor toegang tot belangrijke intermediaire carbokation
Nieuwe katalytische benadering voor toegang tot belangrijke intermediaire carbokation Vergelijkingen van rechthoekig naar polair formulier
Vergelijkingen van rechthoekig naar polair formulier NASA ziet tyfoon Bavi op een miljoen mijl afstand
NASA ziet tyfoon Bavi op een miljoen mijl afstand Steam converteren naar BTU
Steam converteren naar BTU
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian | Spanish |

-
Wetenschap © https://nl.scienceaq.com

