
Wetenschap
Argon is niet het middel voor metallische waterstof
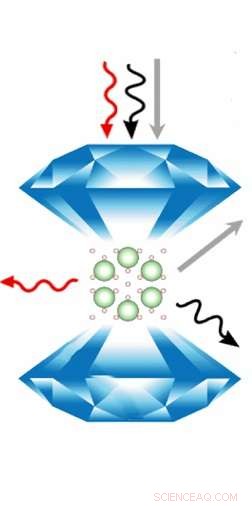
Een illustratie van Ar(H2)2 in de diamanten aambeeldcel. De pijlen vertegenwoordigen verschillende manieren waarop spectroscopische instrumenten het effect van extreme drukken op de kristalstructuur en moleculaire structuur van de verbinding bestuderen. (Voor kenners, de rode pijl staat voor Raman-spectroscopie, de zwarte pijl staat voor synchrotron röntgendiffractie, en de grijze pijl staat voor optische absorptiespectroscopie.) Credit:Cheng Ji.
Waterstof is zowel het eenvoudigste als het meest overvloedige element in het universum, dus het bestuderen ervan kan wetenschappers leren over de essentie van materie. En toch zijn er nog veel waterstofgeheimen om te ontsluiten, inclusief hoe het het beste in een supergeleidende, metalen toestand zonder elektrische weerstand.
"Hoewel theoretisch ideaal voor energieoverdracht of -opslag, metallische waterstof is uiterst uitdagend om experimenteel te produceren, " zei Ho-kwang "Dave" Mao, die een team van natuurkundigen leidde bij het onderzoeken van het effect van het edelgas argon op waterstof onder druk.
Er is lang gesuggereerd dat het introduceren van onzuiverheden in een monster van moleculaire waterstof, H2, zou kunnen helpen de overgang naar een metaalachtige toestand te vergemakkelijken. Dus Mao en zijn team gingen op zoek naar de intermoleculaire interacties van waterstof die zwak gebonden is, of "gedoopt, "met argon, Ar(H2)2, onder extreme druk. Het idee is dat de onzuiverheid de aard van de bindingen tussen de waterstofmoleculen zou kunnen veranderen, het verminderen van de druk die nodig is om de niet-metaal-naar-metaal overgang te induceren. Eerder onderzoek had uitgewezen dat Ar(H2)2 een goede kandidaat zou kunnen zijn.
Verrassend genoeg, ze ontdekten dat de toevoeging van argon de moleculaire veranderingen die nodig zijn om een metallische toestand in waterstof te initiëren niet vergemakkelijkte. Hun bevindingen worden gepubliceerd door de Proceedings van de National Academy of Sciences .
Het team bracht de met argon gedoteerde waterstof tot 3,5 miljoen keer de normale atmosferische druk - of 358 gigapascal - in een diamanten aambeeldcel en observeerde de structurele veranderingen met behulp van geavanceerde spectroscopische hulpmiddelen.
Wat ze ontdekten was dat waterstof in zijn moleculaire vorm bleef, zelfs tot de hoogste druk, wat aangeeft dat argon niet de facilitator is die velen hadden gehoopt dat het zou zijn.
"In tegenstelling tot voorspellingen, de toevoeging van argon zorgde niet voor een soort 'chemische druk' op de waterstof, waardoor de moleculen dichter bij elkaar worden geduwd. Liever, het had het tegenovergestelde effect, ", zei hoofdauteur Cheng Ji.
 Nieuwe katalysator voldoet aan de uitdaging om uitlaatgassen van moderne motoren te reinigen
Nieuwe katalysator voldoet aan de uitdaging om uitlaatgassen van moderne motoren te reinigen Video:De chemie achter van kleur veranderende vogels
Video:De chemie achter van kleur veranderende vogels Poreuze enkelkristallijne monolieten op centimeterschaal met Lewis-zuurplaatsen met hoge dichtheid om propaandehydrogena te verbeteren
Poreuze enkelkristallijne monolieten op centimeterschaal met Lewis-zuurplaatsen met hoge dichtheid om propaandehydrogena te verbeteren Ontwerpen van synthetische materialen op natuurlijke basis
Ontwerpen van synthetische materialen op natuurlijke basis Langdurige pijnverlichting met MOF's
Langdurige pijnverlichting met MOF's
 Hoge golven spoelen de stranden van Chicago weg terwijl Lake Michigan weer opengaat
Hoge golven spoelen de stranden van Chicago weg terwijl Lake Michigan weer opengaat Wat kunnen we leren door fossielen te bestuderen?
Wat kunnen we leren door fossielen te bestuderen?  Onderzoekers volgen stofvervuiling, gezondheid om gevaren in West-Afrika te herkennen
Onderzoekers volgen stofvervuiling, gezondheid om gevaren in West-Afrika te herkennen NASA kijkt naar compacte tropische storm Don in infrarood licht
NASA kijkt naar compacte tropische storm Don in infrarood licht Paleoklimatoloog weegt in op hete droogte als hoofdauteur van IPCC-klimaatrapport
Paleoklimatoloog weegt in op hete droogte als hoofdauteur van IPCC-klimaatrapport
Hoofdlijnen
- Voordelen en nadelen van Western Blot
- Wat zijn de vier stikstofhoudende bases van DNA?
- Chimpansees in het wild wijzigen waarschuwingen op basis van wat anderen in hun groep al weten, studie vondsten
- Luiheid heeft deze menselijke voorouder misschien verdoemd
- 6 veelvoorkomende hallucinaties en wat ze ons vertellen
- Squash-variëteit waarvan ooit werd gedacht dat ze uitgestorven was, gedijt goed op biologische boerderij
- Menselijke evolutie: tijdlijn, stadia, theorieën en bewijsmateriaal
- Berekening van de tijd voor celverdubbeling
- Wat is het Human Epigenome Project?
- Zichtbaar licht gebruiken om koolstofdioxide efficiënt af te breken
- Leven bevroren in de tijd onder een elektronenmicroscoop krijgt Nobelprijs
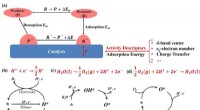
- Activiteitsbeschrijvingen voor elektrokatalysatoren in toepassingen voor energieopslag
- Betaalbare loodsensor voor thuis, stadswaterleidingen

- Mac en kaas naar Mars brengen

 Hoe microben de gezondheid van koraalriffen weerspiegelen
Hoe microben de gezondheid van koraalriffen weerspiegelen Zou er leven kunnen zijn in de oceaan van Plutos?
Zou er leven kunnen zijn in de oceaan van Plutos? Hoe beginconcentraties te berekenen
Hoe beginconcentraties te berekenen Afbeelding:hotspot Sicilië
Afbeelding:hotspot Sicilië Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien
Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien Schoolverzuim steeg tijdens pandemie, voornamelijk in meer achtergestelde gebieden
Schoolverzuim steeg tijdens pandemie, voornamelijk in meer achtergestelde gebieden Kokosolieverbindingen stoten insecten beter af dan DEET
Kokosolieverbindingen stoten insecten beter af dan DEET Waarom stoppen bij plastic zakken en rietjes? Pleidooi voor een wereldwijd verdrag dat de meeste kunststoffen voor eenmalig gebruik verbiedt
Waarom stoppen bij plastic zakken en rietjes? Pleidooi voor een wereldwijd verdrag dat de meeste kunststoffen voor eenmalig gebruik verbiedt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Portuguese | Swedish | German | Dutch | Danish | Norway | Spanish |

-
Wetenschap © https://nl.scienceaq.com

