
Wetenschap
COVID-19-virus verstoort de eiwitproductie:onderzoeker bespreekt haar recente bevindingen
Ondanks de enorme vooruitgang in ons begrip van COVID-19 in de afgelopen vier jaar, is de ziekte nog steeds volop onder ons – en er valt nog veel te leren.
Eén ding weten we wel:na een infectie is het van cruciaal belang dat onze cellen nieuwe eiwitten aanmaken ter verdediging tegen het virus.
Maar Talya Yerlici, een postdoctoraal onderzoeker aan de Temerty Faculteit der Geneeskunde van de Universiteit van Toronto, liet onlangs zien hoe SARS-CoV-2 de aanmaak van eiwitten verstoort.
Zij is de eerste auteur van een artikel waarin het proces wordt beschreven en dat onlangs is gepubliceerd in het tijdschrift Cell Reports .
Schrijver Jenni Bozec sprak onlangs met Yerlici – die is gevestigd in het laboratorium van professor Karim Mekhail op de afdeling laboratoriumgeneeskunde en pathobiologie – over de bevindingen.
Wat heb je ontdekt over hoe COVID-19 eiwitten gebruikt?
Eén manier waarop SARS-CoV-2 ons ziek maakt, is door een strategie te gebruiken die ‘host shutoff’ wordt genoemd. Dit betekent dat het virus weliswaar kopieën van zichzelf maakt, maar ook de productie van vitale componenten in onze cellen vertraagt. Als gevolg hiervan duurt het langer voordat ons lichaam op de infectie reageert.
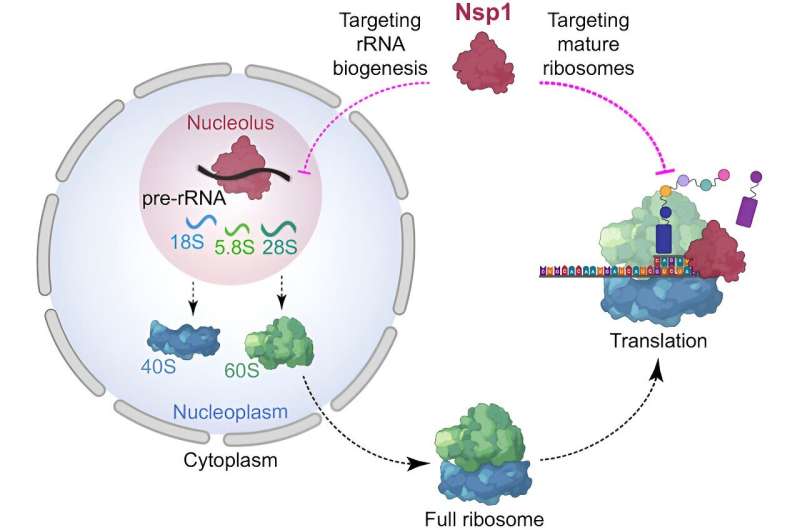
Wanneer SARS-CoV-2 onze cellen binnendringt, verstoort het het proces van het maken van eiwitten, die essentieel zijn voor de goede werking van onze cellen. Een specifiek SARS-CoV-2-eiwit genaamd Nsp1 speelt een cruciale rol in dit proces. Het verhindert dat ribosomen, de machinerie die eiwitten maakt, hun werk effectief doen. Het virus is als een slimme saboteur in onze cellen, die ervoor zorgt dat aan zijn eigen behoeften wordt voldaan, terwijl het vermogen van onze cellen om zichzelf te verdedigen wordt verstoord.
We ontdekten dat Nsp1 goed is in het blokkeren van de aanmaak van nieuwe eiwitten door ribosomen, maar ook de productie van nieuwe ribosomen verstoort. In feite schakelt het de productie van de machine uit en de mogelijkheid om de machine zelf te maken – een serieuze dubbele klap.
Het doet dit door de rijping of verwerking van gespecialiseerde RNA-moleculen die nodig zijn om ribosomen te bouwen, te blokkeren. Dit voegt een nieuwe laag van complexiteit toe aan ons begrip van de interferentie van SARS-CoV-2 met de gastheercel.
Hoe kan deze ontdekking de behandeling van mensen met COVID-19 beïnvloeden?
Voortbouwend op ons gepubliceerde onderzoek zal het van cruciaal belang zijn om te begrijpen hoe Nsp1 werkt om te voorkomen dat verschillende soorten menselijke cellen, weefsels en organen eiwitten aanmaken wanneer ze zijn geïnfecteerd met verschillende varianten van SARS-CoV-2 en gerelateerde coronavirussen.
Wetenschappers hebben gewerkt aan het vinden van precisiemedicijnen die Nsp1 kunnen tegengaan en kunnen helpen bij de strijd tegen het voortdurend evoluerende SARS-CoV-2-virus. Deze medicijnen zijn bedoeld om geïnfecteerde cellen te helpen eiwitten te blijven produceren en een robuuste immuunrespons op te bouwen bij het omgaan met infecties. Lopend onderzoek naar dergelijke medicijnen zou nu baat moeten hebben bij het testen of ze kunnen voorkomen dat Nsp1 interfereert met zowel de productie als de functie van ribosomen, en dit zou moeten helpen effectievere precisiemedicijnen te vinden.
Wat trok je aan in deze onderzoekslijn?
Dit project is gestart vanwege omstandigheden tijdens de COVID-lockdown. Wij wilden helpen in de strijd tegen de pandemie. Omdat ik echter niet fysiek in het laboratorium kon werken, maakten we van de gelegenheid gebruik om de volgende generatie sequencing-datasets computationeel vanuit huis te analyseren.
Toen we naar gepubliceerde RNA-sequencing-datasets keken, realiseerden we ons dat cellen die zijn geïnfecteerd met SARS-CoV-2, vergeleken met niet-geïnfecteerde cellen, moeite kunnen hebben met het verwerken van de RNA-moleculen die nodig zijn om ribosomen te bouwen. Door deze analyse hebben we samen met Dr. Mekhail hypothesen ontwikkeld en het project ontworpen.
Ik had het voorrecht om nauw samen te werken met de getalenteerde leden van het Mekhail-lab, waaronder de groep van Alexander Palazzo van de afdeling biochemie van Temerty Medicine en de laboratoria van Brian Raught en Razqallah Hakem van het Princess Margaret Cancer Center (University Health Network).
Dit werk zou niet mogelijk zijn geweest zonder de collectieve inspanningen van ons team en onze medewerkers, en ik ben dankbaar voor hun bijdragen. Mijn verantwoordelijkheden omvatten het uitvoeren van talloze praktische experimenten en bio-informatica-analyses, het analyseren van de resultaten en het voorbereiden van het artikel voor peer review en publicatie.
Wat waren de meest uitdagende en lonende aspecten van dit project?
Het meest uitdagende onderdeel was het uitvoeren van onderzoek tijdens een wereldwijde pandemie, die veel logistieke hindernissen met zich meebracht – van verstoorde laboratoriumroutines tot beperkingen bij het verzamelen en gebruiken van monsters die besmet waren met SARS-CoV-2.
Aan de andere kant was de kans om bij te dragen aan ons begrip van de virale mechanismen van SARS-CoV-2 en licht te werpen op potentiële therapeutische doelen ongelooflijk bevredigend. Het is zeer bevredigend om ons onderzoek te zien uitmonden in een gepubliceerd artikel en te weten dat dit als inspiratiebron kan dienen voor toekomstige strategieën voor de bestrijding van coronavirussen.
Wat zijn je langetermijndoelen als wetenschapper?
Als onafhankelijk onderzoeker in mijn toekomstige laboratorium wil ik bestuderen hoe de complexe processen van het maken van ribosomen de natuurlijke afweer van het lichaam tegen virussen beïnvloeden. Het is een gebied dat ik boeiend vind en dat volop mogelijkheden biedt voor verdere verkenning.
Eén benadering waarin ik vooral geïnteresseerd ben, is de integratie van RNA-sequencing met genetische CRISPR en chemische screenings van kleine moleculen, waarbij verschillende stadia van ribosoombiogenese worden aangepakt bij diverse infectie- of infectie-nabootsende omstandigheden.
Dergelijke geïntegreerde benaderingen zijn veelbelovend voor het blootleggen van nieuwe mechanismen die ten grondslag liggen aan de regulering van antivirale reacties en zouden ons moeten helpen innovatieve en impactvolle manieren te vinden om virale infecties te bestrijden.