
Wetenschap
DNA-reparatiemechanisme verder opgehelderd in cryo-elektronenmicroscopie-experiment
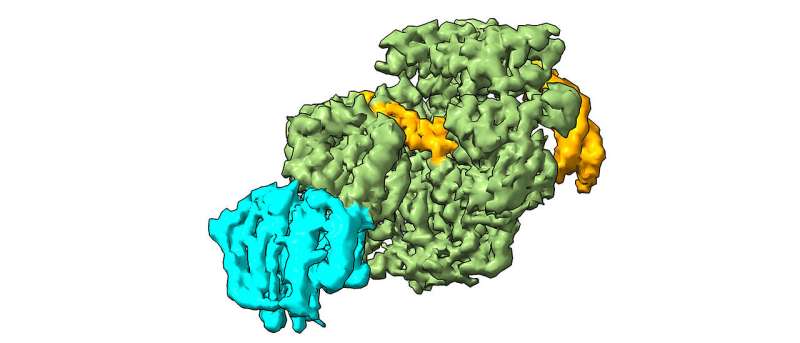
Onderzoekers hebben ontdekt hoe het eiwit XPD ernstige DNA-schade detecteert en de reparatie ervan regelt.
Het XPD-eiwit is een centraal onderdeel van ons lichaamseigen ‘DNA-reparatieteam’, bekend als nucleotide excisieherstel (NER). Net als een speurhond detecteert NER gemarkeerde schadegebieden, spoort het beschadigde DNA op en rekruteert andere reparatie-eiwitten om de defecte delen uit te snijden en te vervangen. Bij gezonde mensen voorkomt XPD bijvoorbeeld de ontwikkeling van huidkanker door UV-beschadigd DNA te detecteren en te repareren.
Een team van onderzoekers van de Universiteit van Würzburg (JMU) heeft nu voor het eerst precies ontdekt hoe het XPD-eiwit de aanwezigheid van DNA-schade kan detecteren en verifiëren. Het team werd geleid door biochemicus Caroline Kisker, voorzitter van Structurele Biologie aan het Rudolf Virchow Centrum in Würzburg, in samenwerking met de chemicus Claudia Höbartner van de afdeling Organische Chemie. De studie is gepubliceerd in Nature Structural &Molecular Biology .
Onderzoek naar ernstige DNA-schade
Het team uit Würzburg concentreerde zich op de manier waarop het XPD-eiwit werkt bij crosslinking tussen strengen – een van de ernstigste vormen van DNA-schade die we kennen. Het wordt bijvoorbeeld veroorzaakt door gifstoffen uit het milieu en industriële chemicaliën. "Interstrand crosslinking zorgt ervoor dat DNA tijdens de celdeling verkeerd wordt gekopieerd en gelezen", legt Kisker uit. "Dit leidt tot genetische schade die kanker kan veroorzaken."
In hun onderzoek gebruikten de wetenschappers cryo-elektronenmicroscopie om te analyseren hoe XPD de dubbele DNA-helix afwikkelt om de defecte plaatsen van cross-linking tussen de strengen bloot te leggen, en creëerden ze een model van hoe de schade wordt gedetecteerd en verwijderd.
"De bevindingen uit ons werk vormen de basis voor nieuwe benaderingen voor de behandeling van verschillende soorten kanker", zegt Jochen Kuper, lid van het team van Kisker. "Door specifiek reparatiemechanismen zoals NER in kankercellen te verzwakken, zouden we de effectiviteit van medicijnen aanzienlijk kunnen vergroten."
In verdere studies wil het onderzoeksteam onderzoeken hoe XPD verschillende andere soorten DNA-schade detecteert.