
Wetenschap
Onderzoekers brengen druggable genomische doelwitten in kaart in evoluerende malariaparasieten
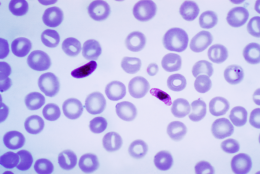
Deze microfoto van een bloeduitstrijkje bevat een macro- en microgametocyt van de parasiet Plasmodium falciparum. Krediet:Wikipedia.
Onderzoekers van de University of California San Diego School of Medicine, met collega's in het hele land en over de hele wereld, hebben volledige genoomanalyses en chemogenetica gebruikt om nieuwe medicijndoelen en resistentiegenen te identificeren in 262 parasietcellijnen van Plasmodium falciparum -protozoaire pathogenen die malaria veroorzaken - die resistent zijn tegen 37 verschillende antimalariamiddelen.
De studie, gepubliceerd in het nummer van 12 januari van Wetenschap , bevestigde eerder bekende genetische modificaties die substantieel bijdragen aan de resistentie tegen geneesmiddelen van de parasieten, maar onthulde ook nieuwe doelen die het begrip van de onderliggende biologie van de parasieten verdiepen.
"Deze verkenning van de P. falciparum resistoom - de verzameling van antibioticaresistentiegenen - en het voor geneesmiddelen geschikte genoom ervan zullen helpen bij het ontdekken van nieuwe geneesmiddelen en ons begrip vergroten van hoe de malariaparasiet evolueert om terug te vechten, " zei senior auteur Elizabeth Winzeler, doctoraat, hoogleraar farmacologie en medicijnontdekking bij de afdeling kindergeneeskunde van de UC San Diego School of Medicine.
P. falciparum is een eencellige protozoa die op mensen wordt overgedragen door de beet van geïnfecteerde Anopheles-muggen. Het is verantwoordelijk voor ongeveer de helft van alle malariagevallen. De enorm onevenredige impact van malaria op de menselijke gezondheid - de Wereldgezondheidsorganisatie schat dat er wereldwijd 216 miljoen gevallen waren en 445, 000 sterfgevallen in 2016 - is deels te wijten aan de bijzondere bedrevenheid van de parasieten in het veranderen van genomen om medicamenteuze behandeling en het menselijke immuunsysteem te ontwijken en te weerstaan.
"Een enkele menselijke infectie kan ertoe leiden dat een persoon meer dan een biljoen aseksuele parasieten in het bloedstadium bevat, " zei Winzeler. "Zelfs met een relatief langzame willekeurige mutatiesnelheid, deze cijfers zorgen voor een buitengewoon aanpassingsvermogen. In slechts een paar cycli van replicatie, de P. falciparum genoom kan een willekeurige genetische verandering krijgen die ten minste één parasiet resistent kan maken tegen de activiteit van een medicijn of een door de mens gecodeerd antilichaam."
Een dergelijke snelle evolutie stelt aanzienlijke uitdagingen voor het beheersen van de ziekte, zeiden onderzoekers, maar het kan ook worden misbruikt in vitro om precies te documenteren hoe de parasiet evolueert in aanwezigheid van bekende antimalariamiddelen om resistentie tegen geneesmiddelen te creëren. Het kan ook worden gebruikt om nieuwe doelwitten voor geneesmiddelen te onthullen.
In plaats van zich te concentreren op de interactie van parasieten met afzonderlijke verbindingen of enkele verdachte genen te onderzoeken in P. falciparum , Winzeler en collega's gebruikten sequencing van het hele genoom en een diverse reeks antimalariaverbindingen. De resulterende dataset onthulde een diversiteit aan mutaties. Resistente parasieten bevatten vaak een mutatie in een vermoedelijk doelwitgen en aanvullende mutaties in andere, niet-verwante genen.
"Onze bevindingen toonden en onderstreepten de uitdagende complexiteit van geëvolueerde resistentie tegen geneesmiddelen in P. falciparum , " zei Winzeler, "maar ze identificeerden ook nieuwe medicijndoelen of resistentiegenen voor elke verbinding waarvoor resistente parasieten werden gegenereerd. Het onthulde het gecompliceerde chemogenetische landschap van P. falciparum , maar bood ook een potentiële gids voor het ontwerpen van nieuwe remmers van kleine moleculen om deze ziekteverwekker te bestrijden."
 We kunnen Australië niet droogtebestendig maken, en proberen is een dwaze boodschap
We kunnen Australië niet droogtebestendig maken, en proberen is een dwaze boodschap De hitte gaat maar door:juni de meest geroosterde ooit, Juli kan volgen
De hitte gaat maar door:juni de meest geroosterde ooit, Juli kan volgen Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific
Onderzoeker doet ontdekking van diepzeekoraalriffen in de diepten van de Noord-Pacific Koolstof volgen van het oceaanoppervlak tot in de diepte
Koolstof volgen van het oceaanoppervlak tot in de diepte Gesloten kringloopsystemen die astronauten in de ruimte in leven houden, kunnen de basis vormen voor strategieën voor circulaire economie
Gesloten kringloopsystemen die astronauten in de ruimte in leven houden, kunnen de basis vormen voor strategieën voor circulaire economie
Hoofdlijnen
- Het verschil tussen hoe interne en externe regulatoren werken
- Uitwerpselen van verstrikte Noord-Atlantische walvissen onthullen torenhoge stressniveaus
- Wat is de regeling in de microbiologie?
- Landbouwgroepen dagen waarschuwing onkruidverdelger in Californië uit
- Zwaarste beenvissen ter wereld geïdentificeerd en correct benoemd
- Een Chromosome-diagram interpreteren
- Waar vindt ademhaling plaats?
- Mensen waren de Neanderthalers niet te slim af,
- Hoe is het schrijven geëvolueerd?
- Omgaan met antibiotica niet genoeg om resistentie om te keren

- Selenium beschermt specifieke interneuronen in de hersenen
- Wetenschappelijke evaluatie van neushoorndiëten verbetert dierentuin

- In het laboratorium gekweekt vlees zou de mensheid een ernstig moreel falen kunnen laten negeren

- In beweging blijven - platte wormen werpen licht op de rol van migrerende stamcellen bij kanker
 NASA-ingenieurs ontwikkelen zwarter dan zwarte nanobuisjes (met video)
NASA-ingenieurs ontwikkelen zwarter dan zwarte nanobuisjes (met video) Holografische benadering verbetert heads-up-displays voor vliegtuigen en auto's
Holografische benadering verbetert heads-up-displays voor vliegtuigen en auto's Onderzoekers ontwikkelen nieuwe techniek die licht gebruikt om gespiegelde moleculen te scheiden
Onderzoekers ontwikkelen nieuwe techniek die licht gebruikt om gespiegelde moleculen te scheiden De warmste winter in Moskou sinds het begin van de records:weerservice
De warmste winter in Moskou sinds het begin van de records:weerservice Wetenschapper ontwikkelt game om gebruikers te wapenen tegen nepnieuws over klimaatverandering
Wetenschapper ontwikkelt game om gebruikers te wapenen tegen nepnieuws over klimaatverandering Onderzoekers ontwikkelen voorspellend model voor het meten van lachgasemissies in beken en rivieren
Onderzoekers ontwikkelen voorspellend model voor het meten van lachgasemissies in beken en rivieren ONS, China bereikt een ZTE-deal van $ 1,4 miljard naarmate er tekenen verschijnen van voortgang van de handelsbesprekingen
ONS, China bereikt een ZTE-deal van $ 1,4 miljard naarmate er tekenen verschijnen van voortgang van de handelsbesprekingen Raket met 1e door de VAE gemaakte satelliet gelanceerd vanuit Japan
Raket met 1e door de VAE gemaakte satelliet gelanceerd vanuit Japan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

