
Wetenschap
Het genoom van Leishmania onthult hoe deze parasiet zich aanpast aan veranderingen in de omgeving
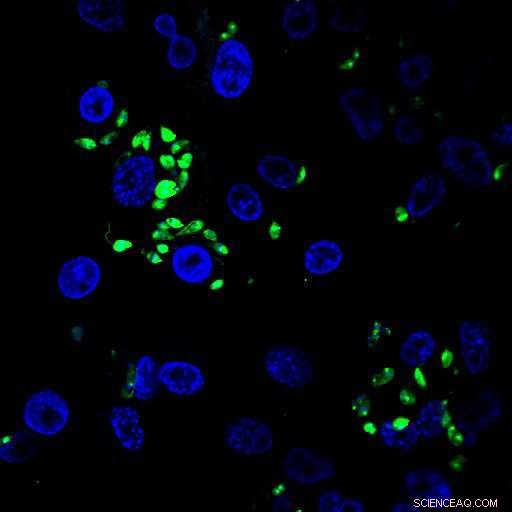
Krediet:Centrum voor genomische regulering
Leishmaniasis is een belangrijke ziekte bij mens en dier die wordt veroorzaakt door Leishmania-parasieten en die 12 miljoen mensen treft in meer dan 98 endemische landen. De ziekte duikt nu op in Europa als gevolg van klimaatverandering en massale ontheemding van de bevolking. Het is bekend dat de parasiet zich snel aanpast aan nieuwe omgevingen met belangrijke gevolgen voor de uitkomst van de ziekte. Het is daarom erkend als een opkomende bedreiging voor de volksgezondheid voor de EU.
In een krant, gepubliceerd in Natuur Ecologie &Evolutie , wetenschappers van het Institut Pasteur in Parijs en het Centre for Genomic Regulation (CRG) in Barcelona, in samenwerking met teams van het Instituut voor Tropische Geneeskunde Antwerpen (ITG) en de Universiteit van Montpellier, hebben nu aangetoond dat aanpassing aan Leishmania het gevolg is van frequente en omkeerbare chromosomale amplificaties. dergelijke variaties, aneuploïdieën genoemd, zijn vergelijkbaar met die welke bij veel kankertypes voorkomen.
Deze bevindingen vormen een belangrijke stap naar een beter begrip van de menselijke Leishmania-infectie, met relevantie voor resistentie tegen parasietgeneesmiddelen, pathogeniteit, en weefseltropisme. Dit nieuwe inzicht in de genomische instabiliteit van Leishmania zou de weg moeten effenen voor de identificatie van resistentiemechanismen tegen parasietgeneesmiddelen in klinisch relevante omgevingen en helpen bij het ontdekken van biomarkers met diagnostische en prognostische waarde.
Leishmaniasis behoort tot de vijf belangrijkste parasitaire ziekten wereldwijd, met naar schatting 350 miljoen mensen met een risico op infectie. De ziekte veroorzaakt een spectrum van klinische manifestaties, variërend van ontsierende cutane tot fatale viscerale vormen, die het gevolg is van infectie door verschillende soorten Leishmania-parasieten. Deze eencellige parasieten passen zich aan een opmerkelijke reeks gastheren aan. Ze groeien als extracellulaire parasieten in phlebotomine-zandvliegen die Leishmania overbrengen op verschillende gewervelde dieren, zoals knaagdieren, honden, en mensen, waar ze groeien in immuuncellen, met name macrofagen, veroorzaakt ernstige pathologieën die tot de dood kunnen leiden.
Leishmaniasis is een van de meest verwaarloosde ziekten en trekt daardoor weinig aandacht. Er is geen menselijk vaccin en er zijn maar weinig behandelingen beschikbaar, die allemaal een of meer belangrijke beperkingen vertonen met betrekking tot de administratie, toxiciteit of kosten. Nog erger, een kenmerk van Leishmania-biologie is toevallig zijn vermogen om zich aan te passen aan een verscheidenheid aan onvoorspelbare fluctuaties binnen zijn menselijke gastheer, met name farmacologische interventies, met belangrijke gevolgen voor de uitkomst van de ziekte, zoals blijkt uit de opkomst van geneesmiddelresistente klinische isolaten.
Om de genetische mechanismen te identificeren die de genomische aanpassing van Leishmania stimuleren, wetenschappers van het Institut Pasteur in Parijs en het Centre for Genomic Regulation (CRG) in Barcelona, in samenwerking met teams van het Instituut voor Tropische Geneeskunde Antwerpen (ITG) en de Universiteit van Montpellier nieuwe technieken ontwikkeld voor vergelijkende genomica, gebaseerd op next generation sequencing en in-silico analyses. Hun werk, die is gepubliceerd in Natuurecologie en evolutie , toont voor het eerst het bestaan in Leishmania aan van een verband tussen veranderingen in het aantal kopieën van chromosomen en de selectie van nieuwe allelen die belangrijk zijn voor de overleving van parasieten.
Het meest verrassende aspect van dit werk is de observatie dat Leishmania erin slaagt allelselectie te combineren met het behoud van een hoge genetische diversiteit. Normaal gesproken moeten deze twee processen elkaar uitsluiten, en je zou verwachten dat een parasiet onder sterke selectie snel zijn genetische diversiteit verliest. In Leishmanië, echter, de zeer frequente chromosomale duplicaties maken het mogelijk om beide te combineren. Inderdaad, de parasiet behoudt zijn diversiteit doordat dezelfde combinatie van allelen gelijktijdig kan worden geselecteerd in genetisch diverse individuen.
Gerard Späth, Directeur van de afdeling Moleculaire Parasitologie en Signalering van het Institut Pasteur in Parijs, die het experimentele deel van deze studie leidde, opmerkingen:"Basis, toegepast, en klinisch onderzoek in Leishmania wordt bijna uitsluitend uitgevoerd met parasieten uit een langetermijncultuur. Ons onderzoek toont aan dat het parasietgenoom onder laboratoriumomstandigheden zeer snel evolueert. Hiermee moet rekening worden gehouden bij het bestuderen van de parasietbiologie en het zoeken naar nieuwe biomarkers, verdovende middelen, of vaccinkandidaten. De toekomst van Leishmania-onderzoek moet op een meer integratieve manier worden uitgevoerd, gezien de complexe genetische interacties tussen parasieten, gewervelde gastheer en insectenvector, en onder klinisch relevante omstandigheden, bijvoorbeeld met behulp van parasieten uit kortdurende kweek of directe weefselsequencing".
Cedric Notredame, Senior hoofdonderzoeker bij het Center for Genomic Regulation in Barcelona, die het vergelijkende genomics-gedeelte van deze studie leidde, legt uit:"Het idee dat genamplificatie een snelweg voor aanpassing is, bestaat al lang, maar ons werk laat zien dat in Leishmania, evolutie heeft dit mechanisme zo opgeschaald dat het een essentieel onderdeel is geworden van de levenscyclus van de parasiet. Een toenemend oeuvre toont aan dat vergelijkbare complexe aneuploïdievariaties een rol spelen bij sommige vormen van kanker en we denken dat de snelle accumulatie van NGS-genomicsgegevens in combinatie met nieuwe in-silicotechnieken - zoals die ontwikkeld in onze studie - binnenkort zal leiden tot een beter begrip van de relaties tussen aneuploïdie en allelselectie".
Professor Jean-Claude Dujardin van het ITG benadrukt:"Het kostte ons meer dan vijf jaar om een ongekende reeks sequentiegegevens van klinische isolaten in het Indiase subcontinent te verzamelen en vorig jaar een eerste analyse te publiceren. Een mooi kenmerk van de moderne wetenschap is dat alle sequentiegegevens moeten openbaar worden gemaakt, die nieuwe samenwerkingen en onderzoeken zoals de onze mogelijk maakt. Het maakte ook de oprichting mogelijk van een nieuwe alliantie tussen het ITG, Institut Pasteur en CRG in de strijd tegen infectieziekten."
De resultaten van deze originele studie zijn zeer relevant voor andere menselijke ziekten die afhankelijk zijn van genoominstabiliteit, zoals een schimmelinfectie of kanker, en nieuwe locaties openen voor de ontdekking van geneesmiddelen tegen leishmania met behulp van gastheergerichte strategieën die zich richten op de metabole afhankelijkheid van de parasiet van de gastheercel, waardoor de adaptieve evolutie van geneesmiddelresistente parasieten wordt voorkomen.
Op basis van de resultaten die in dit artikel zijn gepubliceerd, en met als doel de biologie en epidemiologie van Leishmania te bestuderen in een klinisch relevantere context, Dr. Gerald Späth richtte het internationale consortium 'LeiSHield' op, dat een gezamenlijke inspanning coördineert tussen partnerteams van het Institut Pasteur International Network en daarbuiten, die aanvankelijk werd ondersteund door een startfonds van het Institut Pasteur International Direction, en wordt nu gefinancierd door een subsidie van 1,7 miljoen euro van het EU H2020-programma.
 Aangekapte inheemse bossen eindigen meestal op stortplaatsen, niet in gebouwen en meubels
Aangekapte inheemse bossen eindigen meestal op stortplaatsen, niet in gebouwen en meubels Orkaan Douglas raast over Hawaï terwijl pandemie oplaait
Orkaan Douglas raast over Hawaï terwijl pandemie oplaait Gewasbesparende bodemtesten nu binnen handbereik van boeren
Gewasbesparende bodemtesten nu binnen handbereik van boeren Tropische bomen gebruiken unieke methode om droogte te weerstaan
Tropische bomen gebruiken unieke methode om droogte te weerstaan Grondwateraanvullingspercentages in kaart gebracht voor Afrika
Grondwateraanvullingspercentages in kaart gebracht voor Afrika
Hoofdlijnen
- Wat zijn de meest voorkomende oorzaken van uitsterven?
- Batesiaanse mimiek:hoe copycats zichzelf beschermen
- Vingerafdrukexperimenten
- Een rol van lipiden bij celdeling
- Het opzetten van een genoombrede kaart van bacteriële genen die cruciaal zijn voor de kolonisatie van planten door nuttige microben
- De internationale Human Cell Atlas publiceert strategische blauwdruk, kondigt gegevens aan van de eerste miljoen cellen
- Kan gentherapie kaalheid genezen?
- Wat is het oudste levende wezen op aarde?
- Sequentiebepaling van het genoom van stevia-planten voor het eerst onthuld
- 85 nieuwe soorten beschreven door de California Academy of Sciences in 2017

- Hoe zijn schimmels en planten vergelijkbaar?

- De oorsprong van genen voor het maken van bloemen

- Depolarisatie en repolarisatie van het celmembraan

- Sardines nemen ons mee naar de bronnen van biodiversiteit in de Amazone-rivier

 NASA ziet Debby overgaan in een tropische storm
NASA ziet Debby overgaan in een tropische storm Snelheid plus controle in nieuwe computerchip - het vertragen van licht naar geluid
Snelheid plus controle in nieuwe computerchip - het vertragen van licht naar geluid Vroege Noord-Amerikanen waren mogelijk diverser dan eerder werd vermoed
Vroege Noord-Amerikanen waren mogelijk diverser dan eerder werd vermoed Amerikanen gebruiken elke dag 500 miljoen rietjes. Zou je beloven om Strawless te gaan?
Amerikanen gebruiken elke dag 500 miljoen rietjes. Zou je beloven om Strawless te gaan?  Evacuaties aangedrongen in de buurt van Guatemala's uitbarstende vulkaan van vuur
Evacuaties aangedrongen in de buurt van Guatemala's uitbarstende vulkaan van vuur Amerikaanse inlichtingenchef waarschuwt voor klimaatverandering
Amerikaanse inlichtingenchef waarschuwt voor klimaatverandering De soorten flessen die worden gebruikt voor het opslaan van zuren en basen
De soorten flessen die worden gebruikt voor het opslaan van zuren en basen Fruitvliegjes en elektronen:onderzoekers gebruiken natuurkunde om het gedrag van mensenmassa's te voorspellen
Fruitvliegjes en elektronen:onderzoekers gebruiken natuurkunde om het gedrag van mensenmassa's te voorspellen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

