Wetenschap
Hoe CRISPR-genbewerking werkt
Mutanten zijn cool, Rechtsaf? X-mannen, Teenage Mutant Ninja Turtles en superhelden in stripboeken en films verbazen ons met de speciale krachten die zijn afgeleid van hun genetische mutaties. Echter, die fictieve genetische mutaties zijn nogal moeilijk te verkrijgen - je moet zijn gebeten door een speciale spin of blootgesteld aan een radioactieve stof.
Maar wat als het doen van genetische modificaties niet alleen gemakkelijk was, maar snel en goedkoop, te? Zou je vrijwillig een mutant willen worden? We zullen, met een technologie genaamd CRISPR, je kunt het misschien wel. Begrijp ons niet verkeerd - CRISPR zal je niet in een superheld veranderen, maar deze wetenschappelijke ontdekking heeft het potentieel om een grote impact op ons te hebben.
Kort voor geclusterde regelmatige tussenruimten korte palindroomherhalingen , CRISPR maakt het voor ons mogelijk om genen van elk levend wezen naar een ander te verplaatsen, DNA veranderen voor toekomstige generaties. Het stelt ons in staat genen weg te snijden die vreselijke dingen doen - zoals die welke ziekte veroorzaken - en ze te vervangen door DNA-segmenten die onschadelijk zijn.
Tegelijkertijd, CRISPR-technologie is zo krachtig dat mensen het kunnen gaan gebruiken voor meer dan alleen het genezen van mensen met een ziekte. Misschien om meer ziekteresistente gewassen en vee te creëren. Of om gistmutanten te maken die brandstoffen produceren die we kunnen gebruiken om onze auto's aan te drijven. Misschien worden we heel creatief en maken we designerbaby's, of zelfs de technologie voor het kwaad gebruiken - biowapens ontwerpen die soortspecifiek zijn en hele soorten van de aardbodem wegvagen.
Naarmate we meer leren over wat de MIT Technology Review "de grootste biotech-ontdekking van de eeuw" noemde, "We moeten ook nadenken over wanneer we CRISPR moeten gebruiken en hoe het moet worden gereguleerd.
Inhoud
- Bacteriële moordenaars
- Designer baby's, Invasieve mutanten en doe-het-zelfbiologie
Bacteriële moordenaars
Hoewel de CRISPR-technologie behoorlijk geweldig is, mensen die verschillende organismen genetisch modificeren, is niets nieuws. Aan de low-tech kant, we telen al heel lang selectief gewassen. Toen boeren een sappige sinaasappel of een felgekleurde tomaat tegenkwamen, ze behielden die gewenste genen door zaden van die plant te planten.
Maar de laatste jaren is we hebben de biotechnologie een tandje bijgezet. In het begin van de jaren 2000, wetenschappers ontdekten hoe ze enzymen konden gebruiken, zinkvingernucleasen genoemd, om specifieke ongewenste genen in een verscheidenheid aan organismen te verwijderen en te vervangen. De zinkvinger enzymen, echter, waren duur (meer dan $ 5, 000 per pop), moeilijk te maken, en het slagingspercentage was niet optimaal [bron:Ledford].
Dus terwijl de technologie om genen te bewerken er was, pas toen CRISPR opkwam, voelde het idee om het DNA van een organisme opzettelijk te veranderen binnen handbereik. De eerste verwijzing naar CRISPR was in een tijdschriftartikel uit 1987 waarin wetenschappers rapporteerden dat ze de korte herhalingen van DNA vonden die de basis vormen van de technologie in E coli bacteriën. Maar pas in 2012 werd CRISPR relevant. Vanaf dat moment, het gebruik van CRISPR is enorm gestegen in de wetenschappelijke gemeenschap. Er is meer dan een miljard dollar opgehaald als startkapitaal voor biotechnologiebedrijven die de techniek gebruiken [bron:Ledford]. Overheidsfinanciering voor CRISPR-onderzoek gaat ook door het dak.
Alleen al in 2014 bijna $ 90 miljoen werd toegezegd door de National Institutes of Health voor CRISPR-onderzoek [bron:Ledford]. En sinds 2010 meer dan 200 patenten met betrekking tot CRISPR zijn ingediend [bron:Ledford]. Het snelle tempo van het onderzoek lijkt niet te vertragen. Naarmate wetenschappers meer leren over CRISPR, het lijkt erop dat ze minder leren over hoe de techniek beperkt is en in plaats daarvan over hoe krachtig het is. t
Dus wat is het aan deze techniek dat het zo krachtig maakt?
Designer baby's, Invasieve mutanten en doe-het-zelfbiologie
In 1987, wetenschappers studeren E coli ontdekte herhaalde segmenten in het DNA van de bacterie. Dit type patroon in bacterieel DNA is ongebruikelijk, dus ze fleurden op toen ze het merkten, en deed verslag van de vondst. Overuren, wetenschappers begonnen dit patroon te zien in veel verschillende soorten bacteriën, maar er was nog steeds geen hypothese over wat het was en waarom het daar was. Maar in 2005, een zoekopdracht in een DNA-database toonde aan dat de "geclusterde regelmatig interspaced korte palindroomherhalingen" (of CRISPR) overeenkwamen met virus-DNA.
Maar waarom zouden bacteriën virus-DNA hebben opgeborgen? Wetenschapper Eugene Koonin veronderstelde dat wanneer bacteriën een virusaanval overleven, ze snijden het virus in kleine stukjes en slaan een deel van het virus-DNA op in hun eigen genoom, zodat ze het virus later kunnen herkennen en aanvallen als ze het toevallig weer tegenkomen. Ze bewaren in feite een foto van het virus in hun achterzak, zodat ze de slechterik zouden herkennen als hij ooit weer zou opduiken - een opmerkelijk verdedigingsmechanisme van het bacteriële immuunsysteem.
De hypothese van Koonin was juist. Als dat virus weer toeslaat, de bacteriën maken speciale 'moordenaars'. Deze moordenaars kunnen de RNA-sequentie lezen van elk virus-DNA dat ze tegenkomen, herkennen of het overeenkomt met de informatie die ze in hun DNA hebben opgeslagen, vang het op en hak het fijn. Het is alsof de bacterie heel specifieke, slimme schaar.
Deze ontdekking was best cool, maar niet zo cool als wat de Universiteit van Californië, Berkeley-wetenschapper Jennifer Doudna (die sindsdien samen met Emmanuelle Charpentier de Nobelprijs voor Scheikunde 2020 heeft gewonnen voor hun werk aan CRISPR) dacht met de informatie te maken te hebben. Ze suggereerde dat wetenschappers CRISPR zouden kunnen gebruiken als een hulpmiddel om genen te bewerken. Als ze de bacteriën zouden voorzien van een DNA-segment waarvan bekend is dat het slecht is - laten we zeggen een gen dat blindheid veroorzaakt - zouden ze de bacteriën kunnen sturen om het slechte gen op te sporen, waar de bacteriën het zouden vinden en vermoorden. En dan zouden we kunnen profiteren van het natuurlijke herstelmechanisme in de bacteriecellen om een meer wenselijk gen op zijn plaats te gooien [bron:RadioLab].
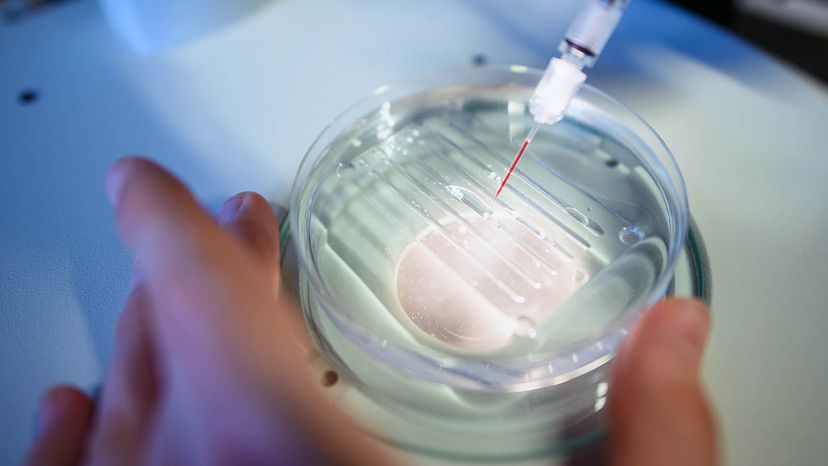
Het werkte! En het bleef werken! Het omkeren van blindheidsmutaties is slechts een van de manieren waarop is aangetoond dat CRISPR werkt. Het stopt de vermenigvuldiging van kankercellen, maakte cellen ondoordringbaar voor HIV, heeft ons geholpen om ziekteresistente tarwe en rijst te creëren, en talloze andere vorderingen. anno 2015, Chinese wetenschappers probeerden zelfs de technologie te gebruiken op niet-levensvatbare menselijke embryo's, maar in slechts enkele gevallen maakte CRISPR de juiste sneden in het DNA [bron:Maxmen].
Maar dit roept de vraag op:willen we het zelfs op embryo's gebruiken? Moeten we dat toestaan? Wie gaat het gebruik van CRISPR reguleren?
Veel meer informatie
CRISPR-technologie is zo relatief nieuw dat de wetenschappelijke gemeenschap de kracht ervan nog niet volledig heeft begrepen. Maar één ding is zeker:ze weten dat het vermogen om het menselijk ras te beïnvloeden, door geen enkele andere biotechnologie kan worden geëvenaard. Met dat grote potentieel, de noodzaak om regelgeving rond het gebruik ervan te ontwikkelen is absoluut noodzakelijk. Maar door het razend tempo waarin onderzoek in het lab plaatsvindt, is er weinig tijd over voor discussie over wat de regels rondom onderzoek en gebruik zouden moeten zijn. Het klinkt geweldig dat CRISPR slechte, ongewenste genen en vervang ze door meer wenselijke. Maar wie bepaalt wat slecht en wat goed is?
Zonder enige regelgeving, CRISPR zou zo ontwikkeld kunnen worden dat het veilig op een menselijk embryo kan worden gebruikt om zijn DNA te veranderen. Zou een van de ouders nee zeggen tegen CRISPR als ze zouden ontdekken dat hun kind het gen voor de ZvH had en dat CRISPR het zou kunnen verwijderen voordat de baby werd geboren? En als we ouders deze beslissingen zouden laten nemen over het knoeien met het DNA van hun baby voordat hij of zij wordt geboren, waar zou dat stoppen? Zouden ze kunnen besluiten om hun baby lang te maken in plaats van klein? Blond in plaats van brunette? De veranderingen die ouders zouden kunnen kiezen om aan hun kind door te geven, zouden blijvende veranderingen zijn die van generatie op generatie zouden worden doorgegeven. Als dit scenario zich afspeelt, het is gemakkelijk in te zien hoe het de kloof tussen hebben en hebben-niets zou kunnen vergroten. En we weten niet wat er op de lange termijn kan gebeuren met een kind wiens genen worden vervangen.
in december 2015, een groep wetenschappers, bio-ethici en beleidsexperts uit verschillende landen kwamen bijeen om te praten over het reguleren van menselijke genbewerking. Een Amerikaanse deskundige zei dat de Food and Drug Administration niet alleen de technologie moest reguleren, maar ook het specifieke gebruik ervan om off-label gebruik te voorkomen. Ze zei ook dat er mogelijk meer risico is bij het bewerken van plantengenen dan bij het bewerken van menselijke genen [bron:Regulatory Affairs Professionals Society].
Met de grote kracht van deze technologie, vragen over CRISPR moeten apart worden beantwoord van die over genetisch gemodificeerde organismen. Iedereen over de hele wereld op één lijn krijgen, echter, zal een uitdaging blijven.
Oorspronkelijk gepubliceerd:3 mei 2016
Veel meer informatie
Opmerking van de auteur:Hoe CRISPR-genbewerking werkt
Het schrijven van dit soort artikelen maakt me bang. Deze technologie is zo, zo spannend. De implicaties lijken over het algemeen zo erg cool, maar het voelt ook alsof we zo veel beginnen uit te vinden over hoe we het leven kunnen manipuleren met technologie dat we het op een gegeven moment zullen verknoeien. CRISPR geeft ons zoveel kracht - en op manieren die we niet kunnen voorzien. De wereld werkt goed, je weet wel? Er mee rommelen is gewoon eng. Nogmaals, hoe kunnen we zo'n krachtige techniek negeren die ons op zoveel manieren kan helpen?
gerelateerde artikelen
- 10 misvattingen over GGO's
- Hoe evolutie werkt
- Hoe genenbanken werken
- Is het ethisch om stamcellen te gebruiken?
Meer geweldige links
- Radiolab:Antilichamen Deel 1:CRISPR
- Wired Magazine:The Genesis Engine
bronnen
- Brennan, Zacharias. "Menselijk gen bewerken, CRISPR en FDA:hoe gaan ze samen?" Regulatory Affairs Professional Society. 2 december 2015. (29 april 2016) http://www.raps.org/Regulatory-Focus/News/2015/12/02/23708/Human-Gene-Editing-CRISPR-and-FDA-How-Will-They-Mix/
- Bruin, Kristen V. "In de garagelabs van doe-het-zelf-genhackers, wiens hobby je misschien angst aanjaagt." Fusion. 29 maart, 2016. (13 april 2016) http://fusion.net/story/285454/diy-crispr-biohackers-garage-labs/
- Ledford, Heidi. "CRISPR, de disruptor." Nature. Volume 522. Pagina's 20-24. 2015.
- Ledford, Heidi. "CRISPR, de disruptor." Nature. Volume 522. Pagina's 20-24. 2015.http://www.nature.com/news/crispr-the-disruptor-1.17673
- Maxmen, Amy. "De Genesis-motor." Bedrade. Augustus 2015. (13 april 2016) http://www.wired.com/2015/07/crispr-dna-editing-2/
- Radiolab. "Antilichamen Deel 1:CRISPR" 6 juni 2015. (13 april 2016) http://www.radiolab.org/story/antibodies-part-1-crispr/
- Regalado, Antonio. "Wie is de eigenaar van de grootste biotech-ontdekking van de eeuw?" MIT Technologie Review. 4 december 2014. (19 april, 2016) https://www.technologyreview.com/s/532796/who-owns-the-biggest-biotech-discovery-of-the-century/
- Piet, Jessica. Afgestudeerd student scheikunde, Emory-universiteit. Persoonlijke correspondentie. 13 april 2015.
- Stoye, Emma. "Crispr-bewerkte paddenstoel ontwijkt regelgeving." Chemie wereld. 26 april 2016. (29 april, 2016) http://www.rsc.org/chemistryworld/2016/04/crispr-gene-editing-mushroom-dodges-gmo-regulation
- Zimmer, Karel. "Doorbraak DNA-editor geboren uit bacteriën." Quanta Magazine. 6 februari 2015. (13 april 2016) https://www.quantamagazine.org/20150206-crispr-dna-editor-bacteria/
Hoofdlijnen
- Kan slapen me gelukkig maken?
- Plantaanpassingen: woestijn, tropisch regenwoud, toendra
- Drie manieren waarop genetische diversiteit optreedt tijdens Meiosis
- Wat is de structuur van stamcellen?
- De betekenis van Penta E
- De effecten van straling op dieren
- Wat is een endotherme reactie?
- De soorten cellen die aan een membraan gebonden zijn Nucleus
- Wat zijn lange ketens van aminozuren genaamd?
 Hoe te berekenen Mislukkingspercentages
Hoe te berekenen Mislukkingspercentages  Een lijst met discrepante activiteiten op het gebied van evenementen
Een lijst met discrepante activiteiten op het gebied van evenementen Wat is het verschil tussen nominale en originele gegevens?
Wat is het verschil tussen nominale en originele gegevens?  Ben je veilig voor bliksem als de lucht helder is?
Ben je veilig voor bliksem als de lucht helder is?  Wat is een halfedelsteen?
Wat is een halfedelsteen?  Hoe wordt aardgas gedolven?
Hoe wordt aardgas gedolven?  Hoe verschilt een elektromagneet van een gewone staafmagneet?
Hoe verschilt een elektromagneet van een gewone staafmagneet?  De Stridsvagn 103 Main Battle Tank
De Stridsvagn 103 Main Battle Tank
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com