
Wetenschap
Heeft Thompson de elektronenwolk bedacht?
Hier is een uitsplitsing:
* J.J. Thomson (1897): Ontdekte het elektron en stelde het "pruimpudding" -model voor. Dit model stelde het atoom voor als een sfeer van positieve lading met negatief geladen elektronen ingebed daarin.
* Ernest Rutherford (1911): Door zijn goudfolie -experiment weerlegde Rutherford het pruimpuddingmodel. Hij stelde het nucleaire model voor, dat een positief geladen kern in het midden van het atoom plaatste, met elektronen die eromheen draaien.
* Niels Bohr (1913): Gebouwd op het model van Rutherford, die het idee introduceert van gekwantiseerde energieniveaus voor elektronen. Het model van Bohr afbeeldde echter nog steeds elektronen als een baan om de kern in gedefinieerde paden.
* Elektronenwolkmodel (1920 - 1930s): Ontwikkeld op basis van de principes van de kwantummechanica, vertegenwoordigt het elektronenwolkmodel elektronen niet als deeltjes die een kern draaien, maar als waarschijnlijkheidsverdelingen. Dit betekent dat de locatie van een elektron niet met zekerheid kan worden bekend, alleen de kans om het in een bepaalde regio te vinden.
Daarom kwam het elektronenwolkmodel tot stand als gevolg van verdere vooruitgang in de atomaire theorie, voortbouwend op het werk van wetenschappers zoals Thomson, Rutherford en Bohr.
 De vroege aarde werd gebombardeerd door een reeks asteroïden ter grootte van een stad
De vroege aarde werd gebombardeerd door een reeks asteroïden ter grootte van een stad Een van Europa's laatste ongetemde rivieren wordt bedreigd door dammen
Een van Europa's laatste ongetemde rivieren wordt bedreigd door dammen Onderzoekers ontdekken een oorzaak voor de opwarming van het noordpoolgebied in het begin van de 20e eeuw
Onderzoekers ontdekken een oorzaak voor de opwarming van het noordpoolgebied in het begin van de 20e eeuw Koolstofstudie in Amazonewoud onthult inheemse gebieden, beschermde gebieden belegerd, toch de beste klimaatoplossing blijven
Koolstofstudie in Amazonewoud onthult inheemse gebieden, beschermde gebieden belegerd, toch de beste klimaatoplossing blijven Na de storm:goedkope luchtkwaliteitsmonitoren gemeten verontreinigende stoffen in Puerto Rico na orkaan Maria
Na de storm:goedkope luchtkwaliteitsmonitoren gemeten verontreinigende stoffen in Puerto Rico na orkaan Maria
Hoofdlijnen
- Parasitaire worm speelt waarschijnlijk een rol bij de achteruitgang van elandpopulaties
- Wat is het vermogen van een organisme om intern en extern te veranderen in relatie tot zijn omgeving?
- Waarom hebben zich zoveel nieuwe ziekten ontwikkeld in de sector salades in zakken?
- Zijn Chewbacca en Bigfoot gerelateerd?
- Wat is fotosytem I en II?
- Is embryo -stamcelonderzoek moraal?
- EP-leden dringen aan op onderzoek naar de invloed van Monsanto op onderzoek
- Onderzoekers ontdekken aanwijzingen over hoe de nek van giraffen is geëvolueerd
- Wat zijn de verschillen in sets van allelen tussen individuen die een populatie heeft genoemd?
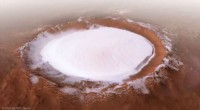
- Mars Express wordt feestelijk:een winterwonderland op Mars
- Nieuw melkwegonderzoek om het uitdijende heelal te meten

- 10 gedenkwaardige meteoorcrashes

- Heeft Cassini bij Titan een universele driver voor prebiotische chemie gevonden?

- Delen van onbemand Russisch ruimteschip verbranden boven Dubai (update)

 organen? - Antwoorden
organen? - Antwoorden  Wat is de eenheid van grijze pixelintensiteit?
Wat is de eenheid van grijze pixelintensiteit?  Hoe kun je aniline en primair amine onderscheiden?
Hoe kun je aniline en primair amine onderscheiden?  Hoe maak je het gemakkelijker om plantaardig afval om te zetten in biobrandstoffen?
Hoe maak je het gemakkelijker om plantaardig afval om te zetten in biobrandstoffen? Landgebruiksplanning voorkomt misbruik van natuurlijke hulpbronnen in Tanzania
Landgebruiksplanning voorkomt misbruik van natuurlijke hulpbronnen in Tanzania Elektronen bijeengedreven met behulp van nieuwe kwantumtool
Elektronen bijeengedreven met behulp van nieuwe kwantumtool De fontein van het leven:waterdruppels bevatten het geheime ingrediënt voor het opbouwen van leven
De fontein van het leven:waterdruppels bevatten het geheime ingrediënt voor het opbouwen van leven Uit welke stoffen bestaat aardolie?
Uit welke stoffen bestaat aardolie?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

