
Wetenschap
Eenvoudige eenstaps N-terminale modificatie van eiwitten
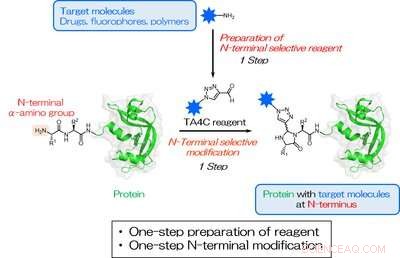
Fig. 1. Een eenstaps bereiding van TA4C en een eenstaps bioconjugatie gericht op een N-terminus a-aminogroep. De blauwe ster vertegenwoordigt een doelmolecuul voor N-terminale modificatie. Krediet:Universiteit van Osaka
Eiwitten worden veel gebruikt in de geneeskunde, biologie en scheikunde. Het verbeteren van hun inherente eigenschappen door functionele moleculen aan hun structuren toe te voegen, is een veel voorkomende en belangrijke stap op veel gebieden. Bijvoorbeeld, door fluorescerende moleculen toe te voegen, kunnen eiwitten worden opgespoord en gekwantificeerd. Er zijn veel modificatiestrategieën met verschillende voordelen beschreven. Onderzoekers van de Universiteit van Osaka rapporteren nu een eenvoudige N-terminus-specifieke wijziging die is uitgevoerd onder milde omstandigheden met behulp van nieuwe reagentia die in één stap zijn bereid. Hun bevindingen werden online gepubliceerd in ChemBioChem .
Het N-uiteinde wordt gedefinieerd als het begin van de eiwitketen waar de aminogroep van de eerste aminozuurbouwsteen beschikbaar is om te reageren. Specifiek richten op het N-uiteinde is nuttig omdat het zelden betrokken is bij de eiwitvouwing, waardoor het gemakkelijk toegankelijk is met een minimale impact op de eiwitfunctie. Het is bekend dat het een unieke en altijd aanwezige plaats is binnen elk eiwit.
Geïnspireerd door eerdere werken, de onderzoekers screenden een reeks cyclische stikstofbevattende verbindingen en ontdekten dat 1H-1, 2, 3-triazool-4-carbaldehyde (TA4C)-derivaten kunnen in een enkele stap worden geconjugeerd aan de N-terminus met relatief hoge conversies, tot 92%.
"Vereenvoudiging van eiwitmodificatie is een waardevolle ontwikkeling voor verschillende gebieden, "corresponderende auteur Akira Onoda legt uit. "Onze aanpak resulteert in zeer efficiënte plaatsspecifieke etikettering onder milde omstandigheden, wat belangrijk is bij het werken met gevoelige biologische moleculen. Zolang het toe te voegen molecuul een aminogroep bevat, een reactie kan worden uitgevoerd om de TA4C-groep in één stap te creëren, die vervolgens reactief is naar het eiwit N-uiteinde."
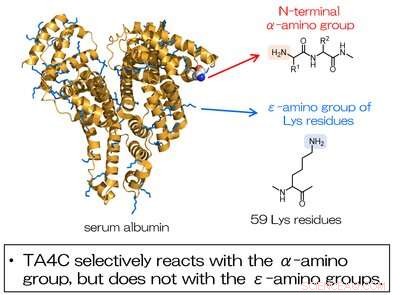
Fig. 2. De modificatie van serumalbumine met behulp van TA4C vindt selectief plaats bij de N-terminale a-aminogroep en niet bij de aminogroepen van Lys-residuen. Krediet:Universiteit van Osaka
De TA4C-reagentia worden in één stap bereid uit een functioneel molecuul met een aminogroep via een reactie die bekend staat als de Dimroth-omlegging. Een verscheidenheid aan amine-bevattende moleculen werd met succes gebruikt, inclusief polyethyleenglycol, biotine, en fluoresceïne, het brede scala aan mogelijke functionaliteiten demonstreert.
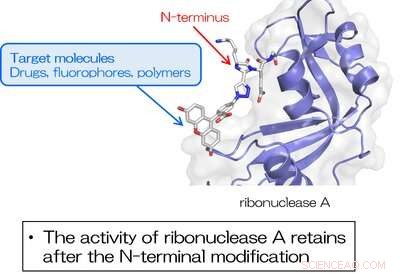
Fig. 3. RNase A gemodificeerd aan de N-terminus met behulp van TA4C behoudt de inherente enzymactiviteit. Krediet:Universiteit van Osaka
"Wij geloven dat onze aanpak als een enorm praktische optie zal bijdragen aan de toolbox voor eiwitmodificatie en de ontwikkeling zal versnellen op veel gebieden die afhankelijk zijn van eiwitconjugatie, " legt corresponderende auteur Takashi Hayashi uit. "Bovendien, door onze aanpak te combineren met technieken die zich richten op andere eiwitsites, kunnen meerdere functies worden geïntroduceerd, grote flexibiliteit bieden. Dit zal nuttig zijn in een breed scala van gebieden, waaronder bio-engineering, geneesmiddelen, en diagnostiek."
 NASA onderzoekt extra-tropische grote Lorenzos-regenval
NASA onderzoekt extra-tropische grote Lorenzos-regenval Een internationaal plasticverdrag kan een stille lente voor de zeeën voorkomen
Een internationaal plasticverdrag kan een stille lente voor de zeeën voorkomen Vermindering van luchtverontreinigende stoffen zou de opwarming van de aarde kunnen versterken zonder vermindering van broeikasgassen
Vermindering van luchtverontreinigende stoffen zou de opwarming van de aarde kunnen versterken zonder vermindering van broeikasgassen Opwarming van de aarde blijkt aanleiding te geven tot eerdere lentes die bijdragen aan drogere zomers
Opwarming van de aarde blijkt aanleiding te geven tot eerdere lentes die bijdragen aan drogere zomers Microplastics:geen klein probleem voor filtervoedende oceaanreuzen
Microplastics:geen klein probleem voor filtervoedende oceaanreuzen
Hoofdlijnen
- Dit is het seizoen om waakzaam te zijn:het risico op chocoladevergiftiging bij honden piekt met Kerstmis
- Waarom kunnen we de voetstappen van anderen horen,
- Het herprogrammeren van bacteriën in plaats van ze te doden kan het antwoord zijn op antibioticaresistentie
- 10, 000 jaar oud DNA bewijst wanneer vissen meren koloniseerden
- Monstervissen van de diepte
- Albatrospopulaties nemen af door visserij en veranderingen in het milieu
- Jacht op herten beperkt in westelijke Amerikaanse staten na strenge winter
- Glycosylering - onbekend terrein in kaart brengen
- Sommige lemuren zijn eenlingen, anderen hunkeren naar verbinding
- Daglichtschadebesparende tijd

- Belastingregel voor industrie beloont afvang van koolstof

- Het percentage per volume berekenen

- Multimodale beeldvorming toont aan dat spanning de chemie in een fotovoltaïsch materiaal kan stimuleren

- Trek uw eigen elektroden om de ontwikkeling van microdetectieapparatuur te versnellen

 Pennsylvania Spiders That Bite
Pennsylvania Spiders That Bite Opwarming van de aarde, El Nino kan nattere winters veroorzaken, drogere omstandigheden in andere maanden
Opwarming van de aarde, El Nino kan nattere winters veroorzaken, drogere omstandigheden in andere maanden Wetenschappers ontwikkelen minimaal invasieve hersensonde
Wetenschappers ontwikkelen minimaal invasieve hersensonde De effecten van aanbevelingssystemen in e-commerce verschillen per productkenmerken en beoordelingsbeoordelingen
De effecten van aanbevelingssystemen in e-commerce verschillen per productkenmerken en beoordelingsbeoordelingen Beeldvorming van lichtgolfvormen in luchtplasma
Beeldvorming van lichtgolfvormen in luchtplasma Vervuiling richt grote schade aan op het immuunsysteem van koralen
Vervuiling richt grote schade aan op het immuunsysteem van koralen Een nieuw tijdperk in de zoektocht naar donkere materie
Een nieuw tijdperk in de zoektocht naar donkere materie Bepalen wanneer India in botsing kwam met Azië om de Himalaya-bergen te vormen
Bepalen wanneer India in botsing kwam met Azië om de Himalaya-bergen te vormen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

