
Wetenschap
Aanvankelijke afstoting bij chemische binding sluit latere aantrekking niet uit
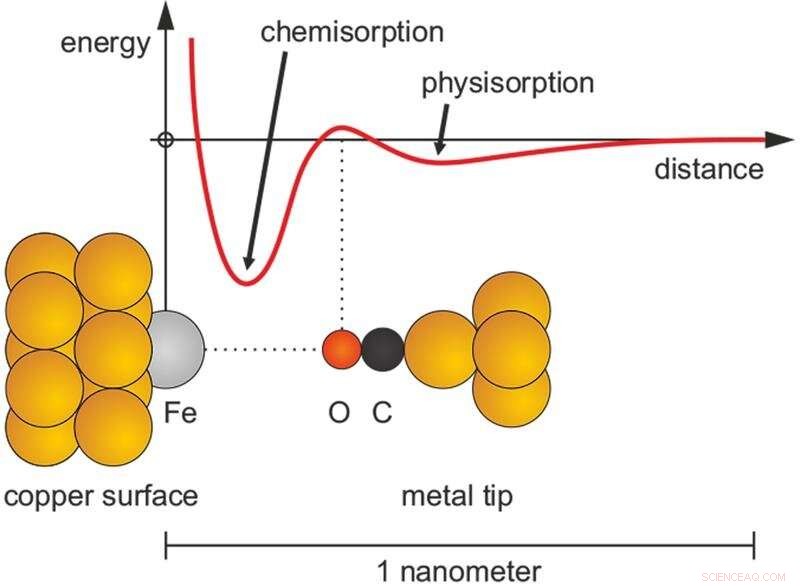
Overgang van een zwakke fysieke binding (fysisorptie) naar een sterke chemische binding (chemisorptie).
De filosoof Arthur Schopenhauer formuleerde een metafoor genaamd het stekelvarken dilemma, wat een bepaalde optimale afstand tussen mensen verklaart. Mensen voelen zich alleen op een te grote afstand en ongemakkelijk als ze te dichtbij zijn. Schopenhauer legde de ideale afstand uit aan de hand van de volgende gelijkenis:"Een aantal stekelvarkens kroop bij elkaar voor warmte op een koude dag in de winter; maar toen ze elkaar begonnen te prikken met hun stekels, ze waren verplicht zich te verspreiden. Echter, de kou dreef hen weer samen, toen precies hetzelfde gebeurde. Eindelijk, na vele bochten van ineengedoken en uiteenspatten, ze ontdekten dat ze het beste af waren door op een kleine afstand van elkaar te blijven. Op dezelfde manier, de behoefte van de samenleving drijft de menselijke stekelvarkens samen, alleen om wederzijds afgestoten te worden door de vele stekelige en onaangename eigenschappen van hun aard."
De Nobelprijswinnaar Richard Feynman rapporteerde een soortgelijk fenomeen voor atomen, de basisbouwstenen van materie. Zijn driedelige leerboek, De Feynman-lezingen over natuurkunde , begint met de veronderstelling dat in het geval van een catastrofale gebeurtenis die alle menselijke kennis uitholt, de volgende zin zou de meest bruikbare informatie over de natuur in de kortste vorm bevatten:" ...alle dingen zijn gemaakt van atomen - kleine deeltjes die in eeuwigdurende beweging rondbewegen, elkaar aantrekken als ze een beetje uit elkaar staan, maar afstotend wanneer ze in elkaar worden geperst."
Echter, de aard van de interactie van atomen en moleculen met oppervlakken is nog complexer, zoals de natuurkundige Lenard-Jones al in 1932 ontdekte. In sommige gevallen twee manieren van hechting kunnen optreden:een zwakke hechting, fysisorptie genoemd, en een sterke binding, chemisorptie genoemd. Fysisorptie zorgt ervoor dat stof aan oppervlakken blijft kleven of dat gekko's op muren en plafonds kunnen lopen zonder eraf te vallen. Chemisorptie is 10 tot 100 keer sterker dan fysisorptie. De wisselwerking tussen fysisorptie en chemisorptie is cruciaal voor het reinigen van uitlaatgassen in katalysatoren van auto's en in industriële reactoren die basischemicaliën bouwen door middel van katalytische reacties.
De twee wijzen van adsorptie worden uitgedrukt door een energiecurve die twee minima laat zien. Die energiecurven worden al tientallen jaren weergegeven in leerboeken over fysische chemie en oppervlaktewetenschap, hoewel experimentele toegang beperkt was tot de evenwichtspunten waar fysisorptie en chemisorptie plaatsvinden. Een groep experimentele natuurkundigen van de Universiteit van Regensburg, Ferdinand Huber, Julian Berwanger en Franz J. Giessibl, hebben experimenteel het ontstaan van de energiecurve vastgelegd die betrokken is bij de overgang van fysisorptie naar chemisorptie.
Ze bereikten dit door een CO-molecuul aan de punt van een atoomkrachtmicroscoop te bevestigen en het naar een enkel ijzeratoom te verplaatsen dat op een koperen oppervlak zit en de kracht registreerde die in het proces werkte. Het team omvatte kwantumchemici Svitlana Polyesa, Sergiy Mankovsky en Hubert Ebert van de Ludwig-Maximilians-Universiteit München, die de theoretische verklaring heeft uitgewerkt. Het overwinnen van de energetische barrière tussen fysisorptie en chemisorptie vereist een herschikking van de elektronen (hybridisatie) die de bindingen vormen, zoals is bevestigd in de kwantumchemische berekeningen.
Terugkomend op Schopenhauer en menselijke relaties, het is niet ongehoord dat mensen zich ook zeer aangetrokken kunnen voelen na het overwinnen van een mogelijke aanvankelijke afstoting.
 Een potje poolen in de live cell
Een potje poolen in de live cell Onderzoekers ontdekken dat traditionele waarnemingen van vloeistofstromen het grote geheel kunnen missen
Onderzoekers ontdekken dat traditionele waarnemingen van vloeistofstromen het grote geheel kunnen missen Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land
Wetenschappers gebruiken röntgenstralen om de geheimen van schalie te kraken, een hoeksteen van een van de snelst groeiende energiebronnen van het land Een bijgewerkt begrip van het synthetiseren van chemicaliën met toegevoegde waarde
Een bijgewerkt begrip van het synthetiseren van chemicaliën met toegevoegde waarde Sporen van opiaten gevonden in oud Cypriotisch schip
Sporen van opiaten gevonden in oud Cypriotisch schip
Hoofdlijnen
- What Is Crossing Over in Genetics?
- Luie valsspeler leeft onder de grond,
- Een eiwitduo zorgt ervoor dat de chromosomen in de voortplantingscellen hun significante andere vinden
- Het effect van zout en suiker op gedehydrateerde cellen
- Waarom is de trekduif uitgestorven?
- Onderzoek toont aan dat plantengroeiregulatoren gunstig kunnen zijn voor de vestiging van uien, productie
- Waarin verschillen mensen van onze voorouders?
- Mieren in het bladerdak van het Amazone-regenwoud hebben veel meer bacteriën in hun ingewanden dan grondbewoners
- COVID-19 heeft de manier waarop we rouwen veranderd
- Nieuwe milieuvriendelijke elektrochemische reactie kan bruikbare halfgeleidermaterialen synthetiseren

- Gecontroleerde faagtherapie kan zich richten op medicijnresistente bacteriën en tegelijkertijd mogelijke onbedoelde gevolgen omzeilen

- Onderzoekers krijgen inzicht in hoe enzymen specifieke reacties bereiken
- Wetenschappers vinden een manier om DNA-oppervlaktehybridisatie te versnellen

- Onderzoek naar spinnenlijm lost plakkerig probleem op

 Europa zet $ 1,18 miljard in om het leven in zee beter te beschermen
Europa zet $ 1,18 miljard in om het leven in zee beter te beschermen Prehistorisch reptiel zwanger van achtling
Prehistorisch reptiel zwanger van achtling Elektrisch textiel verlicht een lamp wanneer uitgerekt
Elektrisch textiel verlicht een lamp wanneer uitgerekt Elektromagnetische tovenarij:draadloze krachtoverdracht verbeterd door achterwaarts signaal
Elektromagnetische tovenarij:draadloze krachtoverdracht verbeterd door achterwaarts signaal Het effect van bevriezen en ontdooien op rots
Het effect van bevriezen en ontdooien op rots  Wat mobiele telefoons betekenen voor vluchtelingen
Wat mobiele telefoons betekenen voor vluchtelingen Vloeibare metalen de geheime ingrediënten om het milieu schoon te maken
Vloeibare metalen de geheime ingrediënten om het milieu schoon te maken Wat doen dieren als ze ziek worden?
Wat doen dieren als ze ziek worden?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

