
Wetenschap
Kanker gericht met herbruikbare brandnetelbehandeling
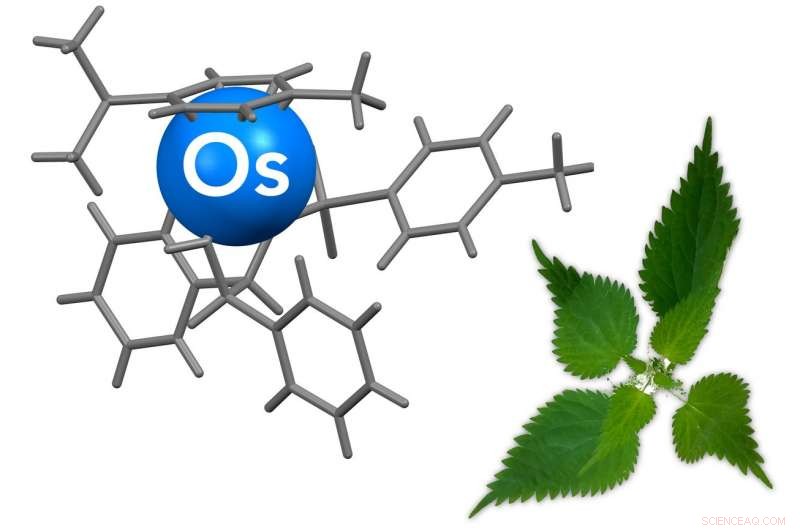
Vertegenwoordiging van de organische osmiumverbinding, die wordt geactiveerd met behulp van een niet-toxische dosis natriumformiaat, een natuurlijk product dat in veel organismen voorkomt, inclusief brandnetels en mieren. Krediet:Dr. James Coverdale/Universiteit van Warwick
Kankercellen kunnen effectiever en selectiever worden vernietigd met een unieke nieuwe herbruikbare behandeling, geactiveerd met een stof die voorkomt in brandnetels en mieren - dankzij nieuw onderzoek van de Universiteit van Warwick.
Onder leiding van professor Peter J. Sadler van Warwick's Department of Chemistry, onderzoekers hebben een nieuwe aanvalslijn tegen kanker ontwikkeld:een organische osmiumverbinding, die wordt geactiveerd met behulp van een niet-toxische dosis natriumformiaat, een natuurlijk product dat in veel organismen voorkomt, inclusief brandnetels en mieren.
Genoemd JPC11, het richt zich op een metabolisch proces waarop kankercellen vertrouwen om te overleven en zich te vermenigvuldigen. Het doet dit door een belangrijke stof die door kankercellen wordt gebruikt om de energie te leveren die ze nodig hebben voor snelle deling (pyruvaat) om te zetten in een onnatuurlijk lactaat, wat leidt tot de vernietiging van de cellen.
uniek, deze chemo-katalysatorbehandeling kan worden gerecycled en hergebruikt in een kankercel om deze herhaaldelijk aan te vallen.
Dit ongekende functionele vermogen om de verbinding in kankercellen te recyclen en opnieuw te gebruiken, zou ertoe kunnen leiden dat toekomstige geneesmiddelen tegen kanker in kleinere, effectiever, en mogelijk minder toxische doses, waardoor de bijwerkingen van chemotherapie afnemen.
De onderzoekers hebben zich gericht op het potentieel om deze verbinding te gebruiken bij eierstok- en prostaatkanker.
Eierstokkanker wordt in toenemende mate resistent tegen bestaande chemotherapiemedicijnen (zoals het platinamedicijn, cisplatine). Aangezien dit nieuwe onderzoek op een totaal nieuwe en unieke manier functioneert, het kan deze verworven resistentie overwinnen en het spectrum van antikankeractiviteit verbreden.
belangrijk, de ontwikkeling opent een mogelijkheid voor een meer selectieve kankerbehandeling, aangezien werd waargenomen dat JPC11 specifiek gericht was op de biochemie van kankercellen, gezonde cellen grotendeels onaangeroerd laten - een andere verbetering vergeleken met bestaande op platina gebaseerde medicijnen, die ook niet-kankercellen kunnen aanvallen.
Dr. James Coverdale, een Research Fellow van Warwick's Department of Chemistry, commentaar:
"Dit is een belangrijke stap in de strijd tegen kanker. Het manipuleren en toepassen van gevestigde chemie in een biologische context biedt een zeer selectieve strategie voor het doden van kankercellen.
"We hebben ontdekt dat chemokatalysator JPC11 een uniek werkingsmechanisme heeft - en we hopen dat dit zal leiden tot effectievere, selectieve en veiligere behandelingen in de toekomst."
Professor Peter Sadler, een medicinale chemicus aan de Universiteit van Warwick merkte op:
"Platinumverbindingen zijn de meest gebruikte medicijnen voor chemotherapie bij kanker. maar we moeten dringend reageren op de uitdagingen van het omzeilen van resistentie en bijwerkingen. Ons laboratorium is gericht op de ontdekking van werkelijk nieuwe geneesmiddelen tegen kanker die cellen op totaal nieuwe manieren kunnen doden. Chemo-katalysatoren, vooral die met immunogene eigenschappen, een doorbraak zou kunnen betekenen.
"Het zal tijd kosten om van het laboratorium naar de kliniek te gaan, maar we hebben het geluk een getalenteerde enthousiaste, internationaal team dat samenwerkt met collega's in het Warwick Cancer Research Center over de grenzen van de chemie heen, cel- en systeembiologie en kankergeneeskunde die vastbesloten zijn om te slagen."
Professor Martin Wills, katalysatorspecialist aan de Universiteit van Warwick, commentaar:
"Hoewel asymmetrische katalytische hydrogeneringsprocessen goed ontwikkeld zijn in de materiaalindustrie, dit onderzoek levert het eerste voorbeeld ooit op dat dit in cellen wordt bereikt met behulp van een synthetische katalysator."
Handigheid (moleculaire asymmetrie) is van cruciaal belang voor de functie van biomoleculen in het lichaam. eiwitten, enzymen en ons DNA, bijvoorbeeld - worden overhandigd. Alleen de juiste hand werkt, op dezelfde manier dat een rechterhand niet past in een linkerhandschoen.
In dit geval, de osmiumverbinding JPC11, met natriumformiaat, kan selectief een molecuul met een specifieke 'handigheid' produceren - en zo manipuleren hoe kankercellen groeien.
Dr. Coverdale legde uit:
"De 'handigheid' van moleculen is van cruciaal belang in het lichaam. Onze handen zijn bijna identiek, maar zijn spiegelbeelden van elkaar. Hetzelfde kan gelden voor moleculen, en in sommige gevallen, het hebben van de verkeerde molecuul kan ingrijpende biologische gevolgen hebben. Wij geloven dat manipulatie van de 'handigheid' van moleculen in cellen een nieuwe strategie zou kunnen bieden voor het bestrijden van ziekten."
 Drones gebruikt om aswolken van vulkaan Guatemalteeks te analyseren
Drones gebruikt om aswolken van vulkaan Guatemalteeks te analyseren Onderzoekers vinden sommige bossen cruciaal voor het tegengaan van klimaatverandering, biodiversiteit
Onderzoekers vinden sommige bossen cruciaal voor het tegengaan van klimaatverandering, biodiversiteit Sub maakt snelle stijging in Indische Oceaan; bemanning veilig
Sub maakt snelle stijging in Indische Oceaan; bemanning veilig NASA's Aqua Satellite vindt een groot haveloos oog in tyfoon Krosa
NASA's Aqua Satellite vindt een groot haveloos oog in tyfoon Krosa Wat is een inktvissenrol in het ecosysteem?
Wat is een inktvissenrol in het ecosysteem?
Hoofdlijnen
- Studie:Grote witte haaien zwemmen steeds dieper
- Welke is eencellig: Prokaryoten of eukaryoten?
- Wat zijn genetisch gemodificeerde organismen (GGO's)? Zijn ze veilig?
- Functies van menselijke organen
- Wat zijn drie primaire doelen van mitose?
- De nadelen van gelelektroforese
- Retrovirus versus DNA-virus
- Studie biedt gedetailleerd inzicht in het vroege leven van grijze zeehondenpups op zee
- Afbraak in het Noordpoolgebied
- Een nieuwe generatie kunstmatige netvliezen op basis van 2D-materialen

- Onderzoekers kraken mengsels van oplosmiddelen puzzel
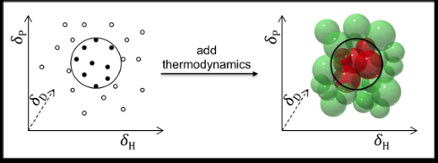
- Tweefasig materiaal met verrassende eigenschappen

- Veelgebruikte medicijnbron voor inzichten in de vorming van vlinderkristallen
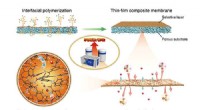
- Wetenschappers maken doorbraak in ionengeleidende composietmembranen
 Waarom goud-palladiumlegeringen beter zijn dan palladium voor waterstofopslag
Waarom goud-palladiumlegeringen beter zijn dan palladium voor waterstofopslag Een supergeleider van het Kagome-rooster onthult een cascade van kwantumelektrontoestanden
Een supergeleider van het Kagome-rooster onthult een cascade van kwantumelektrontoestanden 2D-spintronica heeft computergebruik al getransformeerd - nu maakten ze het in drie dimensies werkend
2D-spintronica heeft computergebruik al getransformeerd - nu maakten ze het in drie dimensies werkend Nanobuisjes organiseren zichzelf en wiebelen:evolutie van een niet-evenwichtssysteem toont maximale entropieproductie
Nanobuisjes organiseren zichzelf en wiebelen:evolutie van een niet-evenwichtssysteem toont maximale entropieproductie kroniek van de complexe ecologische veranderingen veroorzaakt door de steeds vluchtigere El Niño – La Niña-cycli
kroniek van de complexe ecologische veranderingen veroorzaakt door de steeds vluchtigere El Niño – La Niña-cycli Alles wat u moet weten over de wereldwijde watercrisis
Alles wat u moet weten over de wereldwijde watercrisis Studie:Leningvervangende beurzen verhogen het slagingspercentage van studenten met een laag inkomen
Studie:Leningvervangende beurzen verhogen het slagingspercentage van studenten met een laag inkomen Kwaliteit van verkopers cruciaal voor groei, inkomsten voor online platforms
Kwaliteit van verkopers cruciaal voor groei, inkomsten voor online platforms
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

