Wetenschap
Radicale methoden voor geïnfecteerde implantaten
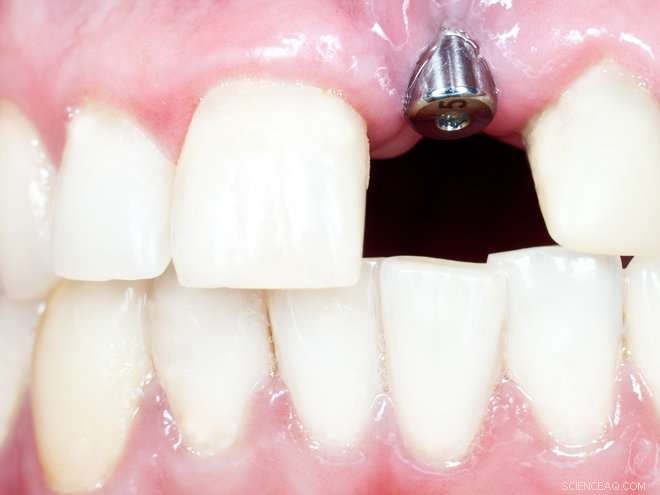
Tandimplantaten komen in Noorwegen steeds vaker voor als vervanging voor tanden. De vervanging komt niet altijd zonder problemen, echter. Krediet:Colourbox.com
Moleculen die vaker bekend staan om hun potentieel om kanker te veroorzaken, kunnen een nieuwe, gezondheidsbevorderende rol. Wetenschappers ontdekken nu hoe deze "radicalen" kunnen worden gebruikt om infecties te voorkomen en het succes van tandheelkundige implantaten op de lange termijn te bevorderen.
Hoewel tandartsen aanbevelen dat we onze eigen tanden zo lang mogelijk behouden, steeds meer van ons zullen uiteindelijk een of meer tanden moeten vervangen door titanium implantaten. Dit geldt vooral voor de oudere generaties.
Echter, tandheelkundige implantaten blijken vaak slechts een gedeeltelijk succesvolle vervanging te zijn. Bacteriën kunnen het gebied rond een implantaat koloniseren. Bacteriële infecties rond een implantaat kunnen uiteindelijk leiden tot verlies van het bot dat het implantaat ondersteunt, waardoor de patiënt een grote behoefte heeft aan uitgebreide behandeling en als gevolg daarvan een algehele slechtere mondgezondheid.
Als het bot rond een implantaat geïnfecteerd raakt, er een ernstig risico bestaat dat de patiënt een uitgebreide restauratieve tandheelkundige behandeling en onderhoud nodig heeft om de functie van het implantaat te behouden en het verloren bot te herstellen, als het überhaupt mogelijk is. Bijgevolg, onderzoek naar biomaterialen die kunnen worden gebruikt om de hergroei van verloren bot te vergroten en te begeleiden, is een toonaangevend gebied van tandheelkundig onderzoek geworden.
Biofilms op implantaten
Om een tandheelkundig implantaat te laten functioneren, het moet stevig aan het kaakbeen worden bevestigd. Dit betekent dat de botcellen de bacteriën moeten verslaan in de zogenaamde "race om het oppervlak" van het implantaat. Door de race te winnen, de botcellen zullen nieuw botweefsel vormen rond het implantaat, het implantaat in het bot vastmaken.
Echter, het zijn vaak de bacteriën die de race winnen. Ze vormen een biofilm, een dunne laag bacteriën op het implantaatoppervlak. – Biofilm is een slimme manier voor bacteriën om oppervlakken te koloniseren; het maakt de bacteriën sterker, legt David Wiedmer uit, een research fellow aan de Faculteit der Tandheelkunde van de Universiteit van Oslo. Als de bacteriën de overhand krijgen op het implantaatoppervlak, het implantaat is vatbaar voor infectie, met mogelijk ernstige gevolgen voor de gezondheid van de patiënt.
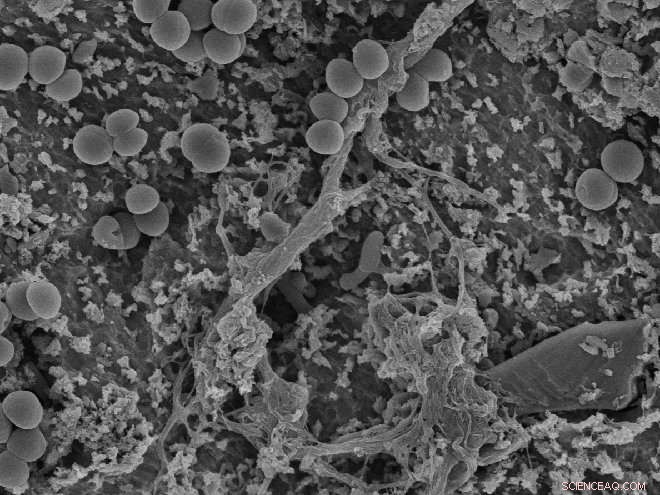
De bacteriën wonnen de race om het oppervlak te veroveren:de ronde "stippen" zijn bacteriën die zich aan een implantaatoppervlak hebben gehecht. De proeven van Wiedmer toonden aan dat de radicale moleculen kunnen bijdragen aan het verstoren van de bacteriën en een antibacterieel effect kunnen veroorzaken. Krediet:OD, UiO/David Wiedmer
Geïnfecteerde implantaten worden meestal behandeld met antibiotica. – Als bacteriën een biofilm vormen, antibiotica werken vaak niet omdat bacteriën binnen een biofilm worden beschermd. In het licht van de dramatische toename van antibioticaresistente bacteriën, er is dringend behoefte aan alternatieve behandelingen, zegt Wiedmer, die van oorsprong werktuigbouwkundig ingenieur is. Hij begon te kijken naar vrije radicalen als alternatief. Deze onstabiele moleculen kunnen stress veroorzaken bij bacteriën, die op hun beurt een antibacterieel effect kunnen creëren.
Zeer reactieve radicale moleculen
Vrije radicalen zijn onstabiele moleculen omdat ze een ongepaard elektron hebben. Dus, ze zijn altijd op zoek naar een ander elektron om mee te paren. Van vrije radicalen is bekend dat ze schadelijke en pathogene moleculen zijn die veranderingen in het DNA kunnen veroorzaken, die op hun beurt mutaties kunnen veroorzaken die tot kanker kunnen leiden. Wiedmer's hypothese was dat de reactiviteit van vrije radicalen ook gebruikt zou kunnen worden om bacteriën te doden.
Hij baseerde zijn idee op een bekend chemisch proces, fotokatalyse:wanneer titaandioxide (TiO2) wordt blootgesteld aan ultraviolet licht, zoals gevonden in zonlicht, in aanwezigheid van zuurstof, het oppervlak reinigt zichzelf van organisch vuil, door het af te breken in water en zuurstof. Dit reinigingsproces is gebaseerd op de vorming van vrije radicalen en het is dezelfde reactie die in zonnecellen wordt gebruikt om energie te produceren.
Tandimplantaten hebben ook TiO2 op hun oppervlak. Bijna alle tandheelkundige implantaten zijn gemaakt van titanium, en TiO2 ontstaat wanneer titanium in contact komt met zuurstof uit de lucht of het bloed, bijv. wanneer een implantaat in de mond wordt ingebracht.
Donkere katalyse voor behandeling en preventie
Echter, het is moeilijk om fotokatalytische reacties op implantaten teweeg te brengen. Dit komt door het voor de hand liggende probleem van het toevoegen van het nodige zonlicht aan de reactie tussen de TiO2 op het implantaatoppervlak en de zuurstof in het bloed wanneer het implantaat al in het bot van uw kaak is ingebracht.

Door te onderzoeken hoe snel de chemische oplossing zijn blauwe kleur verloor, Promovendus David Wiedmer kon detecteren welke soorten titaandioxide (TiO2) ertoe bijdroegen dat de bacteriën geen biofilm op de implantaten zouden vestigen. Krediet:OD, UiO/Margit Selsjord
Om deze reden, Wiedmer heeft onderzoek gedaan naar de behandeling van bacteriële infecties op implantaten met behulp van een methode die hij 'donkere katalyse' noemt. Door TiO en waterstofperoxide (H2O2) te combineren, in plaats van water en zonlicht, hij bereikt een soortgelijk effect als fotokatalyse. Wanneer H2O2 wordt toegevoegd aan een implantaat dat is bedekt met een laag TiO2, Er komen ook vrije radicalen vrij, maar deze keer in het donker.
Gezien de sterke antibacteriële eigenschappen van de geproduceerde vrije radicalen, Wiedmer onderzocht donkere katalyse op TiO2 in twee verschillende biomedische toepassingen. De eerste geteste toepassing was om een bestaande infectie rond een implantaat te behandelen. Zijn onderzoek ging ook na of de methode een preventief effect zou kunnen hebben op "steigers", poreuze raamwerken die in het kaakbot kunnen worden ingebracht om botcellen te ondersteunen en te begeleiden om te groeien en "nieuw" bot te vormen.
Veelbelovend, maar moeilijk te implementeren
Wiedmer heeft reden om optimistisch te zijn dat het ooit mogelijk zal zijn om bacteriële infecties rond tandheelkundige implantaten onder controle te krijgen en gemakkelijker te voorkomen. Zijn studies toonden aan dat donkere katalyse een veelbelovende methode is om infecties te behandelen, omdat het radicalen creëert die bacteriën helpen bestrijden.
Het onderzoek gaf ook aan dat donkere katalyse verder zou kunnen worden ontwikkeld en toegepast op botsteigers. Deze steigers ondersteunen de regeneratie van verloren botweefsel waarin vervolgens implantaten kunnen worden ingebracht. In zijn studie, Wiedmer ontdekte dat radicalen gevormd door donkere katalyse kunnen voorkomen dat bacteriën het oppervlak van poreuze TiO2-steigers koloniseren.
"Het preventieve effect is eigenlijk belangrijker dan het gebruik ervan bij de behandeling van reeds bestaande infecties. implantaten die problemen veroorzaken door infecties kunnen, als laatste redmiddel, worden geëxtraheerd. Maar je kunt een poreuze steiger niet gemakkelijk verwijderen als er al bot in de poriën van de steiger is gegroeid, " hij legt uit.
Echter, er moet nog veel onderzoek worden gedaan voordat donkere katalyse kan worden toegepast in tandartspraktijken. Wiedmer kon niet sluitend uitsluiten dat de radicalen ook het cellulaire DNA zouden beschadigen tijdens de bestrijding van de bacteriën. – (EN) Ik hoop dat deze nieuwe strategie om vrije radicalen te gebruiken om bacteriën te doden, ons kan helpen bij het vinden van alternatieve behandelingen voor antibiotica. Hoewel er nog een weg te gaan is, inclusief klinische proeven, dit project zou uiteindelijk wat meer licht in het donker kunnen werpen, zegt Wiedmer met een grijns.
 Zonnewaterstof:Laten we eens kijken naar de stabiliteit van foto-elektroden
Zonnewaterstof:Laten we eens kijken naar de stabiliteit van foto-elektroden Tips voor roest en spuitwerk Smeedijzeren gazebo
Tips voor roest en spuitwerk Smeedijzeren gazebo Krachtigste en mildste reagentia verkregen op basis van milieuvriendelijk jodium
Krachtigste en mildste reagentia verkregen op basis van milieuvriendelijk jodium Parodontitis:onderzoekers zoeken naar een nieuwe werkzame stof
Parodontitis:onderzoekers zoeken naar een nieuwe werkzame stof Moleculaire motoren:Chemische carrousel draait in de kou
Moleculaire motoren:Chemische carrousel draait in de kou
 Verschillende soorten waterlichamen
Verschillende soorten waterlichamen  35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel
35% van de microplastics die in de wereldzeeën terechtkomen, is afkomstig van synthetisch textiel Hoe wordt warmte overgedragen van de zon naar de aarde?
Hoe wordt warmte overgedragen van de zon naar de aarde?  Hoe Morel-paddestoelen te jagen in Indiana
Hoe Morel-paddestoelen te jagen in Indiana Sommige droogteperiodes tijdens de Indiase moesson zijn te wijten aan unieke verstoringen in de Noord-Atlantische Oceaan
Sommige droogteperiodes tijdens de Indiase moesson zijn te wijten aan unieke verstoringen in de Noord-Atlantische Oceaan
Hoofdlijnen
- Welk proces voeren Ribosomes uit?
- Hoe maak je een DNA-model met ijslollystokjes
- Hoe een DNA-monster wordt verzameld en voorbereid voor onderzoek
- Lijst met celorganellen en hun functies
- Wat zijn de stadia van cytokinese?
- Onderzoekers brengen druggable genomische doelwitten in kaart in evoluerende malariaparasieten
- Onderzoeker rapporteert belangrijke componenten van antivirale verdediging van honingbijen
- Wetenschapper duikt in honderden onderwatergrotten op zoek naar nieuwe vormen van leven
- Baby bongo geboren, waarschijnlijk binnenkort in Species Survival Center
 Wat is het Higgs-deeltje precies?
Wat is het Higgs-deeltje precies?  IBM zegt dat het een mijlpaal is in kwantumcomputing
IBM zegt dat het een mijlpaal is in kwantumcomputing Engineering van de Mississippi-rivier heeft koolstof uit de atmosfeer gehouden, zegt nieuwe studie
Engineering van de Mississippi-rivier heeft koolstof uit de atmosfeer gehouden, zegt nieuwe studie Studie:studenten met een lagere sociaaleconomische achtergrond hebben hogere cijfers nodig om naar de beste Britse rechtsscholen te gaan
Studie:studenten met een lagere sociaaleconomische achtergrond hebben hogere cijfers nodig om naar de beste Britse rechtsscholen te gaan Geen demontage vereist:niet-destructieve methode om de levensduur van dragers in SiC . te meten
Geen demontage vereist:niet-destructieve methode om de levensduur van dragers in SiC . te meten NASA-hoofd:oorzaak gat in ruimtestation wordt bepaald
NASA-hoofd:oorzaak gat in ruimtestation wordt bepaald Wat betekent neutralisatie?
Wat betekent neutralisatie?  Laura's restjes gaan naar het oosten, een ramp achterlatend in Louisiana
Laura's restjes gaan naar het oosten, een ramp achterlatend in Louisiana
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com