
Wetenschap
Onderzoekers ontwikkelen een klein antilichaam dat het coronavirus kan neutraliseren
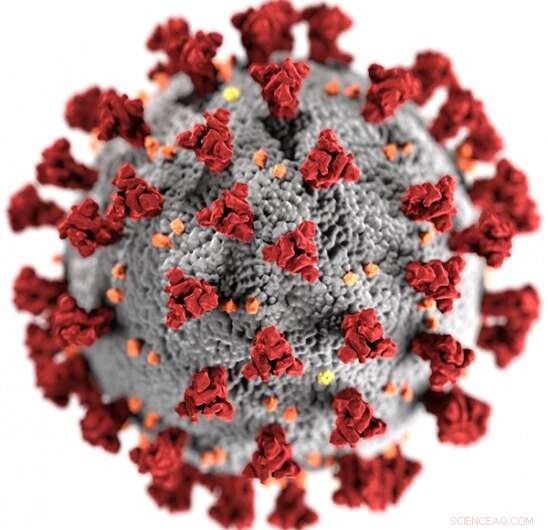
Afbeelding van de ultrastructurele morfologie tentoongesteld door het nieuwe coronavirus 2019 (2019-nCoV). Krediet:CDC
Om 2 uur 's nachts afgelopen april, Michael Schoof heeft de cijfers op zijn scherm drie keer gecontroleerd, haalde diep adem, en vuurde een e-mail af die hij de hele dag had gewacht om te verzenden.
"Ik denk dat het werkt", was de voorzichtige bewoording van zijn bericht.
Schoof, een afgestudeerde student in het lab van Peter Walter, doctoraat, een gerenommeerd wetenschapper gespecialiseerd in eiwitsortering en celmembranen, maakte deel uit van een klein team op een quixotische missie:om SARS-CoV-2 te immobiliseren, het nieuwe coronavirus dat COVID veroorzaakt, door gebruik te maken van een synthetische versie van kleine antilichamen die oorspronkelijk zijn ontdekt in lama's en kamelen. Deze "nanolichamen, "zoals ze bekend staan, was afkomstig van het UC San Francisco-lab van Aashish Manglik, MD, doctoraat, een opkomende eiwitwetenschapper die de afgelopen drie jaar een enorme bibliotheek van nanobodies had opgebouwd en nieuwe manieren had ontwikkeld om hun ongebruikelijke eigenschappen te benutten.
Tijdens de vorige maand, Schoof had het grootste deel van zijn wakkere uren doorgebracht in het verder lege laboratoriumcomplex op de Mission Bay-campus van UCSF. Het was het hoogtepunt van de COVID-piek in de lente van 2020, en alleen essentieel gezondheidspersoneel en degenen die aan wetenschap in verband met de pandemie werkten, werden toegelaten tot de faciliteiten van de universiteit. Schoof had zijn kamergenoot gesleept, een medestudent genaamd Reuben Saunders, om met hem aan het project te werken. Bestaan op gestoomde dumplings en liters thee, ze hadden de 2 miljard nanobodies in de bibliotheek van Manglik doorzocht in de hoop een molecuul te identificeren dat in staat is om het dodelijke SARS-CoV-2 te bereiken en het te immobiliseren. Nutsvoorzieningen, Tenslotte, Schoof was ervan overtuigd dat ze hun eerste grote doorbraak hadden bereikt.
De eerste stap bij een virale infectie is een cellulaire kaping. Om controle te krijgen over een menselijke cel, SARS-CoV-2 vergrendelt de grijphaakachtige spikes op zijn eigen buitenkant aan eiwitten die ACE2-receptoren worden genoemd aan de buitenkant van een doelcel. Maar wat als, vroegen de onderzoekers zich af, ze de kaper konden blokkeren door de grijphaken iets anders te geven om aan vast te klikken?
Die dag, Schoof was begonnen met het uitvoeren van tests op honderden kolonies gist, elk ontworpen om bepaalde nanobodies uit de bibliotheek van Manglik te produceren. Al deze specifieke nanobodies hadden aangetoond dat ze in staat waren zich vast te klampen aan de pieken van SARS-CoV-2. Nu was het tijd om de belangrijkste vragen te stellen:hoe stevig waren deze nanobodies aan de spikes gebonden? Waren ze in staat om te concurreren met de ACE2-receptoren?
Er achter komen, Schoof had zijn nanobody tot expressie brengende gistcellen gemengd met fluorescerende SARS-CoV-2-spikes. Toen hij naar de resultaten van de eerste twee platen keek, hij voelde een golf van opwinding, die hij snel temperde met de wetenschappelijke scepsis die hij had geleerd te cultiveren. Sommige nanobodies plakten aan de SARS-CoV-2-pieken, maar konden nog steeds opzij worden geschoven door een overmaat aan menselijke ACE2-receptoren:duidelijk bewijs van een potentiële neutralisator.
"Dat, " herinnert hij zich, "is toen we wisten dat we iets hadden."
In de dagen die volgden op Schoofs omzichtige nachtelijke e-mail, Walter en Manglik maakten gebruik van hun respectievelijke netwerken van wetenschappelijke contacten, versterkingen oproepen van laboratoria over de hele campus en zelfs ver weg als Parijs om te helpen bij de volgende fase van hun zoektocht. Spoedig, het kleine team was veranderd in een waar leger van interdisciplinaire onderzoekers en afgestudeerde studenten. In november, zij publiceerden hun resultaten in het prestigieuze tijdschrift Science. In de krant, bijna 60 co-auteurs beschreven een gewaagde, innovatieve COVID-tegenmaatregel, voorstellen dat hun nanobodies op een goedkope, gemakkelijk te vervoeren neusspray die SARS-CoV-2 kan neutraliseren. Onder henzelf, ze noemden de moleculen AeroNabs.
Vanaf dat moment, het UCSF-team is op zoek naar een industriële partner die bereid is het kostbare en rigoureuze klinische proefproces te financieren, maar momenteel zijn farmaceutische bedrijven gericht op de ontwikkeling van vaccins voor preventie en meer traditionele antilichamen voor behandeling.
Maar de nanobody-aanpak is veelbelovend. Door de eenvoudige structuur van nanobodies, AeroNabs kunnen veel goedkoper en sneller in massaproductie zijn, veel gemakkelijker te vervoeren, en veel gemakkelijker op te slaan dan de traditionele antilichamen die momenteel in gebruik en in ontwikkeling zijn.
"Dit is iets dat je zou kunnen nemen na een positieve test die je virale lading onmiddellijk zou kunnen verminderen, ", zegt Walter. "Dus je kansen om een ernstige ziekte te ontwikkelen zouden door deze behandeling worden verminderd."
Hij merkt ook op dat massale vaccinatie tijd zal vergen, en dat niet iedereen in de bevolking kan of zal worden gevaccineerd, waardoor passieve bescherming nog steeds ongelooflijk waardevol is. "En, " hij voegt toe, "We weten niet hoe breed het vaccin beschikbaar zal zijn buiten de rijkste landen ter wereld."
Dynamisch duo
De zaden van het AeroNabs-project werden in 2017 geplant, toen Walter Manglik een lezing over zijn werk hoorde houden.
Op het eerste gezicht, de twee wetenschappers lijken een vreemd stel te zijn. Met zijn volle bos donker haar, jongensachtige glimlach, en gladgeschoren kin, Manglik kan worden aangezien voor een afgestudeerde student. In feite, hij is een rijzende ster in zijn vakgebied die in 2013 maakte Wetenschappelijke Amerikaan '30 onder de 30' lijst. Geboren in Indië, Manglik bracht zijn eerste acht jaar door in Saoedi-Arabië voordat zijn familie naar Des Moines emigreerde. Iowa, waar hij de wetenschap ontdekte op de universiteit. De 60-jarige Walter, anderzijds, heeft een volle witte baard en snor en een bril met kleine lenzen. Hij is geboren en opgegroeid in Duitsland, kwam naar de VS voor zijn afstudeerwerk, en heeft een legendarische carrière in kaart gebracht. Zijn vele onderscheidingen zijn onder meer de prestigieuze Lasker Award, vaak gezien als een voorloper van een Nobelprijs. Maar ondanks hun verschillen, Walter en Manglik delen een diepe passie voor moleculaire biologie en haar eindeloos flexibele organische bouwstenen:eiwitten.
Mangliks toespraak die dag ging over zijn poging om een van 's werelds grootste bibliotheken van nanobodies samen te stellen - een veelbelovende, relatief nieuw type antilichaam afgeleid van het bloed van lama's, kamelen, en andere dieren in de kameelachtige familie. Hij had voor het eerst over nanobodies geleerd op de graduate school aan Stanford, nadat hij verliefd was geworden op de studie van receptoren, een brede familie van eiwitten die betrokken zijn bij intercellulaire signalering. Receptoren steken uit cellen zoals antennes, elk reageert op een specifiek chemisch signaal. Tijdens het bestuderen van menselijke adrenaline-receptoren, Manglik maakte uitgebreid gebruik van nanobodies, die, dankzij hun kleine formaat, kan veel nauwkeuriger met receptoren interageren dan de op maat gemaakte antilichamen die hij gebruikte om receptoreigenschappen te onderzoeken. Zijn experimenten onthulden hoe verschillende geometrische configuraties van receptoren hun signaalgedrag beïnvloeden.
"Eiwitten zijn niet alleen simpele lego's die in elkaar passen - ze zijn als lego's gemaakt van jello of stopverf, " legt Manglik uit. "Ze zijn constant in beweging. In feite, het is de beweging van een eiwit, het blijkt, dat maakt echt uit voor hoe het werkt. En nanobodies kunnen ons helpen die beweging te beheersen."
Nanobodies:een zegen voor de wetenschap
Nanobodies werden eind jaren tachtig ontdekt door een paar studenten aan de Vrije Universiteit van Brussel, nadat ze hun biologieprofessor op beroemde wijze benaderden, een immunoloog genaamd Raymond Hamers, klagen over een opdracht. De geschiedenis heeft de reden voor hun klacht verduisterd; volgens een veel geciteerd verslag waren de studenten bang dat de opdracht, waarvoor ze de antilichamen in menselijk bloed moesten analyseren, ze kunnen besmetten met een ziekte. Een andere versie zegt dat de studenten het experiment saai vonden en hun professor vroegen om hen iets originelers toe te wijzen.
Wat de waarheid ook is, niemand betwist wat er daarna gebeurde. Snuffelen in een laboratoriumkoelkast, Hamers vond een flesje bevroren kamelenserum van dromedarissen dat besmet was met parasieten waarvan gedacht werd dat ze Afrikaanse slaapziekte veroorzaken. Hij gaf het aan de studenten en stelde voor dat ze de antilichamen in het kamelenbloed isoleren om te zien hoe ze eruit zagen. Toen de studenten het bloed zuiverden, ze ontdekten iets verbazingwekkends.
Naast de standaard antilichamen die in alle gewervelde dieren worden aangetroffen, de gezuiverde monsters bevatten een afgeleid antilichaam dat nog nooit eerder in de wetenschap is gezien - kleiner, eenvoudiger eiwitten, die de studenten aanvankelijk aanzagen voor fragmenten van conventionele antistoffen. Nader onderzoek onthulde dat ze een geheel nieuwe klasse van immuunstoffen waren, zonder een van de eiwitketens die in alle andere eerder bestudeerde antilichamen worden gevonden.
De ontdekking leidde tot een baanbrekend artikel uit 1993 in het prestigieuze tijdschrift Natuur . Hamers en zijn studenten noemden de nieuwe kleine eiwitten nanobodies. Gelijkaardige enkelketenige antilichamen werden later geïdentificeerd in lama's, alpaca's, guanacos (een ander Zuid-Amerikaans zoogdier met lange nek), en zelfs haaien.
Al snel werd duidelijk dat nanobodies niet alleen immunologisch bruikbaar waren, maar dat ze door hun kleine formaat nuttige experimentele hulpmiddelen waren - zoals Manglik en zijn UCSF-collega's ruimschoots kunnen bevestigen.
Bestuderen hoe deze gelatineuze bouwstenen op moleculair niveau bewegen, snap en los, en interactie werd Manglik's focus toen hij toetrad tot de UCSF-faculteit. Hij wist al vroeg dat nanobodies een groot deel van zijn werk zouden uitmaken. Hoewel er antilichamen en nanobodies bestaan om dieren te helpen infecties te bestrijden, Manglik ziet ze ook als een eindeloos kneedbaar hulpmiddel dat kan worden gebruikt om een breed scala aan processen in het menselijk lichaam te hacken en om wetenschappelijke basismysteries te ontcijferen. Maar nanobodies waren tijdrovend om te maken en vereisten toegang tot kameelachtigen. Als afgestudeerde student, Manglik had vertrouwd op een medewerker in België die een receptoreiwit van belang zou injecteren in een lama, oogst vervolgens de nanobodies uit het bloed van het dier. Het hele proces vergde maanden van zeer gespecialiseerd werk, waartoe slechts enkele groepen in staat waren.
Om de toegang tot nanobodies voor onderzoekers overal te democratiseren, Manglik werkte samen met Andrew Kruse, doctoraat, een goede vriend van de middelbare school die lid was geworden van de faculteit van de Harvard Medical School. Samen, de twee laboratoria creëerden biljoenen unieke nanobody-coderende DNA-sequenties, elk geïnspireerd op de nanobodies die normaal in lama's worden aangetroffen. De DNA-sequenties voor deze nanobodies zijn ondergebracht in een enorme pool van miljarden kleine gistcellen, die elk kunnen worden overgehaald om een kopie van een individueel nanobody op het oppervlak ervan te plaatsen. De noodzaak van een levende lama volledig omzeilend, zo'n bibliotheek geeft onderzoekers toegang tot gistcellen die nanobodies herbergen die specifiek zijn voor een bepaalde taak. Manglik en Kruse hebben hun bibliotheken openlijk gedeeld met honderden laboratoria over de hele wereld.
"Het idee is dat bij een dier, er zijn biljoenen verschillende nanobodies om te vechten tegen alles wat het kan tegenkomen, " zegt hij. "We wilden een bibliotheek maken die voor miljarden individuele nanobodies codeerde. Deze bibliotheek zou een geweldig startpunt zijn voor het vinden van een nanobody tegen eigenlijk alles - allemaal in het laboratorium en zonder de noodzaak om een dier te injecteren."
Nadat ik Manglik dit alles had horen uitleggen, Walter stuurde zijn afgestudeerde student Michael Schoof naar het lab van Manglik. Schoof probeerde het gedrag van een eiwit gerelateerd aan traumatisch hersenletsel te moduleren, en Walter vermoedde dat de nanobodies van Manglik daarbij nuttig zouden kunnen zijn.
Toen sloeg het coronavirus toe, de wereld stopte, en bijna alle niet-COVID-gerelateerde activiteiten op de universiteit zijn stilgelegd.
"Dus op dat moment we zeiden, "We zullen, we kunnen nu thuis zitten, of we kunnen bedenken hoe we echt kunnen helpen bij dit streven naar een oplossing, ', herinnert Walter zich.
Binnen een paar dagen, Walter en Schoof hadden e-mailcontact met Manglik. Ze kenden de ziektebestrijdende eigenschappen van nanobodies. Een nanobody-technologie had onlangs de FDA-goedkeuring gekregen voor de behandeling van een bloedstollingsstoornis, en nog een, gebruikt voor de behandeling van een respiratoir virus, klinische proeven in een laat stadium hadden bereikt.
Was het mogelijk dat ze er een konden bouwen om het coronavirus te bestrijden?
Een geweldig resultaat
Vanaf het begin, het team wist het succes van het project zou berusten op hun vermogen om een nanobody te vinden met voldoende bindingsaffiniteit – het vermogen om zich te hechten aan de pieken van het coronavirus en deze te keuren.
Eiwitten hebben specifieke vormen. Hoe goed twee eiwitten bij elkaar passen, bepaalt hun bindingsaffiniteit. Walter en Manglik wisten dat de bindingsaffiniteit die ervoor zorgt dat SARS-CoV-2 zich aan ACE2-eiwitten hecht, in theorie zou kunnen worden overmeesterd door een nanobody die precies op de juiste manier is gevormd.
Manglik had al een belangrijk ingrediënt voor zo'n experiment. Onderzoekers van de Universiteit van Texas (UT) in Austin hadden onlangs de unieke structuur van de SARS-CoV-2-pieken onthuld waardoor het virus zich kon binden aan de ACE2-receptoren van menselijke cellen. Manglik stak zijn hand uit naar Jason McLellan van de UT, doctoraat, die ermee instemden hem hun 'constructie' te sturen - een stukje DNA dat codeert voor de spikes en dat in een andere cel kan worden ingebracht, uitgedrukt in grote hoeveelheden, gezuiverd, en gebruikt voor experimenten.
Het team begon de 2 miljard nanobodies in de bibliotheek te screenen om te zien of ze verbindingen konden vinden met de juiste bindingsaffiniteit voor de SARS-CoV-2-pieken. Binnen drie weken, ze hadden 800 potentiële kandidaten geïdentificeerd, en een week later schreef Schoof zijn voorzichtige nachtelijke e-mail waarin hij Manglik en Walter informeerde dat hij aanvankelijk positieve resultaten had gezien. Tegen eind april, het team had 21 verschillende nanobodies geïdentificeerd die leken te concurreren met de ACE2-receptor, theoretisch het SARS-CoV-2-bevestigingsmechanisme blokkeren.
Toen begon het kleine team te groeien, het werven van structurele biologen om te onderzoeken hoe de nanobodies aan het SARS-CoV-2 spike-eiwit bonden, en vervolgens deze informatie te gebruiken om wijzigingen te ontwerpen om ze nog krachtiger te maken.
Dat vereiste het zuiveren van 21 kandidaat-eiwitten, hun binding testen, en vervolgens de cryo-elektronenmicroscopiefaciliteiten van UCSF te gebruiken om met bijna-atomaire resolutie de meest veelbelovende kandidaten in beeld te brengen, terwijl ze gebonden waren aan de SARS-CoV-2-piek. Om deze monumentale taak te volbrengen, ze bundelden hun krachten met een parallelle inspanning die bekend staat als het QCRG Structural Biology Consortium - een assemblagelijn-achtig proces dat is samengesteld door 12 UCSF-faculteitsleden en meer dan 60 stagiairs om SARS-CoV-2 aan te pakken. De inspanning werd gevoed door een gevoel van urgentie, en de deelnemers werkten slopende uren tot diep in de nacht.
Toen het team eenmaal beelden had van de top nanobodies gebonden aan de SARS-CoV-2-piek, ze begonnen het unieke bindingsmechanisme van elk nanobody te onderzoeken en gebruikten die informatie om een versie van de volgende generatie te ontwerpen. Ze besloten een driearmig nanolichaam te construeren, bestaande uit drie exemplaren van een enkel nanolichaam aan elkaar genaaid, zodat het tegelijkertijd kon binden aan de drie afzonderlijke armen waaruit elke coronaviruspiek bestaat.
Na de nanobodies aan elkaar te hebben genaaid en te hebben getest, Bryan Faust, een afgestudeerde student in het laboratorium van Manglik, leverde de volgende opwindende bevinding op:elk van de drie armen verbeterde de binding van zijn buren exponentieel. Het vermogen van de verbeterde versie om zich aan de virale pieken te binden nam met tweehonderdduizend toe.
"Dit was een geweldig resultaat - om deze enorme verbetering te zien, "Walter herinnert zich. "Het was absoluut feest."
Om de verbinding te testen tegen een levend virus, het team had een laboratorium nodig met een aanduiding van Biosafety Level 3 (BSL-3). De groep rekruteerde Marco Vignozzi, doctoraat, een voormalige UCSF-postdoc die een BSL-3-lab runt aan het Institut Pasteur in Parijs. tegen juni, een van Vignozzi's postdocs voerde het UCSF-nanobody uit tegen daadwerkelijk SARS-CoV-2 om te zien of het in staat was het virus te neutraliseren.
Het eindresultaat was zowel zeer effectief als stabiel - zo stabiel dat het in aerosolvorm kan worden afgeleverd met behulp van een gaasvernevelaar die Manglik op Amazon heeft gekocht.
Met de laserfocus van Big Pharma op het ontwikkelen van vaccins en traditionele antilichamen, het vinden van een snelle weg naar commercialisering is een uitdaging gebleken. Maar Manglik, Walter, en hun team zijn onverschrokken.
"Het is vrijwel zeker dat er in ons leven meer ademhalingspandemieën zullen zijn, " zegt Manglik. "Het kan griep zijn, helmknop SARS-pandemie, of een ziekteverwekker die we nog niet eens kennen. Voor de volgende pandemie, de hoop is dat onderzoekers niet alleen zo snel kunnen gaan als wij, maar misschien nog sneller."
Zonder twijfel, het zou moeilijk zijn om een krachtiger bewijs te vinden van de heerlijke onvoorspelbaarheid en het potentieel van de moderne wetenschap - dat een pandemie die eenzaamheid heeft veroorzaakt, lijden, en de dood gaf ook aanleiding tot deze eclectische bemanning en hun potentieel levensreddende oplossing die slechts een paar jaar geleden misschien absurd leek.
"Het is gewoon een van die dingen waarvan je zegt:"We willen dit avontuur aangaan, '" zegt Walter. "We hebben ons eraan gecommitteerd, en toen werkte het gewoon veel beter dan we hadden kunnen dromen."
 Wetenschappers zetten giftige pesticiden om in behandeling tegen antibioticaresistente bacteriën
Wetenschappers zetten giftige pesticiden om in behandeling tegen antibioticaresistente bacteriën Uitleggen waarom condensatie exotherm is
Uitleggen waarom condensatie exotherm is Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren
Wetenschappers ontwikkelen een nieuwe methode om de efficiëntie van luchtreinigers te verbeteren Hoe antilichamen te gebruiken om chemische reacties onder controle te houden?
Hoe antilichamen te gebruiken om chemische reacties onder controle te houden? Superhydrofobe magnetische spons om water uit olieproducten te helpen zuiveren
Superhydrofobe magnetische spons om water uit olieproducten te helpen zuiveren
 NASA vangt de aanlanding van tropische cycloon Avas aan de kust van Madagaskar
NASA vangt de aanlanding van tropische cycloon Avas aan de kust van Madagaskar Studie:Klimaatverandering treft kinderen onevenredig
Studie:Klimaatverandering treft kinderen onevenredig Waarom effectieve oplossingen voor klimaatverandering zo ongrijpbaar blijven
Waarom effectieve oplossingen voor klimaatverandering zo ongrijpbaar blijven NASA ziet vorming van tropische storm Fernanda in de oostelijke Stille Oceaan
NASA ziet vorming van tropische storm Fernanda in de oostelijke Stille Oceaan Ardern toert verwoestende overstromingen in Nieuw-Zeeland
Ardern toert verwoestende overstromingen in Nieuw-Zeeland
Hoofdlijnen
- Zenuwonderzoek laat zien hoe cellen zich aanpassen om schade te helpen herstellen
- Wat zijn emoties,
- Muizen in sociale conflicten vertonen gedrag dat zich aan regels houdt
- Tientallen nieuwe natuurcorridors geïdentificeerd voor Afrikaanse zoogdieren
- Lovelorn koala gepakt na ontsnapping uit dierentuin op jacht naar partner
- Dode walvis verrast zwemmers op iconisch strand van Rio
- Geneesmiddelresistentie uit schimmels verdrijven
- Woedend debat:houdt het ruimen van wolven stroperij tegen?
- Achter de puppy-hondenogen
- Zachte nanodeeltjes geven plasmonen nieuw potentieel
- Nieuwe analyse van de structuur van spinnenzijde verklaart de paradox van superkracht

- Wetenschappers krijgen een glimp van de innerlijke werking van atomair dunne transistoren

- Moleculaire diepteprofilering gemodelleerd met behulp van buckyballs en energiezuinig argon
- Gelaagde grafeensandwich voor de volgende generatie elektronica

 Wat zijn de echte kosten van een fles frisdrank (en al het andere)?
Wat zijn de echte kosten van een fles frisdrank (en al het andere)? Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs
Nieuw onderzoek onthult effect van opwarming van de aarde op het smelten van Groenlandse ijs Apple verkoopt een nieuwe batterijbehuizing voor zijn nieuwste iPhones ... voor $ 129
Apple verkoopt een nieuwe batterijbehuizing voor zijn nieuwste iPhones ... voor $ 129 Magnetisme en licht combineren om kanker te bestrijden
Magnetisme en licht combineren om kanker te bestrijden Op nul komen:de stad in Japan probeert al zijn afval te recyclen
Op nul komen:de stad in Japan probeert al zijn afval te recyclen Payrollgegevens Facebook-medewerker gestolen uit auto
Payrollgegevens Facebook-medewerker gestolen uit auto Snelle verkenning na de aardbeving van Anchorage in 2018 onthult tekenen van grondfalen
Snelle verkenning na de aardbeving van Anchorage in 2018 onthult tekenen van grondfalen Waymo brengt zelfrijdende vrachtwagens naar snelwegen in Phoenix area
Waymo brengt zelfrijdende vrachtwagens naar snelwegen in Phoenix area
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

