
Wetenschap
Ingenieurs maken nanodeeltjes die hulpmiddelen voor het bewerken van genen leveren aan specifieke weefsels en organen

Krediet:CC0 Publiek Domein
Een van de meest opmerkelijke recente vorderingen in biomedisch onderzoek is de ontwikkeling van zeer gerichte methoden voor het bewerken van genen, zoals CRISPR, die kunnen toevoegen, verwijderen, of met grote precisie een gen in een cel veranderen. De methode wordt al getest of gebruikt voor de behandeling van patiënten met sikkelcelanemie en kankers zoals multipel myeloom en liposarcoom, en vandaag, de makers Emmanuelle Charpentier en Jennifer Doudna ontvingen de Nobelprijs voor scheikunde.
Hoewel het bewerken van genen opmerkelijk nauwkeurig is in het vinden en veranderen van genen, er is nog steeds geen manier om de behandeling op specifieke locaties in het lichaam te richten. De tot nu toe geteste behandelingen omvatten het verwijderen van bloedstamcellen of T-cellen van het immuunsysteem uit het lichaam om ze te modificeren, en ze vervolgens terug in een patiënt te injecteren om de bloedbaan opnieuw te bevolken of een immuunrespons te herstellen - een duur en tijdrovend proces.
Voortbouwend op de prestaties van Charpentier en Doudna, Tufts-onderzoekers hebben voor het eerst een manier bedacht om gen-editing-pakketten op een efficiënte manier door de bloed-hersenbarrière en in specifieke hersengebieden te brengen, in cellen van het immuunsysteem, of aan specifieke weefsels en organen in muismodellen. Deze toepassingen zouden een geheel nieuwe strategie kunnen openen voor de behandeling van neurologische aandoeningen, evenals kanker, besmettelijke ziekte, en auto-immuunziekten.
Een team van Tufts biomedische ingenieurs, onder leiding van universitair hoofddocent Qiaobing Xu, probeerde een manier te vinden om de "kit" voor het bewerken van genen te verpakken, zodat het kon worden geïnjecteerd om zijn werk in het lichaam op gerichte cellen te doen, in plaats van in een laboratorium.
Ze gebruikten lipidenanodeeltjes (LNP's) - kleine "bubbels" van lipidemoleculen die de bewerkingsenzymen kunnen omhullen en naar specifieke cellen kunnen transporteren. weefsels, of organen. Lipiden zijn moleculen met een lange koolstofstaart, waardoor ze een "vette" consistentie krijgen, en een hydrofiele kop, die wordt aangetrokken door een waterige omgeving.
Er is ook typisch een stikstof, zwavel, of op zuurstof gebaseerde verbinding tussen kop en staart. De lipiden rangschikken zich rond de bubbel-nanodeeltjes met de koppen naar buiten gericht en de staarten naar binnen gericht naar het midden.
Xu's team was in staat om het oppervlak van deze LNP's aan te passen, zodat ze uiteindelijk aan bepaalde celtypen kunnen "kleven", versmelten met hun membranen, en laten de gen-editing enzymen in de cellen vrij om hun werk te doen.
Het maken van een gerichte LNP vereist wat chemisch knutselen.
Door een mix van verschillende koppen te creëren, staarten, en linkers, de onderzoekers kunnen - eerst in het laboratorium - een grote verscheidenheid aan kandidaten screenen op hun vermogen om LNP's te vormen die zich richten op specifieke cellen. De beste kandidaten kunnen vervolgens worden getest in muismodellen, en verder chemisch gemodificeerd om de targeting en afgifte van de gen-editing-enzymen aan dezelfde cellen in de muis te optimaliseren.
"We hebben een methode ontwikkeld om het leveringspakket op maat te maken voor een breed scala aan potentiële therapieën, inclusief genbewerking, " zei Xu. "De methoden zijn gebaseerd op combinatorische chemie die door de farmaceutische industrie wordt gebruikt voor het ontwerpen van de medicijnen zelf, maar in plaats daarvan passen we de benadering toe bij het ontwerpen van de componenten van het bestelvoertuig."
In een ingenieus stukje chemische modellering, Xu en zijn team gebruikten een neurotransmitter aan de kop van sommige lipiden om de deeltjes te helpen de bloed-hersenbarrière te passeren, die anders ondoordringbaar zouden zijn voor molecuulsamenstellingen zo groot als een LNP.
Het vermogen om medicijnen veilig en efficiënt door de barrière en in de hersenen te brengen, is al lang een uitdaging in de geneeskunde. In een eerste, Xu's lab leverde een heel complex van boodschapper-RNA's en enzymen die de CRISPR-kit vormen, in gerichte hersengebieden van een levend dier.
Enkele kleine aanpassingen aan de lipide-linkers en -staarten hielpen bij het creëren van LNP's die in de hersenen het kleine molecuul antischimmelmedicijn amfotericine B (voor de behandeling van meningitis) en een DNA-fragment dat bindt aan het gen dat het tau-eiwit produceert dat verband houdt met de ziekte van Alzheimer, kunnen afgeven. ziekte.
Recenter, Xu en zijn team hebben LNP's gemaakt om genbewerkingspakketten in T-cellen in muizen af te leveren. T-cellen kunnen helpen bij de productie van antilichamen, vernietig geïnfecteerde cellen voordat virussen zich kunnen vermenigvuldigen en verspreiden, en reguleren en onderdrukken andere cellen van het immuunsysteem.
De LNP's die ze creëerden, fuseren met T-cellen in de milt of lever - waar ze zich meestal bevinden - om de inhoud voor het bewerken van genen te leveren, die vervolgens de moleculaire samenstelling en het gedrag van de T-cel kunnen veranderen. Het is een eerste stap in het proces van niet alleen het trainen van het immuunsysteem, zoals men zou kunnen doen met een vaccin, maar in feite het ontwikkelen om ziekten beter te bestrijden.
Xu's benadering van het bewerken van T-celgenomen is veel gerichter, efficiënt, en waarschijnlijk veiliger zijn dan methoden die tot nu toe zijn geprobeerd met virussen om hun genoom te wijzigen.
"Door zich op T-cellen te richten, we kunnen een tak van het immuunsysteem aanboren die enorm veelzijdig is in het bestrijden van infecties, beschermen tegen kanker, en het moduleren van ontsteking en auto-immuniteit, " zei Xu.
Xu en zijn team onderzochten verder het mechanisme waarmee LNP's hun weg naar hun doelen in het lichaam zouden kunnen vinden. In experimenten gericht op cellen in de longen, ze ontdekten dat de nanodeeltjes na injectie specifieke eiwitten in de bloedbaan oppikten.
de eiwitten, nu opgenomen in het oppervlak van de LNP's, werd het belangrijkste onderdeel dat de LNP's hielp om hun doelwit vast te houden. Deze informatie kan helpen bij het verbeteren van het ontwerp van toekomstige afleveringsdeeltjes.
Hoewel deze resultaten zijn aangetoond bij muizen, Xu waarschuwde dat er meer studies en klinische proeven nodig zullen zijn om de werkzaamheid en veiligheid van de toedieningsmethode bij mensen te bepalen.
 Wat zijn de kleuren van Neon?
Wat zijn de kleuren van Neon?  On-the-fly analyse van hoe katalysatoren veranderen tijdens reacties om de prestaties te verbeteren
On-the-fly analyse van hoe katalysatoren veranderen tijdens reacties om de prestaties te verbeteren Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden
Biosensortechnologieën om effectievere benaderingen van ziektebehandeling te bieden Zelfgemaakte heldere vloeibare kunststof
Zelfgemaakte heldere vloeibare kunststof  Wetenschappers ontcijferen het multi-domein, volledige structuur van de humane smoothened receptor
Wetenschappers ontcijferen het multi-domein, volledige structuur van de humane smoothened receptor
 Nieuw onderzoek verklaart toekomstige effecten van de uitstoot van broeikasgassen
Nieuw onderzoek verklaart toekomstige effecten van de uitstoot van broeikasgassen Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen
Vijf manieren waarop kunst kan helpen de plasticcrisis op te lossen Hoe Tweet-A-Watt werkt
Hoe Tweet-A-Watt werkt  Australische steden op de heetste plekken op aarde terwijl de hittegolf sist
Australische steden op de heetste plekken op aarde terwijl de hittegolf sist Waarom orkanen sommige plaatsen keer op keer verwoesten:een meteoroloog legt uit
Waarom orkanen sommige plaatsen keer op keer verwoesten:een meteoroloog legt uit
Hoofdlijnen
- Hoe het placebo-effect werkt
- Welke organellen worden beschouwd als het cellen recyclingscentrum?
- Drie nieuwe soorten zoantharen beschreven vanaf koraalriffen in de Indo-Pacific
- Structuur van primaire optogenetische tool onthuld
- Energiestroom (ecosysteem): definitie, proces en voorbeelden (met diagram)
- Team publiceert onderzoek naar ongewone genevolutie in bacteriën
- Unieke manieren om een DNA-model te bouwen
- Hands-on Science Activiteiten op Blood
- Het verschil tussen histon en nonhistone
- Wetenschappers onthullen leegte-opsluitingseffecten van holle nanoreactoren
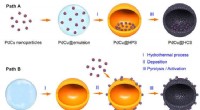
- Gevestigde massaproductietechnologie voor nanodeeltjes van vaste-oplossinglegeringen
- Volledig functionele nano-sneeuwman heeft toepassingen voor groenere energie
- Onderzoekers ontwikkelen kleine gradiëntchip:systeem maakt het gemakkelijker om chemische reactiviteit te meten
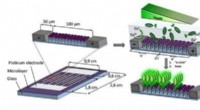
- Team demonstreert grootschalige techniek om kwantumstippen te produceren

 Volharding Marsrover legt video vast, audio van de vierde Ingenuity-vlucht
Volharding Marsrover legt video vast, audio van de vierde Ingenuity-vlucht Hoe duplicaten in twee rijen in OpenOffice te verwijderen
Hoe duplicaten in twee rijen in OpenOffice te verwijderen  Volledig optische diffractieve neurale netwerken verwerken breedbandlicht
Volledig optische diffractieve neurale netwerken verwerken breedbandlicht Hoe bomen naast elkaar bestaan:nieuwe bevindingen uit onderzoek naar biodiversiteit
Hoe bomen naast elkaar bestaan:nieuwe bevindingen uit onderzoek naar biodiversiteit De Facebook Flick en andere vreemde meeteenheden
De Facebook Flick en andere vreemde meeteenheden  De voor- en nadelen van Queuing Theory
De voor- en nadelen van Queuing Theory NASA vindt zware regen ten zuidwesten van tropische cycloon Uesis center
NASA vindt zware regen ten zuidwesten van tropische cycloon Uesis center Risicoanalyse cruciaal instrument voor de bestrijding van mensenhandel
Risicoanalyse cruciaal instrument voor de bestrijding van mensenhandel
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

