
Wetenschap
Een schakelaar die het verkeer over bloedvaten regelt
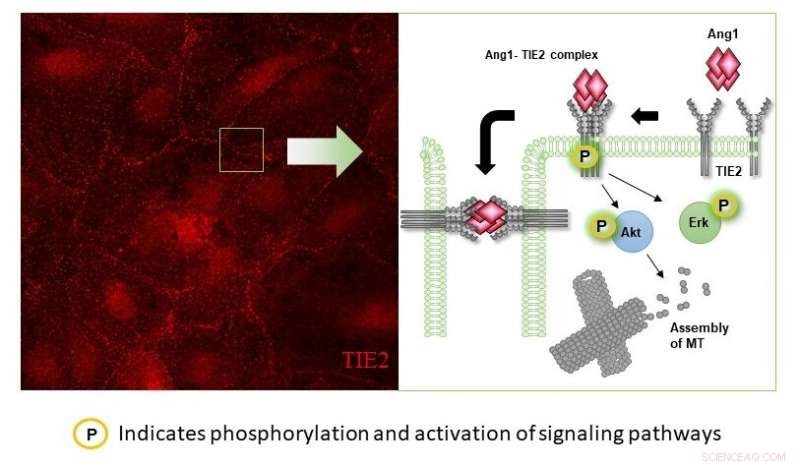
Voorgesteld mechanisme van door angiopoetin-1 (Ang-1) geïnduceerd anti-permeabiliteitseffect in menselijke microvasculaire endotheelcellen. De afbeelding aan de linkerkant toont bloedvatencellen die zijn gekleurd om de locatie van het eiwit TIE2 te identificeren. Wanneer de activator Angiopoetin-1 (Ang-1) wordt toegepast, TIE2 zijn gelokaliseerd nabij het celoppervlak waar Ang1-Tie2 een brug vormt die cellen bij elkaar houdt. In volgende experimenten, het is aangetoond dat Angl-binding cellulaire veranderingen zou kunnen bemiddelen door ofwel de fosforylering van Akt of Erk te verhogen, wat vervolgens helpt de microtubuli te stabiliseren om de cellulaire structuur te behouden. Krediet:Nationale Universiteit van Singapore
NUS-wetenschappers hebben een controlemechanisme ontdekt dat het verkeer van cellen en stoffen door bloedvaten regelt. Dit effect kan een aanzienlijke invloed hebben op de uitzaaiing van kanker.
Nanodeeltjes worden gebruikt in verschillende biomedische toepassingen, inclusief de diagnose en behandeling van kanker. Geneesmiddelafgevende nanodeeltjes zouden kunnen worden geprogrammeerd om geneesmiddelen lokaal af te leveren op de tumorplaats. Echter, recente studies hebben aangetoond dat deze nanodeeltjes kunnen leiden tot de vorming van micrometergrote gaten in de wanden van bloedvaten, waardoor ze "lek" worden. Bij kankerpatiënten, deze gaten kunnen het voor overlevende kankercellen gemakkelijker maken om van hun primaire plaatsen naar andere delen van het lichaam te ontsnappen.
Een onderzoeksteam bestaande uit Prof HO Han Kiat van de afdeling Farmacie, NUS en Prof David LEONG van de afdeling Chemische en Biomoleculaire Engineering, NUS ontdekte dat Angiopoëtine-1 (een soort eiwit) kan helpen om de door nanodeeltjes veroorzaakte openingen in de bloedvaten te dichten en hun doorlaatbaarheid te verminderen. Dit, beurtelings, regelt de doorgang van stoffen en moleculen door de wanden van de bloedvaten. Door de hoeveelheid Angiopoëtine-1 in het lichaam aan te passen, de onderzoekers ontdekten dat ze de "lekken" die in bloedvaten worden veroorzaakt door nanodeeltjes in biomedische toepassingen, kunnen beperken en omkeren.
In hun experimenten, het onderzoeksteam diende borstkankercellen toe onder de huid van muizenmodellen en introduceerde vervolgens titaniumdioxide-nanodeeltjes in hun bloedvaten. Ze stelden vast dat de nanodeeltjes de lekkage van kankercellen in de bloedvaten vergrootten. Dit lekkage-effect kan de beweging van circulerende kankercellen naar verre weefsels verbeteren, wat kan resulteren in de vorming van nieuwe secundaire kankerplaatsen die voorheen niet toegankelijk waren voor de kankercellen.
In vervolg hierop, het team ontdekte dat Angiopoëtine-1 fungeert als een groeifactor voor TIE2, een regelgever van het celoppervlak die van nature in onze bloedvaten voorkomt. Wanneer er meer Angiopoëtine-1 zijn, TIE2-eiwit wordt gelokaliseerd en gestimuleerd om de gaten in de bloedvaten te dichten die door de nanodeeltjes zouden kunnen worden veroorzaakt. Dit vermindert op zijn beurt de doorlaatbaarheid van de bloedvaten en beperkt de hoeveelheid kankercellen die in de bloedbaan lekt.
Prof Ho zei, "De studie toonde aan dat Angiopoëtine-1 mogelijk kan worden gebruikt als een tegenmechanisme om de lekkage veroorzaakt door nanodeeltjes te beperken en om te keren. Dit helpt de extravasatie en het transport van kankercellen naar andere weefsels bij kankerpatiënten te verminderen."
 Op algen geïnspireerde polymeren verlichten de weg voor verbeterd nachtzicht
Op algen geïnspireerde polymeren verlichten de weg voor verbeterd nachtzicht Een biosensor voor het meten van extracellulaire waterstofperoxideconcentraties
Een biosensor voor het meten van extracellulaire waterstofperoxideconcentraties Biologisch afbreekbare gewasbeschermingsmiddelen zonder risico's of bijwerkingen
Biologisch afbreekbare gewasbeschermingsmiddelen zonder risico's of bijwerkingen Onderzoekers vinden veelbelovende kandidaten voor nanodeeltjes voor het afvangen en omzetten van koolstofdioxide
Onderzoekers vinden veelbelovende kandidaten voor nanodeeltjes voor het afvangen en omzetten van koolstofdioxide Hoe de kegelslak dodelijk gif ons kan helpen betere medicijnen te maken
Hoe de kegelslak dodelijk gif ons kan helpen betere medicijnen te maken
 Staten noemen klimaatzorgen om de verkoop van steenkool in de VS te stoppen
Staten noemen klimaatzorgen om de verkoop van steenkool in de VS te stoppen Aanhoudende droogte leidt tot grote voedselzekerheidscrisis in Somalië
Aanhoudende droogte leidt tot grote voedselzekerheidscrisis in Somalië Een blik op 377 metro's:kunnen lokale voedselproducten voldoen aan de lokale vraag van huishoudens?
Een blik op 377 metro's:kunnen lokale voedselproducten voldoen aan de lokale vraag van huishoudens? Waarom is het oog van een orkaan kalm?
Waarom is het oog van een orkaan kalm?  Brand geblust op getroffen olietanker bij Sri Lanka
Brand geblust op getroffen olietanker bij Sri Lanka
Hoofdlijnen
- Interacties tussen eenvoudige moleculaire mechanismen leiden tot complexe infectiedynamiek
- Waarom wordt natrium gebruikt in DNA-extractie?
- Histologie maken Slides
- Paranoia zal vernietigen:wanneer overschrijdt gezonde angst de grens in paranoia?
- Dance-gerelateerde wetenschapsprojecten
- Nieuwe hoop voor ernstig bedreigde aap met stompe neus in Myanmar
- Hoop op een van 's werelds zeldzaamste primaten:eerste telling van Zanzibar Red Colobus-aap
- Honden en wolven delen parasieten
- Zelfs wilde zoogdieren hebben regionale dialecten
- Team berekent de rol van begraven lagen in epitaxiaal grafeen met enkele lagen

- Onderzoekers fabriceren robuuste superhydrofobe films van anisotrope silicadeeltjes

- Je hersenen op mesh:injecteerbare flexibele sonde versmelt met neuronen, veroorzaakt weinig of geen chronische immuunrespons
- Nieuw voorbehandelingsproces levert biocompatibele, stabiele gouden nanostaafjes voor tumorbehandeling
- Team rapporteert schaalbare fabricage van zelf-uitgelijnde grafeentransistors, circuits

 Amerikaanse luchtvaartmaatschappijen wanhopig op zoek naar contant geld, maar vrezen overheidsbemoeienis
Amerikaanse luchtvaartmaatschappijen wanhopig op zoek naar contant geld, maar vrezen overheidsbemoeienis Geo-engineering, andere technologieën zullen klimaatproblemen niet oplossen
Geo-engineering, andere technologieën zullen klimaatproblemen niet oplossen China meldt geen grote instortingen na krachtige aardbeving
China meldt geen grote instortingen na krachtige aardbeving Meer mensen die langer in federaal begeleide huisvesting blijven, ondermijnt het vermogen om gezinnen te dienen, studie vondsten
Meer mensen die langer in federaal begeleide huisvesting blijven, ondermijnt het vermogen om gezinnen te dienen, studie vondsten 5 Feiten over de innerlijke kern van de aarde
5 Feiten over de innerlijke kern van de aarde  Onderzoekers maken 3D-geprinte, zwetende robotspier
Onderzoekers maken 3D-geprinte, zwetende robotspier Lijst met basisapparatuur voor lassen
Lijst met basisapparatuur voor lassen  Verschillende soorten bladeren
Verschillende soorten bladeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Italian | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

