
Wetenschap
Nieuw voorbehandelingsproces levert biocompatibele, stabiele gouden nanostaafjes voor tumorbehandeling
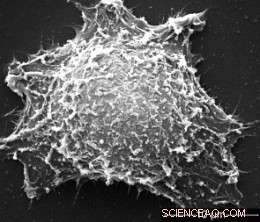
(PhysOrg.com) -- Goud is niet alleen mooi in sieraden; het wordt al lang als medicijn gebruikt. De moderne geneeskunde is vooral gericht op nanoscopisch goud, die kan worden gebruikt als contrastmiddel en bij de behandeling van kanker. In het journaal Angewandte Chemie , Eugene R. Zubarev en zijn team aan de Rice University in Houston hebben nu een nieuw voorbehandelingsproces voor gouden nanostaafjes geïntroduceerd dat hun gebruik in medische toepassingen zou kunnen versnellen.
Hoe kunnen kleine goudstaafjes kanker helpen bestrijden? Kankercellen zijn gevoeliger voor temperatuur dan gezond weefsel, en dit feit kan worden benut door lokale verwarming van de aangetaste delen van het lichaam. Dit is waar de gouden nanostaafjes in het spel komen. Ze kunnen worden ingebracht in de kankercellen en de zieke gebieden die worden bestraald met nabij-infrarood licht (foto-geïnduceerde hyperthermie). De staafjes absorberen dit licht zeer sterk en zetten de lichtenergie om in warmte, die ze doorgeven aan hun omgeving.
Gouden nanostaafjes worden normaal gesproken geproduceerd in een geconcentreerde oplossing van cetyltrimethylammoniumbromide (CTAB) en zijn dus gecoat in een dubbele laag CTAB. De CTAB wordt alleen op het oppervlak afgezet, niet chemisch gebonden. In een waterige omgeving, de CTAB-moleculen lossen langzaam op. Dit is problematisch omdat CTAB zeer giftig is. Het simpelweg weglaten van de CTAB is geen oplossing, want zonder deze coating zouden de nanostaafjes aan elkaar klonteren. Om de staven zowel stabiel als biocompatibel te maken, er zijn verschillende min of meer complexe voorbehandelingsmethoden ontwikkeld. Echter, voor veel van deze processen het is niet bekend hoeveel van het giftige CTAB op de nanostaafjes achterblijft. Een ander probleem is dat de voorbehandeling de opname van de nanostaafjes in cellen kan verstoren, die het succes van fotothermische kankerbehandeling drastisch vermindert.
Zubarev en zijn medewerkers hebben nu een nieuwe strategie ontwikkeld die deze problemen oplost:ze hebben de CTAB vervangen door een variant die een zwavel-waterstofgroep bevat, afgekort als MTAB. Met verschillende analytische processen, de wetenschappers hebben kunnen bewijzen dat de CTAB op deze nanostaafjes volledig is vervangen door een MTAB-laag. De MTAB-moleculen binden zich chemisch aan gouden nanostaafjes via hun zwavelatomen. Ze binden zo stevig dat de laag zelfs in een waterige oplossing op zijn plaats blijft en de staven zelfs kunnen worden gevriesdroogd. Ze zijn onbeperkt houdbaar als bruin poeder en lossen binnen enkele seconden weer op in water.
Tests op celculturen tonen aan dat gouden nanostaafjes van MTAB niet giftig zijn, zelfs bij hogere concentraties. In aanvulling, ze worden in grote hoeveelheden opgenomen door tumorcellen. De wetenschappers schatten dat onder de omstandigheden van hun experiment, een enkele cel neemt meer dan twee miljoen nanostaafjes in beslag. Dit zou een effectieve fotothermische tumorbehandeling mogelijk maken.
 Canadees leger alert terwijl bosbranden woeden
Canadees leger alert terwijl bosbranden woeden Honderden scholen sluiten vanwege giftige smog die Bangkok verstikt
Honderden scholen sluiten vanwege giftige smog die Bangkok verstikt De epidemie van doekjes en maskers plaagt riolen, stormafvoeren
De epidemie van doekjes en maskers plaagt riolen, stormafvoeren Sedimenten onthullen moessonneerslagmechanisme in centraal-oostelijk China
Sedimenten onthullen moessonneerslagmechanisme in centraal-oostelijk China Studie onthult onzekerheid over hoeveel koolstof de oceaan in de loop van de tijd absorbeert
Studie onthult onzekerheid over hoeveel koolstof de oceaan in de loop van de tijd absorbeert
Hoofdlijnen
- Onderzoek toont aan dat honden slimmer zijn dan katten
- Elektronenmicroscoopbeelden laten zien hoe cellen een vitaal mineraal opnemen
- Hoe symbiose werkt
- Wetenschapper duikt in honderden onderwatergrotten op zoek naar nieuwe vormen van leven
- Leuke wetenschappelijke experimenten op cellen
- De evolutionaire oorsprong van de darm
- Vergroening van citrusvruchten behandelen met koper:effecten op bomen, bodems
- Je lichaam aan: een hittegolf
- Wat gebeurt er als mitose verkeerd gaat?
- Nieuwe nanosensoren voor de detectie van TNT
- Grafeen is zowel transparant als ondoorzichtig voor straling

- Onderzoekers omarmen imperfectie om het transport van biomoleculen te verbeteren

- Onderzoekers creëren een schakelaar met één molecuul

- Verbetering van de werkzaamheid van immuniteitsactiverende nucleïnezuurgeneesmiddelen
 Is uw supercomputer stumped? Er is misschien een kwantumoplossing
Is uw supercomputer stumped? Er is misschien een kwantumoplossing Twee Korea's op scherp terwijl tyfoon schiereiland nadert
Twee Korea's op scherp terwijl tyfoon schiereiland nadert Wafeldun materiaal luidt de toekomst van draagbare technologie in
Wafeldun materiaal luidt de toekomst van draagbare technologie in Wat is 5 cent waard?
Wat is 5 cent waard?  Onderzoekers starten magnetische spingolven op nanoschaal op in hun zoektocht naar low-energy computing
Onderzoekers starten magnetische spingolven op nanoschaal op in hun zoektocht naar low-energy computing Horseshoe Crab Science Project
Horseshoe Crab Science Project  Een wet ter bescherming van degenen die slachtoffers van geweld tegen vrouwen steunen
Een wet ter bescherming van degenen die slachtoffers van geweld tegen vrouwen steunen Op de natuur geïnspireerde materialen kunnen worden gebruikt in toepassingen variërend van tunneling tot ruimtevaart
Op de natuur geïnspireerde materialen kunnen worden gebruikt in toepassingen variërend van tunneling tot ruimtevaart
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

