
Wetenschap
Gecamoufleerde nanodeeltjes die worden gebruikt om killer-eiwit aan kanker te leveren
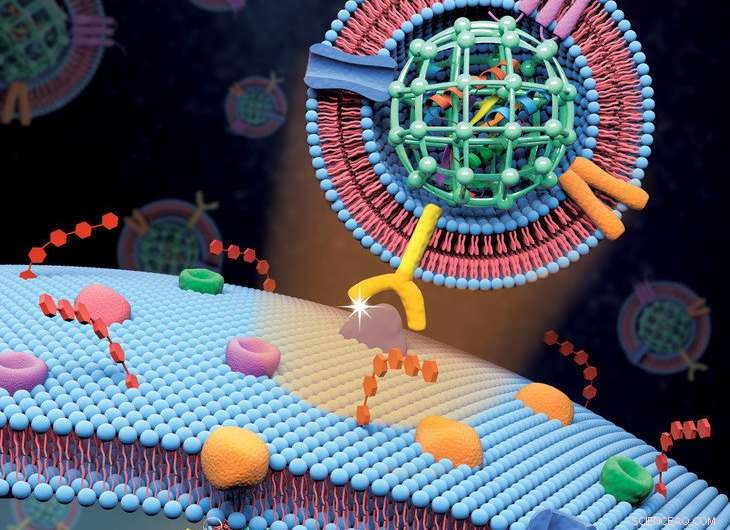
Extracellulaire blaasjesachtige metaal-organische nanodeeltjes zijn ontwikkeld voor de intracellulaire afgifte van biofunctionele eiwitten. Het biomimetische nanoplatform kan de eiwitlading beschermen en verschillende biologische barrières overwinnen om systemische levering en autonome afgifte te bereiken. Krediet:Zheng Lab/Penn State
Een biomimetisch nanosysteem kan therapeutische eiwitten leveren om selectief kankertumoren aan te pakken, volgens een team van onderzoekers van Penn State.
Met behulp van een eiwittoxine genaamd gelonine van een plant in de Himalaya, de onderzoekers sloten de eiwitten op in zelf-geassembleerde metaal-organische raamwerken (MOF) nanodeeltjes om ze te beschermen tegen het immuunsysteem van het lichaam. Om de levensduur van het medicijn in de bloedbaan te verlengen en om de tumor selectief aan te pakken, het team verhulde de MOF in een coating gemaakt van cellen uit de tumor zelf.
Bloed is een vijandige omgeving voor medicijnafgifte. Het immuunsysteem van het lichaam valt buitenaardse moleculen aan of spoelt ze uit het lichaam via de milt of lever. Maar cellen, inclusief kankercellen, laat kleine deeltjes vrij die extracellulaire blaasjes worden genoemd en die communiceren met andere cellen in het lichaam en een "eet me niet"-signaal naar het immuunsysteem sturen.
"We hebben een strategie ontworpen om te profiteren van de extracellulaire blaasjes die zijn afgeleid van tumorcellen, " zei Siyang Zheng, universitair hoofddocent biomedische en elektrotechniek aan Penn State. "We verwijderen 99 procent van de inhoud van deze extracellulaire blaasjes en gebruiken vervolgens het membraan om onze metaal-organische nanodeeltjes in te pakken. Als we onze extracellulaire blaasjes van de patiënt kunnen krijgen, door middel van een biopsie of operatie, dan zullen de nanodeeltjes de tumor opzoeken via een proces dat homotypische targeting wordt genoemd."
Gong Cheng, hoofdauteur van een nieuw artikel waarin het werk van het team wordt beschreven en een voormalig postdoctoraal wetenschapper in de groep van Zheng, nu aan Harvard, zei, "MOF is een klasse van kristallijne materialen samengesteld door metalen knopen en organische linkers. In ons ontwerp, zelfassemblage van MOF-nanodeeltjes en inkapseling van eiwitten worden gelijktijdig bereikt door een eenpotsbenadering in een waterige omgeving. De verrijkte metaalaffiniteitsplaatsen op MOF-oppervlakken werken als de knoophaak, zodat het extracellulaire vesikelmembraan gemakkelijk op de MOF-nanodeeltjes kan worden geknikt. Onze biomimetische strategie zorgt ervoor dat de synthetische nanodeeltjes eruitzien als extracellulaire blaasjes, maar ze hebben de gewenste lading binnen."
Het nanodeeltjessysteem circuleert in de bloedbaan totdat het de tumor vindt en zich vastklampt aan het celmembraan. De kankercel neemt het nanodeeltje op in een proces dat endocytose wordt genoemd. Eenmaal in de cel, de hogere zuurgraad van de intracellulaire transportblaasjes van de kankercel zorgt ervoor dat de metaal-organische nanodeeltjes uit elkaar vallen en het giftige eiwit vrijgeven in cytosol en de cel doden.
"Ons metaal-organisch frame heeft een zeer hoog laadvermogen, dus we hoeven niet veel van de deeltjes te gebruiken en dat houdt de algemene toxiciteit laag, ' zei Zheng.
De onderzoekers bestudeerden de effectiviteit van het nanosysteem en de toxiciteit ervan in een klein diermodel en rapporteerden hun bevindingen in een omslagartikel in de Tijdschrift van de American Chemical Society .
De onderzoekers geloven dat hun nanosysteem een hulpmiddel biedt voor de gerichte levering van andere eiwitten die verhuld moeten worden door het immuunsysteem. Penn State heeft octrooibescherming aangevraagd voor de technologie.
 Infraroodsensor als nieuwe methode voor medicijnontdekking
Infraroodsensor als nieuwe methode voor medicijnontdekking Bakstenen bouwen van plastic afval
Bakstenen bouwen van plastic afval Middeleeuwse kruitrecepten opblazen
Middeleeuwse kruitrecepten opblazen Interfacial engineering core@shell nanodeeltjes voor actieve en selectieve directe H2O2-generatie
Interfacial engineering core@shell nanodeeltjes voor actieve en selectieve directe H2O2-generatie Polymeren die ziektekiemen snel en effectief doden, zullen helpen in de strijd tegen multiresistente microben
Polymeren die ziektekiemen snel en effectief doden, zullen helpen in de strijd tegen multiresistente microben
 Klimaatverandering, armoede en mensenrechten:een noodsituatie zonder precedent
Klimaatverandering, armoede en mensenrechten:een noodsituatie zonder precedent Wat is een condensatie-eenheid?
Wat is een condensatie-eenheid?  Grondwateronderzoeken kunnen worden aangetast door vooringenomenheid van overlevenden
Grondwateronderzoeken kunnen worden aangetast door vooringenomenheid van overlevenden Eigenzinnig zomermoessongedrag beïnvloedt regenval in Oost-Azië
Eigenzinnig zomermoessongedrag beïnvloedt regenval in Oost-Azië Krachtig, lokale verhalen kunnen ons inspireren om actie te ondernemen tegen klimaatverandering
Krachtig, lokale verhalen kunnen ons inspireren om actie te ondernemen tegen klimaatverandering
Hoofdlijnen
- Hoe bijen hun weg naar huis vinden
- Vleugelafdrukken kunnen individuele vleermuizen net zo effectief identificeren als vingerafdrukken mensen identificeren
- Introns versus Exons: Wat zijn de overeenkomsten & verschillen?
- Is de Krebs-cyclus aëroob of anaëroob?
- Interessante feiten over DNA-vingerafdrukken
- 10 fascinerende feiten over de nieuwe levensboom-evolutiekaart
- Een veranderend klimaat, wijn wisselen
- Hoe een cel te splitsen in Two
- Clathrin-assemblage definieert het begin en de geometrie van corticale patronen
- Een vooruitgang in de richting van ultradraagbare elektronische apparaten

- Hightech nanovezels kunnen helpen om voedingsstoffen in voedsel ter plaatse te krijgen

- Onderzoeksteam ontwikkelt het eerste flexibele random access memory met faseverandering
- Onderzoekers modelleren plasmonische convectie op macroschaal om de beweging van vloeistof en deeltjes te beheersen
- Banden omgezet in grafeen dat sterker beton maakt

 Energieonderzoekers bedenken foutloze katalysatoren
Energieonderzoekers bedenken foutloze katalysatoren Van het toilet tot de gootsteen:waterrecycling bestrijdt schaarste
Van het toilet tot de gootsteen:waterrecycling bestrijdt schaarste Blauwe pigmentontdekker maakt belangrijke ontwerpvooruitgang voor toekomstig duurzaam, levendige pigmenten
Blauwe pigmentontdekker maakt belangrijke ontwerpvooruitgang voor toekomstig duurzaam, levendige pigmenten Groepen meetinstrument sondes zonnecelmaterialen
Groepen meetinstrument sondes zonnecelmaterialen Een machine learning-techniek gebruiken om een hondachtige robot wendbaarder en sneller te maken
Een machine learning-techniek gebruiken om een hondachtige robot wendbaarder en sneller te maken Klimaatverandering komt voor je snacks:waarom herhaalde droogte gedroogd fruit en groenten bedreigt
Klimaatverandering komt voor je snacks:waarom herhaalde droogte gedroogd fruit en groenten bedreigt Waar vindt u geodes
Waar vindt u geodes  Aanpassen aan fluctuerende temperaturen
Aanpassen aan fluctuerende temperaturen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | German | Dutch | Danish | Norway | Portuguese | Swedish |

-
Wetenschap © https://nl.scienceaq.com

