
Wetenschap
Superresolutiesysteem onthult mechanica van kleine DNA-walker
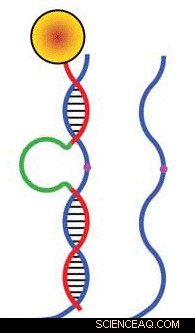
Deze geanimeerde gif toont het loopmechanisme achter een DNA-loopsysteem dat biomedische en industriële toepassingen kan vinden. Krediet:Purdue University-afbeelding / Jared Pike
Onderzoekers hebben een nieuw type 'superresolutie'-microscopie geïntroduceerd en deze gebruikt om het precieze loopmechanisme te ontdekken achter kleine structuren gemaakt van DNA die biomedische en industriële toepassingen zouden kunnen vinden.
De onderzoekers toonden ook aan hoe de "DNA-walker" een geneesmiddel tegen kanker kan afgeven, die een potentiële nieuwe biomedische technologie vertegenwoordigen, zei Jong Hyun Choi, een universitair hoofddocent werktuigbouwkunde aan de Purdue University.
Synthetische nanomotoren en rollators zijn ingewikkeld ontworpen systemen die chemische energie uit de omgeving halen en omzetten in mechanische beweging. Echter, omdat ze te klein zijn om te worden waargenomen met conventionele lichtmicroscopen, onderzoekers zijn niet in staat geweest om de precieze stappen te leren die betrokken zijn bij de loopmechanismen, kennis die essentieel is voor het perfectioneren van de technologie.
"Als je deze wandelaars niet in actie kunt oplossen of volgen, je zult hun mechanische werking niet kunnen begrijpen, ' zei Choi.
Hij leidde een Purdue-team dat dit probleem heeft opgelost door een superresolutiemicroscopiesysteem te ontwikkelen dat is ontworpen om de DNA-wandelaars te bestuderen. De nieuwe bevindingen verschenen in het tijdschrift wetenschappelijke vooruitgang op 20 januari.
Onderzoekers over de hele wereld maken synthetische motoren op basis van DNA en RNA, de genetische materialen in cellen die bestaan uit een opeenvolging van vier chemische basen:adenine, guanine, cytosine en thymine. De ontwerpen zijn geïnspireerd op natuurlijke biologische motoren die zijn geëvolueerd om specifieke taken uit te voeren die cruciaal zijn voor de functie van cellen.
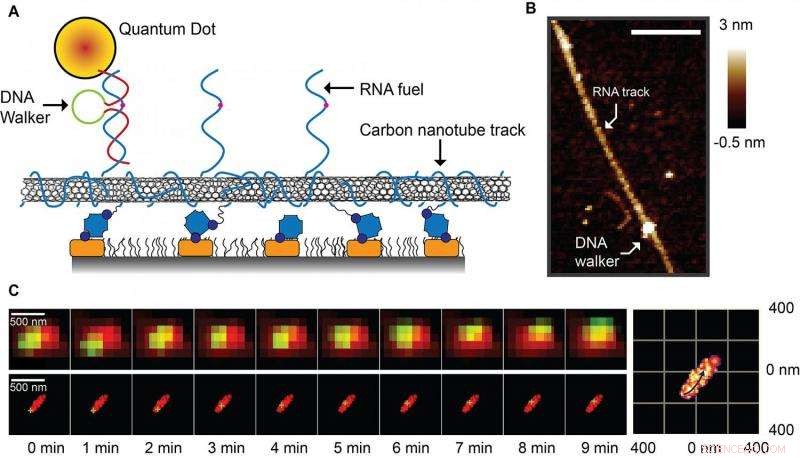
Een nieuw type 'superresolutie'-microscopie heeft onderzoekers van de Purdue University in staat gesteld het loopmechanisme achter een DNA-loopsysteem te bepalen dat biomedische en industriële toepassingen zou kunnen vinden. De wandelaar (A) reist langs een koolstof-nanobuisspoor dat "versierd" is met strengen RNA-brandstof, die het oogst voor energie. Een atomic force microscoopafbeelding (B) toont de DNA-walker die aan dit spoor is bevestigd. Onderaan zijn onbewerkte afbeeldingen gemaakt met de superresolutiemicroscoop die de DNA-wandelaar (groen) langs de baan laten zien (rood). Krediet:Purdue University-afbeelding / Jing Pan
De Purdue-onderzoekers hebben een DNA-loopsysteem ontworpen dat bestaat uit een enzymatische kern en twee armen. De wandelaar reist langs een koolstof-nanobuisspoor dat "versierd" is met strengen RNA. De enzymatische kern splitst segmenten van deze RNA-strengen af terwijl de wandelaar continu naar voren beweegt, binding aan en het oogsten van energie uit het RNA. De rollator beweegt in een cyclus van zes stappen die wordt herhaald zolang er RNA-brandstof is.
Een fluorescerend nanodeeltje is bevestigd aan één arm van de DNA-walker, waardoor het gloeit wanneer het wordt blootgesteld aan licht in het zichtbare deel van het spectrum. Het koolstof-nanobuisspoor fluoresceert ook wanneer het wordt blootgesteld aan licht in een deel van het nabij-infraroodspectrum. Omdat het nieuwe microscopiesysteem met superresolutie werkt in zowel het zichtbare als het nabij-infraroodspectra, het is mogelijk om het loopmechanisme te volgen.
De superresolutietechnologie stelt onderzoekers in staat structurele kenmerken op te lossen die veel kleiner zijn dan de golflengte van zichtbaar licht, wat normaal gesproken moeilijk is met conventionele microscopen vanwege de Abbe-diffractielimiet, vastgesteld door natuurkundige Ernst Abbe in 1873. De limiet is ongeveer 250 nanometer, die groot is in vergelijking met de kleine wandelaars, met een lengte van ongeveer 5 nanometer.
Als de DNA-walker wordt blootgesteld aan laserlicht, het nanodeeltje en nanobuisje knipperen willekeurig aan en uit. Deze flitsen worden vastgelegd als talrijke fluorescerende stippen in duizenden beeldframes. Deze verzameling punten wordt vervolgens gebruikt om de precieze beweging van de wandelaar te reconstrueren, die beweegt in een cyclus van zes stappen waarbij delen van de RNA-streng worden gesplitst en de energie ervan wordt geoogst voordat naar de volgende streng wordt gegaan.
Bevindingen onthulden dat drie primaire stappen dit loopmechanisme domineren.
"Dus, als je deze drie stappen binnen deze loopcyclus kunt beheersen, dan kun je deze wandelaars echt bestuderen en beter beheersen, " zei Choi. "Je kunt ze versnellen, je kunt ze laten stoppen en in verschillende richtingen bewegen."
Terwijl het voorheen 20 uur of langer zou hebben geduurd om een volledige loopcyclus te bestuderen, de nieuwe aanpak versnelt het proces tot ongeveer een minuut.
 Studie kijkt naar het leven binnen en buiten koolwaterstofsijpelingen op de zeebodem
Studie kijkt naar het leven binnen en buiten koolwaterstofsijpelingen op de zeebodem Aloe Vera Science Experiments
Aloe Vera Science Experiments  Uitbarstende vulkaan zorgt voor een opleving van het Filippijnse toerisme
Uitbarstende vulkaan zorgt voor een opleving van het Filippijnse toerisme Brandweerlieden controleren hoofdfront van bosbrand bij Athene
Brandweerlieden controleren hoofdfront van bosbrand bij Athene Opwarming kan de aankomst van toeristen in Indonesië beïnvloeden
Opwarming kan de aankomst van toeristen in Indonesië beïnvloeden
Hoofdlijnen
- Video:Op weg naar nul honger wereldwijd
- Verschil tussen triglyceriden en fosfolipiden
- Celmuursamenstelling van de zes koninkrijken
- DNA Extraction by Spooling Method
- In welke levensfase komt mitose sneller voor?
- Hoe worden bacteriën resistent tegen antibiotica?
- Waarom wordt magnesiumchloride gebruikt in PCR?
- Wat hebben alle levende organismen gemeen?
- Sommige lemuren zijn eenlingen, anderen hunkeren naar verbinding
- Baanbrekende bevindingen over de eigenschappen van daguerreotypieën

- Kleinste harde schijf tot nu toe schrijft informatie atoom voor atoom

- Directe visualisatie van kwantumstippen onthult vorm van kwantumgolffunctie
- Grafeenballon levert ongekende beelden op van gehydrateerde eiwitmoleculen
- Nanobuis fotodetector gebouwd

 Eencellige architecten inspireren nieuwe nanotechnologie
Eencellige architecten inspireren nieuwe nanotechnologie Onderzoeker bestudeert vampier zilverprik
Onderzoeker bestudeert vampier zilverprik Holografie kwantumsprong kan een revolutie teweegbrengen in beeldvorming
Holografie kwantumsprong kan een revolutie teweegbrengen in beeldvorming Biologische voedingsmiddelen verifiëren
Biologische voedingsmiddelen verifiëren Five Classes of Chordates
Five Classes of Chordates NASA-satelliet onthult vorming van Filippijnse Zee Tropische Depressie 16W
NASA-satelliet onthult vorming van Filippijnse Zee Tropische Depressie 16W Kwantumtrucs om de geheimen van topologische materialen te onthullen
Kwantumtrucs om de geheimen van topologische materialen te onthullen Kleurverandering urinetest voor kanker toont potentieel in muisstudie
Kleurverandering urinetest voor kanker toont potentieel in muisstudie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

