
Wetenschap
Nieuw hydrogel-nanoplatform dat tumoren bij muizen identificeert en verkleint
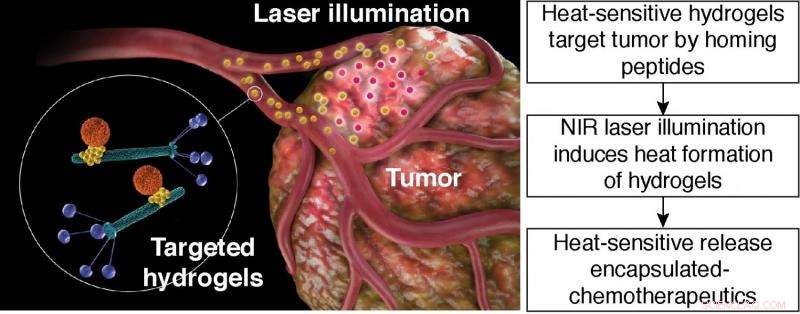
Warmtegevoelige afgifte van ingekapselde chemotherapeutica. Schematische illustratie van gerichte hydrogel fotothermische therapie. Gerichte hydrogel:oranje deeltje, op liposomen gebaseerde nanodrager; geel deeltje, Gouden nanodeeltjes; groene staven, bacteriofaagdeeltjes met peptideliganden weergegeven op het faagcoating-eiwit (blauw). Krediet:Hosoya, et al.
(Phys.org) - Gefunctionaliseerde nanodeeltjes zijn een manier om medicijnen toe te dienen voor chemotherapeutica. Echter, het is moeilijk gebleken om nanodeeltjes op de tumorplaats te krijgen. Een methode die onderzoekers hebben gebruikt om kankercellen te targeten, is het maken van hydrogels gemaakt van filamenteuze bacteriofaag (faag) en gouden nanodeeltjes. Peptide-bindende liganden kunnen worden opgenomen in het faaggedeelte van de hydrogel dat zich dan zal richten op bekende carcinoomcellen.
Een interdisciplinaire groep onderzoekers van verschillende universiteiten in Japan, de VS, en Duitsland hebben een hydrogelplatform ontwikkeld dat tumoren kan targeten, bieden niet-invasieve beeldvorming, en laat een chemotherapeutisch medicijn vrij. Ze hebben hun platform aangetoond in zowel in vitro studies als in muismodellen. Aanvullend, ze laten zien dat hun platform generaliseerbaar is naar verschillende doelen en chemotherapeutica. Hun werk verschijnt in de Proceedings van de National Academy of Sciences .
Hosoja, et al.'s hydrogelplatform bestaat uit bacteriofaag, gouden nanodeeltjes, en dragers van nanogrootte zoals liposomen of mesopoureuze silicadeeltjes. In deze instelling, faagdeeltjes zijn in staat om specifieke moleculen op de tumorcellen te herkennen. De gouden nanodeeltjes dienen als een "reporter" voor de verdeling van de hydrogel. De nanocarrier vervoert verschillende chemicaliën of farmaceutische ladingen. De nanocarrier laat lading los na een specifieke stimulus, zoals warmte.
In het huidige werk Hosoja, et al. bewees voor het eerst dat hittegevoelige liposomen (HSL's) zouden dienen als een formidabele warmtegevoelige drager. In theorie, als de HSL begint te smelten, het geeft het medicijn vrij dat erin is verwerkt. Met behulp van calceïne, een fluorescerend actief molecuul, ze stelden vast dat de HSL calceïne afgaf bij het bereiken van 40 O C, als voorspeld. Toen de HSL op een constante temperatuur (42 O C), het gaf alle calceïne binnen 10 minuten vrij. Hosoja, et al. bewees vervolgens dat deze HSL's nog steeds reageerden op veranderingen in temperatuur wanneer ze in het hydrogelplatform werden opgenomen.
De volgende stap was om aan te tonen dat de HSL-bevattende hydrogels reageerden op NIR-verwarming terwijl ze zich in een matrix bevonden. De auteurs gebruikten agarosegel als hun modelsysteem. Ze ontdekten dat de HSL-bevattende hydrogel reageerde op NIR-verwarming en naarmate het laservermogen toenam, de temperatuur van de hydrogel nam toe. Vervolgens bepaalden ze of NIR-verwarming de afgifte van doxorubicine (dox) zou veroorzaken, een chemotherapeuticum. Ze waren in staat om een "reproduceerbare en robuuste foton-dosisafhankelijke toename in fluorescentie-intensiteit" te produceren.
Om de warmteverdeling in de hydrogel van NIR te bepalen, ze gebruikten magnetische resonantie temperatuurbeeldvorming op de HSL-bevattende hydrogels op het agaroseplatform. De thermische gradiëntbeelden bevestigden dat de gecentraliseerde warmte werd geproduceerd door de hydrogel via de NIR-laser. Ze gebruikten gadolinium-ingekapselde HSL-bevattende hydrogels om te bevestigen dat geneesmiddelafgifte plaatsvond op de locatie van de laserstraal.
Hoewel deze resultaten aantonen dat de afgifte van geneesmiddelen kan worden gecontroleerd met behulp van NIR, ze moeten nog testen of het systeem zich op de kankerplaats kan richten. Om dit te doen, Hosoja, et al. namen een ligand op dat een goed ingeburgerd cyclisch peptide heeft dat aan CRKL bindt. CRKL-bindende faagdeeltjes richten zich op EF43. fgf-4 borstcarcinoom cellen. Met behulp van rhodamine-gelabelde HSL-bevattende hydrogels, ze toonden aan dat de faag zich richtte op de carcinoomcellen, wat bevestigt dat het nog steeds zijn bindende eigenschappen behoudt, zelfs wanneer het in het nanoplatform wordt opgenomen.
Vervolgens deden ze in vivo testen bij muizen. Ze volgden de locatie en effecten van hun HSL-bevattende hydrogelplatform bij muizen die EF43 hadden. fgf-4 borstcarcinoom. Optische fluorescentiebeeldvormingsstudies toonden aan dat de tumor zichtbaar was bij muizen die werden behandeld met het gerichte hydrogelsysteem in vergelijking met controles. Analyse van de tumoren na 24 uur onthulde dat gouden nanodeeltjes, gerichte faag, en HSL's bevonden zich in de tumor. Aanvullende studies om te zien of hun systeem vervolgens een chemotherapeuticum kon afgeven met behulp van NIR op de tumorplaats, bleken ook succesvol. De auteurs zagen verminderde tumorgroei bij muizen met HSL-bevattende hydrogels met dox, en bevestigden hun resultaten met behulp van wiskundige modellering.
Eindelijk, om de veelzijdigheid van hun hydrogel nanoplatform te testen, Hosoja, et al. opgenomen mesoporeuze silica nanodeeltjes (MSNP) in het hydrogelsysteem. De chemische eigenschappen van MSNP maken het mogelijk om verschillende chemotherapeutica te verpakken. Ze testten of MSNP-bevattende hydrogels FITC konden leveren in twee verschillende kankermodellen, hetzelfde borstkankermodel dat eerder werd gebruikt (EF43. fgf-4 ) en een model voor prostaatkanker. Ze vonden een gerichte binding aan de twee kankers en studies met dox toonden een afname van de tumorgrootte.
Dit werk demonstreert een hydrogelplatform dat de fysische of chemische eigenschappen van bekende nanodragersystemen zoals warmtegevoelige liposomen of mesoporeuze silica-nanodeeltjes niet verandert. Dit platform maakt targeting, warmte-geïnduceerde levering, en is zowel veelzijdig als reproduceerbaar. Met aanvullende onderzoeken, dit systeem kan een algemeen, robuuste methode voor gerichte medicijnafgifte.
© 2016 Fys.org
 Cryo-EM onthult structuur en mechanisme van de 5-HT3-receptor
Cryo-EM onthult structuur en mechanisme van de 5-HT3-receptor Kunnen we zien dat het licht wordt uitgezonden door waterstofatomen wanneer ze overgaan op een grondtoestand?
Kunnen we zien dat het licht wordt uitgezonden door waterstofatomen wanneer ze overgaan op een grondtoestand?  Rood of geel? Een eenvoudige papieren test detecteert valse of ondermaatse antibiotica
Rood of geel? Een eenvoudige papieren test detecteert valse of ondermaatse antibiotica Microfluïdisch systeem met celscheidende krachten kan ontrafelen hoe nieuwe pathogenen aanvallen
Microfluïdisch systeem met celscheidende krachten kan ontrafelen hoe nieuwe pathogenen aanvallen Doorbraak in het begrijpen van enzymen die antibiotica maken voor resistente ziekteverwekkers
Doorbraak in het begrijpen van enzymen die antibiotica maken voor resistente ziekteverwekkers
 Hittegolf Spanje breekt records en doodt er één
Hittegolf Spanje breekt records en doodt er één meer regen, minder sneeuw verhoogt de wateroverlast
meer regen, minder sneeuw verhoogt de wateroverlast Hoe openingen in het Antarctische zee-ijs het wereldwijde klimaat beïnvloeden
Hoe openingen in het Antarctische zee-ijs het wereldwijde klimaat beïnvloeden Verzuring van de oceaan veroorzaakt osteoporose van koraal op iconische riffen
Verzuring van de oceaan veroorzaakt osteoporose van koraal op iconische riffen NASA vindt een oog en een gigantische staart in tyfoon Hagupit
NASA vindt een oog en een gigantische staart in tyfoon Hagupit
Hoofdlijnen
- Wolven bleken meer coöperatief te zijn met hun eigen soort dan honden met die van hen
- Kwam Eiwit, DNA of RNA als eerste?
- Prehistorische soa's kunnen de reden zijn waarom mensen monogaam werden
- Panspermia:zorgden buitenaardse zaden ervoor dat het leven op aarde explodeerde?
- Hetzelfde gen, verschillende paringstechnieken bij vliegen
- Klasactiviteiten op het ademhalingssysteem
- Drone-foto's bieden snellere, goedkopere gegevens over de belangrijkste Antarctische soorten
- Laat me je bladeren zien - Gezondheidscontrole voor stadsbomen
- Hoe nemen we beslissingen?
- Fosforeen onthult zijn supergeleiding

- Onderzoekers fabriceren robuuste superhydrofobe films van anisotrope silicadeeltjes

- Zelfassemblerende nanokubussen voor antennes en lenzen van de volgende generatie

- Nieuw materiaal om olievlekken op te vangen?

- Nieuw algoritme kan materialen met ongebruikelijke eigenschappen ontdekken, waaronder onzichtbaarheid

 Structurele en dynamische verschillen tussen selectieve en niet-selectieve ionkanalen
Structurele en dynamische verschillen tussen selectieve en niet-selectieve ionkanalen Concept Amerikaans rapport zegt extreme stormen gedreven door klimaatverandering
Concept Amerikaans rapport zegt extreme stormen gedreven door klimaatverandering Onderzoek breidt tweetalig taalprogramma voor baby's uit
Onderzoek breidt tweetalig taalprogramma voor baby's uit Een verbinding maken:twee manieren waarop foutsegmenten hun scheiding kunnen overwinnen
Een verbinding maken:twee manieren waarop foutsegmenten hun scheiding kunnen overwinnen Bacteriën groeien in agar
Bacteriën groeien in agar  Nieuwe verklaring voor plotselinge ineenstorting van warmte in plasma's kan helpen bij het creëren van fusie-energie op aarde
Nieuwe verklaring voor plotselinge ineenstorting van warmte in plasma's kan helpen bij het creëren van fusie-energie op aarde Het combineren van werk en tertiaire studie is nu moeilijker dan in 2012, zegt studie
Het combineren van werk en tertiaire studie is nu moeilijker dan in 2012, zegt studie Gebruik je je werktelefoon buiten werktijd?
Gebruik je je werktelefoon buiten werktijd?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

