
Wetenschap
Onderzoek kan leiden tot nanosensoren die fibrinogeen herkennen, insuline, of andere biomarkers
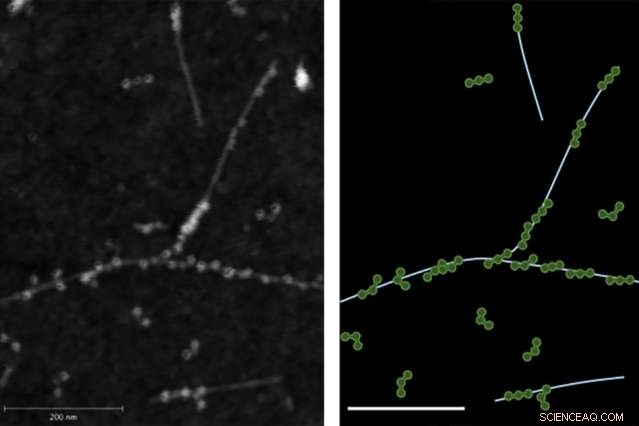
De afbeelding met atomaire krachtmicroscopie (AFM) aan de linkerkant toont de fysieke binding tussen fibrinogeeneiwitten en enkelwandige koolstofnanobuizen. Rechts is een spoor te zien van het AFM-beeld met het fibrinogeen in groen en nanobuisjes in lichtblauw.
Met behulp van koolstof nanobuisjes, Chemische ingenieurs van MIT hebben een nieuwe methode bedacht voor het detecteren van eiwitten, inclusief fibrinogeen, een van de stollingsfactoren die cruciaal zijn voor de bloedstollingscascade.
Deze aanpak, indien ontwikkeld tot een implanteerbare sensor, kan nuttig zijn voor het monitoren van patiënten die bloedverdunners gebruiken, waardoor artsen ervoor kunnen zorgen dat de medicijnen de bloedstolling niet te veel verstoren.
De nieuwe methode is de eerste die synthetische herkenningsplaatsen (vergelijkbaar met natuurlijke antilichamen) voor eiwitten creëert en deze direct koppelt aan een krachtige nanosensor zoals een koolstofnanobuisje. De onderzoekers hebben ook aanzienlijke vooruitgang geboekt op een vergelijkbare herkenningsplaats voor insuline, waardoor patiënten met diabetes beter kunnen worden gevolgd. Het kan ook mogelijk zijn om deze benadering te gebruiken om eiwitten te detecteren die geassocieerd zijn met kanker of hartziekte, zegt Michael Strano, de Carbon P. Dubbs Professor in Chemical Engineering aan het MIT.
Strano is de senior auteur van een paper waarin de methode in Nature Communications wordt beschreven. Gili Bisker, een postdoc in Strano's lab, is de hoofdauteur van de krant.
Een gerichte zoekopdracht
De nieuwe sensor is het nieuwste voorbeeld van een methode die is ontwikkeld in het laboratorium van Strano, bekend als Corona Phase Molecular Recognition (CoPhMoRe).

Dit scanning-elektronenmicroscopiebeeld toont enkelwandige koolstofnanobuizen, het door de onderzoekers gebruikte uitgangsmateriaal.
Deze techniek maakt gebruik van de interacties tussen een bepaald polymeer en een oppervlak van nanodeeltjes, zoals dat van een fluorescerende enkelwandige koolstofnanobuis, wanneer het polymeer om de nanobuis wordt gewikkeld.
Bepaalde delen van de polymeren hechten zich vast aan het oppervlak van de nanodeeltjes als ankers, terwijl andere regio's zich naar buiten uitstrekken in hun omgeving. Dit naar buiten gerichte gebied, ook bekend als de geadsorbeerde fase of corona, heeft een 3D-structuur die afhangt van de samenstelling van het polymeer.
CoPhMoRe werkt wanneer een specifiek polymeer adsorbeert aan het oppervlak van nanodeeltjes en een corona creëert die het doelmolecuul herkent. Deze interacties zijn zeer specifiek, net als de binding tussen een antilichaam en zijn doelwit. De binding van het doelwit verandert de natuurlijke fluorescentie van de koolstofnanobuisjes, waardoor de onderzoekers kunnen meten hoeveel van het doelmolecuul aanwezig is.
Het laboratorium van Strano heeft deze benadering eerder gebruikt om herkenningsplaatsen te vinden en nansensoren voor estradiol en riboflavine te ontwikkelen. onder andere moleculen. Het nieuwe artikel vertegenwoordigt hun eerste poging om corona-fasen te identificeren die eiwitten kunnen detecteren, die groter zijn, ingewikkelder, en kwetsbaarder dan de moleculen die door hun vorige sensoren werden geïdentificeerd.
Voor deze studie is Bisker begon met het screenen van koolstofnanobuisjes verpakt in 20 verschillende polymeren, waaronder DNA, RNA, en polyethyleenglycol (PEG), een polymeer dat vaak aan geneesmiddelen wordt toegevoegd om hun levensduur in de bloedbaan te verlengen.
Zelfstandig, geen van de polymeren had enige affiniteit voor de 14 geteste eiwitten, allemaal genomen uit menselijk bloed. Echter, toen de onderzoekers in polymeer verpakte nanobuisjes testten tegen dezelfde eiwitten, ze vonden een match tussen een van de gemodificeerde nanobuisjes en fibrinogeen.
"Een chemicus of bioloog zou niet van tevoren kunnen voorspellen dat er enige affiniteit zou zijn tussen fibrinogeen en deze coronafase, " zegt Strano. "Het is echt een nieuw soort moleculaire herkenning."
fibrinogeen, een van de meest voorkomende eiwitten in menselijk bloed, maakt deel uit van de bloedstollingscascade. Wanneer een bloedvat beschadigd is, een enzym genaamd trombine zet fibrinogeen om in fibrine, een vezelig eiwit dat stolsels vormt om de wond af te dichten.
Een sensor voor fibrinogeen kan artsen helpen bepalen of patiënten die bloedverdunners gebruiken nog voldoende stollingscapaciteit hebben om hen te beschermen tegen letsel, en zou artsen in staat kunnen stellen nauwkeuriger afgestemde doseringen te berekenen. Het kan ook worden gebruikt om de bloedstolling van patiënten te testen voordat ze geopereerd worden, of om wondgenezing te volgen, zegt Bisker.
Synthetische antilichamen
De onderzoekers geloven dat hun synthetische moleculaire herkenningsmiddelen een verbetering zijn ten opzichte van bestaande natuurlijke systemen op basis van antilichamen of DNA-sequenties die bekend staan als aptameren. die kwetsbaarder zijn en de neiging hebben om na verloop van tijd af te breken.
"Een van de voordelen hiervan is dat het een volledig synthetisch systeem is dat een veel langere levensduur in het lichaam kan hebben, ' zegt Bisker.
In 2013, onderzoekers in het laboratorium van Strano hebben aangetoond dat sensoren van koolstofnanobuisjes meer dan een jaar actief kunnen blijven in muizen nadat ze zijn ingebed in een polymeergel en chirurgisch onder de huid zijn geïmplanteerd.
Naast insuline, de onderzoekers zijn ook geïnteresseerd in het detecteren van troponine, een eiwit dat wordt vrijgegeven door stervende hartcellen, of het detecteren van eiwitten geassocieerd met kanker, die nuttig zou zijn voor het volgen van het succes van chemotherapie. Deze en andere eiwitsensoren kunnen cruciale componenten worden van apparaten die medicijnen afgeven als reactie op een teken van ziekte.
"Door therapeutische markers in het menselijk lichaam in realtime te meten, we kunnen medicijnafgiftesystemen mogelijk maken die veel slimmer zijn, en medicijnen vrijgeven in precieze hoeveelheden, " zegt Strano. "Echter, het meten van die biomarkers is de eerste stap."
 Ontzoutingsproces
Ontzoutingsproces  De effecten van cadmiumplateren 304 roestvrij staal
De effecten van cadmiumplateren 304 roestvrij staal  Door machinaal leren ondersteund moleculair ontwerp voor hoogwaardige organische fotovoltaïsche materialen
Door machinaal leren ondersteund moleculair ontwerp voor hoogwaardige organische fotovoltaïsche materialen Water creëert vallen in organische elektronica
Water creëert vallen in organische elektronica Het strakste niet-aminoglycoside-ligand voor de bacteriële ribosomale RNA A-site
Het strakste niet-aminoglycoside-ligand voor de bacteriële ribosomale RNA A-site
 NASA tuurt in het grote heldere oog van orkaan Walaka
NASA tuurt in het grote heldere oog van orkaan Walaka Wat zit er in de buitenste band van een orkaan?
Wat zit er in de buitenste band van een orkaan?  Klein lek gevonden van nucleaire Sovjet-onderzeeër die in 1989 zonk
Klein lek gevonden van nucleaire Sovjet-onderzeeër die in 1989 zonk Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie
Een halve graad warmer betekent 30, 000 meer doden per jaar in stedelijk China:studie Verkeersvervuiling neemt af tijdens lockdown, maar andere risico's voor de luchtkwaliteit nemen toe, onderzoekers onthullen
Verkeersvervuiling neemt af tijdens lockdown, maar andere risico's voor de luchtkwaliteit nemen toe, onderzoekers onthullen
Hoofdlijnen
- Uit een grootschalig onderzoek blijkt dat veel geplande wegen in de tropen niet gebouwd mogen worden
- Een niet-verslavende opioïde pijnstiller zonder bijwerkingen
- Ingenieurs hacken celbiologie om 3D-vormen te maken van levend weefsel
- Processen die ATP als energiebron gebruiken
- Wat is de functie van het enzym ligase bij het vormen van recombinant DNA?
- Hoe levert embryologie bewijs voor evolutie?
- Hoe verdeelt het cytoplasma zich tussen dochtercellen na mitose?
- Het bewijs zit in de voetafdruk:mensen kwamen eerder naar Amerika dan gedacht
- Onderzoekers ontdekken wat er bij libellen op het menu staat
- Rekbaar, sterk geleidende film veelbelovend voor draagbare elektronica

- Nieuwe lichtgestuurde gel maakt grote vooruitgang in zachte robotica (met video)

- Hoe ondoordringbaar is het ondoordringbare grafeen?

- Chitosan gecoat, met chemotherapie verpakte nanodeeltjes kunnen zich richten op kankerstamcellen
- Microprocessors van potloodstift

 Nieuw model voor droge bodems voor Pacific Northwest kan de gezondheid van bossen helpen veranderen in klimaat
Nieuw model voor droge bodems voor Pacific Northwest kan de gezondheid van bossen helpen veranderen in klimaat Lasers gebruiken om explosies te bestuderen
Lasers gebruiken om explosies te bestuderen Bevroren buizen, elektrische problemen blijven bestaan terwijl koude snap de grip vergemakkelijkt
Bevroren buizen, elektrische problemen blijven bestaan terwijl koude snap de grip vergemakkelijkt Moleculen opblazen met extreme röntgenstraling
Moleculen opblazen met extreme röntgenstraling Een chaos die alleen op Mars te vinden is
Een chaos die alleen op Mars te vinden is Nanosponzen nemen keer op keer olie op
Nanosponzen nemen keer op keer olie op Hulpmiddelen gebruikt door vroege ontdekkingsreizigers
Hulpmiddelen gebruikt door vroege ontdekkingsreizigers  Moleculaire verkeersopstopping zorgt ervoor dat water sneller door nanokanalen beweegt
Moleculaire verkeersopstopping zorgt ervoor dat water sneller door nanokanalen beweegt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

