
Wetenschap
Wetenschappers demonstreren verbeterde katalysatorcontrole, energiebesparing zou kunnen resulteren
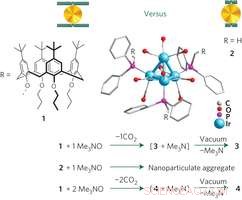
Synthese en schematisch mechanisch model van ligand-gestabiliseerde open-site clusters. Credit: Natuur Nanotechnologie
(Phys.org) —Geïnspireerd door hoe enzymen werken in de biologische processen van de natuur, onderzoekers hebben een manier aangetoond om de controle over synthetische katalysatoren te verbeteren, volgens een artikel dat mede is geschreven door een computerchemicus van de Universiteit van Alabama en dat is gepubliceerd in een recent online nummer van het tijdschrift Natuur Nanotechnologie .
"Dit werk is een opwindend voorbeeld van hoe we leren om de beheersing van chemische reacties op het niveau van een enkel atoom te verbeteren, " zei dr. David Dixon, de Robert Ramsay Chair of Chemistry aan de Universiteit van Alabama.
Katalysatoren versnellen chemische reacties waardoor ze sneller gaan en minder energie verbruiken. Schattingen geven aan dat de economische impact van katalytische verwerking, inclusief de bestrijding van vervuiling, is $ 10 biljoen per jaar, zei Dixon.
De UA-onderzoeker noemde het verbeteren van de omzetting van biomassa - meestal plantaardige materialen - in transportbrandstoffen als een voorbeeld van hoe het ontwerpen van efficiëntere katalysatoren de samenleving ten goede zou kunnen komen.
De krant, getiteld "Selectieve moleculaire herkenning door nanoschaalomgevingen in een ondersteunde iridiumclusterkatalysator, " werd op 20 april gepubliceerd in de online editie van het tijdschrift.
In het onderzoek, gesponsord door het Amerikaanse ministerie van Energie, de wetenschappers lieten zien hoe moleculaire binding - de interactie die atomen bij elkaar houdt - naar believen op specifieke locaties in de katalysator kan worden in- en uitgeschakeld. De vondst, onderzoekers zeiden, heeft potentieel ingrijpende gevolgen voor chemische omzettingen met metaalkatalysatoren.
Het onderzoeksteam omvatte Drs. Alex Katz, van de Universiteit van Californië, Berkeley, en Bruce Gates, van de Universiteit van Californië, Davy. Shengjie Zhang, een van Dixons afgestudeerde studenten, speelde een leidende rol in de computationele inspanning van het artikel, en Dr. Alexander Okrut van het Katz-laboratorium leidde de experimentele inspanning.
"Dit zal ons helpen om betere katalysatoren te ontwerpen die minder energie verbruiken en waardevolle producten te produceren met minder verspillende bijproducten. ' zei Dixon.
"Bij enzymen de katalysatoren van de natuur, het wisselen van site-reactiviteit leidt tot vruchtbare conversies terwijl andere volledig worden uitgesloten, " zei Katz. "Zo'n omschakeling op een actieve metaalplaats zorgt ervoor dat enzymen in water kunnen functioneren, bijvoorbeeld, naast vele andere prestaties, waaronder het zijn van 's werelds snelste en meest selectieve katalysatoren, die worden gebruikt om het leven in stand te houden. Nutsvoorzieningen, we zijn ook in staat om soortgelijke omschakelingen te realiseren in door de mens gemaakte katalysatoren."
"Dit biedt, "Gate voegde toe, "de belofte van groenere en goedkopere gekatalyseerde industriële processen - door te doen wat de natuur zo goed doet, behalve dat we dit nu doen in door de mens gemaakte systemen."
 Met suiker bedekte wereld
Met suiker bedekte wereld Afstemming van de elektrokatalytische prestaties van bifunctionele katalysatoren
Afstemming van de elektrokatalytische prestaties van bifunctionele katalysatoren Li-ionen transport over elektrolyten en SEI
Li-ionen transport over elektrolyten en SEI Hoogenergetisch vormgeheugenpolymeer kan op een dag robots helpen hun spieren te buigen
Hoogenergetisch vormgeheugenpolymeer kan op een dag robots helpen hun spieren te buigen Gigantische elektronische geleidbaarheidsverandering aangedreven door kunstmatige omschakeling van kristaldimensionaliteit
Gigantische elektronische geleidbaarheidsverandering aangedreven door kunstmatige omschakeling van kristaldimensionaliteit
 NASA vindt windschering nog steeds van invloed op tropische storm Saola
NASA vindt windschering nog steeds van invloed op tropische storm Saola Kleine huizen zien er prachtig uit, maar hebben een donkere kant:drie dingen die ze je niet vertellen over marketing-blurb
Kleine huizen zien er prachtig uit, maar hebben een donkere kant:drie dingen die ze je niet vertellen over marketing-blurb Wetenschappers:Chemische vervuiling is een wereldwijde bedreiging die wereldwijde actie vereist
Wetenschappers:Chemische vervuiling is een wereldwijde bedreiging die wereldwijde actie vereist Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval
Versnelde uitspoeling van radiocesium uit strooisel op de bosbodem door hevige regenval Klimaatverandering kan leiden tot grotere atmosferische rivieren
Klimaatverandering kan leiden tot grotere atmosferische rivieren
Hoofdlijnen
- Lood visgerei kan een bedreiging vormen voor de populaties van duikers
- Wat is het laatste nieuws over de darmflora? Concordia-studenten microbiologie publiceren hun bevindingen
- Onderzoekers identificeren een paar receptoren die essentieel zijn voor de communicatie tussen mannen en vrouwen bij planten
- Studie waarschuwt dat slangenschimmelziekte een wereldwijde bedreiging kan zijn
- Gentherapie biedt langdurige behandeling voor muizen met diabetes
- Waarin verschillen mensen van onze voorouders?
- Hoe werkt DNA-vertaling?
- Luiheid heeft deze menselijke voorouder misschien verdoemd
- Het verschil tussen orthologe en paralogische genen
- Van rimpels en draden:door capillariteit geïnduceerde huidplooien vormen spontaan uitgelijnde DNA-nanodraad

- Onthulling van de elektronenbeweging in een koolstofnanospoel

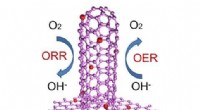
- Rationele hybridisatie van N-gedoteerde grafeen / koolstofnanobuizen voor zuurstofreductie en zuurstofontwikkelingsreactie
- Geleidingsmetingen op grafeen nanoribbons vertellen onderzoekers hoe moleculaire draden kunnen worden geoptimaliseerd

- Team pleit voor hoogwaardige koolstofnanobuisvezels voor de industrie

 De luchtkwaliteit is sinds 2016 verslechterd, geassocieerd met meer vroegtijdige sterfgevallen in de VS
De luchtkwaliteit is sinds 2016 verslechterd, geassocieerd met meer vroegtijdige sterfgevallen in de VS Onderzoekers evalueren certificeringsprogramma's als opties voor het behoud van tropische bossen
Onderzoekers evalueren certificeringsprogramma's als opties voor het behoud van tropische bossen Soorten organismen die van plantencellen zijn gemaakt
Soorten organismen die van plantencellen zijn gemaakt Waar is de meeste van de massa van een atoom gelegen?
Waar is de meeste van de massa van een atoom gelegen?  Poetin tikt firebrand aan om omstreden ruimteagentschap te leiden
Poetin tikt firebrand aan om omstreden ruimteagentschap te leiden Hoe waarschijnlijkheidsvoorspellingen worden geformuleerd, beïnvloedt hoe mensen voorspellingen doen
Hoe waarschijnlijkheidsvoorspellingen worden geformuleerd, beïnvloedt hoe mensen voorspellingen doen Afgunst verdeelt de samenleving
Afgunst verdeelt de samenleving Afbeelding:Hubble bekijkt een oogverblindende kosmische ketting
Afbeelding:Hubble bekijkt een oogverblindende kosmische ketting
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

