
Wetenschap
Kankerwetenschappers geloven dat nanodeeltjes nauwkeurig tumoren kunnen targeten, bijwerkingen vermijden
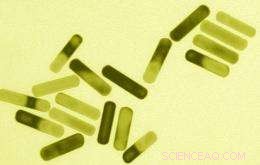
MIT-onderzoekers ontwikkelden deze gouden nanostaafjes die energie absorberen van nabij-infrarood licht en het uitstralen als warmte, kankercellen vernietigen. Afbeelding:Sangeeta Bhatia-laboratorium; MIT
In de afgelopen 40 jaar, wetenschappers hebben veel geleerd over hoe cellen kanker worden. Een deel van die kennis is vertaald naar nieuwe behandelingen, maar meestal zijn artsen gedwongen te vertrouwen op standaard chemotherapie en bestraling, die bijna net zoveel schade kunnen toebrengen aan de patiënten als aan de tumoren. Deze serie kijkt naar gerichte behandelingen die in het verschiet liggen, en wat er moet gebeuren om ze te realiseren.
doxorubicine, een medicijn dat vaak wordt gebruikt om leukemie en andere vormen van kanker te behandelen, doodt tumorcellen door hun DNA te beschadigen. Hoewel het medicijn effectief is, het kan ook giftig zijn voor hartcellen. In 2005, de FDA keurde een nieuw type doxorubicine goed, bekend als Doxil. In deze nieuwe formulering het medicijn is verpakt in een vettige laag die een liposoom wordt genoemd, die het vermogen om hartcellen (en andere gezonde cellen) binnen te dringen belemmert.
Doxil, meestal voorgeschreven voor eierstokkanker in een laat stadium, vertegenwoordigt de eerste generatie kankerbehandelingen geleverd door kleine deeltjes. Doxil-deeltjes zijn op de schaal van miljoensten van een meter, maar wetenschappers werken nu aan nanodeeltjes, die worden gemeten in miljardsten van meters. Dergelijke deeltjes zouden artsen in staat kunnen stellen grotere doses chemotherapie te geven terwijl gezond weefsel wordt gespaard van gevaarlijke bijwerkingen.
Verschillende geneesmiddelen met nanodeeltjes zijn nu in klinische proeven, en nog veel meer worden ontwikkeld in onderzoekslaboratoria. Deze deeltjes hebben een groot potentieel om de prestaties van bestaande kankermedicijnen te verbeteren, zegt arts en ingenieur Sangeeta Bhatia, de Wilson hoogleraar gezondheidswetenschappen en technologie en elektrotechniek en computerwetenschappen aan het MIT. “Chemotherapie en bestraling en chirurgie zijn wat we nu hebben, maar nanotechnologie is in opkomst als een benadering die het bestaande arsenaal aan klinische hulpmiddelen aanvult om een significante impact te hebben, ' zegt ze.
Liposomen werden ongeveer 50 jaar geleden voor het eerst ontdekt, maar meer recentelijk wetenschappers hebben zich gerealiseerd dat grote synthetische moleculen (polymeren) zoals polyethyleenglycol (PEG) niet-toxisch kunnen zijn en geen immuunrespons opwekken. PIN, die bestaat uit een lange keten van herhalende eenheden die ethers worden genoemd, kan worden gehecht aan afbreekbare polymeren om kleine, geneesmiddelafgevende deeltjes. Die deeltjes zijn opmerkelijk stabiel en kunnen medicijnen beschermen tegen het lichaamseigen immuunsysteem, die hen anders zouden kunnen vernietigen voordat ze hun bestemming bereiken. Ongeveer 15 jaar geleden, wetenschappers onder leiding van MIT's Institute Professor Robert Langer ontdekten dat PEG zich ook leent voor chemische manipulatie, waardoor wetenschappers op maat gemaakte medicijnafgiftedeeltjes kunnen maken.
"Naarmate de nanowetenschap begon te evolueren en we bedreven werden in het maken van onze eigen nanodeeltjes, we hebben manieren gevonden om nanodeeltjes specifiek te ontwerpen, zodat ze eigenschappen hadden die we wilden, " zegt Paula Hammond, de Bayer Professor of Chemical Engineering en lid van het David H. Koch Institute for Integrative Cancer Research aan het MIT. Bijvoorbeeld, wetenschappers kunnen deeltjes ontwerpen om hun medicijnlading te ontladen wanneer ze zure zakken in een tumorcel tegenkomen.
Wetenschappers kunnen zich ook specifiek richten op nanodeeltjes om tumorcellen aan te vallen. Er zijn twee manieren om dat te doen:een passieve en een actieve. In 1980, wetenschappers realiseerden zich dat de bloedvaten rond tumoren kleine gaatjes hebben, tot 500 nanometer in diameter, waardoor kleine deeltjes uit de bloedbaan in de vloeistof rond de tumor kunnen stromen.
Terwijl die passieve targeting nanodeeltjes op de juiste plaats brengt, de deeltjes spoelen weg na ongeveer 12 tot 24 uur, zegt Hammond. “Als je wilt dat de chemotherapie dichter bij zijn doel komt, dan moet je iets doen om ervoor te zorgen dat de kankercel het opneemt, ' zegt ze.
Daartoe, zij en Bhatia werken aan nieuwe manieren om nanodeeltjes actief te targeten door ze te versieren met moleculen die zich binden aan eiwitten die in grote hoeveelheden op tumorcellen worden aangetroffen. Bijvoorbeeld, ze kunnen eiwitten hechten die zich binden aan folaatreceptoren, die zich in hoge dichtheid op kankercellen bevinden omdat de cellen grote hoeveelheden folaat nodig hebben om nieuw DNA te produceren terwijl ze zich delen. Echter, folaatreceptoren worden ook gevonden op gezonde cellen, in kleinere aantallen, dus er is nog steeds een kans op ongewenste bijwerkingen.
Om dat obstakel te helpen overwinnen, een medewerker van Bhatia's, Erkki Ruoslahti aan de Universiteit van Californië in Santa Barbara, heeft een nieuwe manier ontwikkeld om bibliotheken van eiwitten te screenen om degenen te identificeren die zich uitsluitend aan tumorcellen zullen binden. Deze aanpak heeft honderden nieuwe kandidaten opgeleverd, zegt Bhatia, die ook lid is van het Koch Institute en het Howard Hughes Medical Institute.
Veel toepassingen voor nanodeeltjes
Andere nanotechnologische benaderingen van kanker maken gebruik van de unieke fysische eigenschappen van sommige nanodeeltjes. Bijvoorbeeld, gouden nanodeeltjes absorberen verschillende frequenties van licht, afhankelijk van hun vorm. Staafvormige deeltjes absorberen nabij-infrarood licht, die door de huid kunnen gaan. Vorig jaar, Bhatia en een van haar studenten, Geoffrey van Maltzahn, toonden aan dat ze gouden nanostaafjes in muizen konden injecteren, en dat dergelijke nanostaafjes zich zouden ophopen op tumorplaatsen. Toen de nanostaafjes eenmaal in de tumoren waren, de onderzoekers verwarmden ze met nabij-infrarood licht, het verhogen van de temperatuur tot 70 graden C, heet genoeg om de tumorcellen te doden zonder nabijgelegen gezond weefsel te beschadigen. De techniek kan ook worden gebruikt om tumorcellen in beeld te brengen.
Een andere veelbelovende toepassing voor nanodeeltjes is het leveren van RNA-interferentie - kleine RNA-strengen die kunnen voorkomen dat cellen de eiwitten produceren die worden gecodeerd door kankergenen. Voortbouwend op dat idee, Hammond werkt nu aan nanodeeltjes die een een-tweetje zouden opleveren, afwisselende lagen van RNA en chemotherapiemedicijnen.
Tot dusver, Doxil is een van de slechts twee geneesmiddelen tegen liposomale kanker die nu in de Verenigde Staten zijn goedgekeurd, maar andere medicijnen die door nanodeeltjes worden afgeleverd, bevinden zich nu in klinische onderzoeken. Klinische proeven zullen naar verwachting binnenkort beginnen voor nanodeeltjes die zijn ontwikkeld door Langer, een lid van het Koch Instituut, Harvard Medical School universitair hoofddocent Omid Farokhzad en anderen. Deze nanodeeltjes zullen het chemotherapiemedicijn docetaxel afleveren aan prostaatkankerpatiënten. In dierstudies, de deeltjes vertoonden een 20-voudige toename van de concentratie op de tumorplaats met minimale bijwerkingen.
Zoals bij elk nieuw type medische behandeling, onderzoekers beoordelen ook veiligheidsrisico's. In de laatste paar jaren, een nieuw gebied van nanotoxicologie is ontstaan om eventuele risico's van nanodeeltjes voor mensen te onderzoeken. Op nanoschaal is materialen nemen vaak nieuwe eigenschappen aan - bijvoorbeeld nanodeeltjes hebben een veel hogere oppervlakte-tot-volumeverhouding dan grotere deeltjes, wat belangrijk is omdat de meeste van hun activiteit aan de oppervlakte plaatsvindt, zegt Vladimir Torchilin, directeur van het Centrum voor Farmaceutische Biotechnologie en Nanogeneeskunde aan de Northeastern University.
Echter, hij zegt, klinische proeven moeten uitwijzen of een bepaald nanodeeltje veilig of gevaarlijk is, net als bij traditionele medicijnen. “Tot nu toe, het is best moeilijk om te zeggen, vooraf, daarom kan het gevaarlijk zijn, dat of dat, " zegt Torchilin, die nanodeeltjes ontwikkelt voor de behandeling van kanker.
In 2007, een FDA-taskforce op nanotechnologie adviseerde dat het agentschap nieuwe richtlijnen zou vormen om te bepalen hoe nanotechnologieproducten moeten worden gereguleerd. Ondertussen, klinische proeven met nanodeeltjes verlopen zoals elke klinische proef met geneesmiddelen. PIN, dat het hoofdbestanddeel is van veel nanodeeltjes die medicijnen afleveren, behoort tot de FDA-categorie van stoffen die "algemeen als veilig worden erkend".
Hammond is optimistisch dat nanotechnologie kankerpatiënten zal helpen, mogelijk binnen de komende drie tot vijf jaar. “Ik denk dat het ons veel te veel voordelen biedt om er afstand van te doen, ' zegt ze.
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Ideeën voor onderzoekspapieren over het smelten van ijs de Fastest
Ideeën voor onderzoekspapieren over het smelten van ijs de Fastest Meerlagige fabricage op wafelschaal van micro-elektronica op basis van zijdefibroïne
Meerlagige fabricage op wafelschaal van micro-elektronica op basis van zijdefibroïne Boomresten omzetten in slimme hydrogels
Boomresten omzetten in slimme hydrogels Hoe zuren zich gedragen in de ultrakoude interstellaire ruimte
Hoe zuren zich gedragen in de ultrakoude interstellaire ruimte Onderzoekers maken binnenlandse hoogwaardige bipolaire membranen mogelijk
Onderzoekers maken binnenlandse hoogwaardige bipolaire membranen mogelijk
 Tien jaar na de enorme olieramp in de VS, angst voor offshore boren blijft bestaan
Tien jaar na de enorme olieramp in de VS, angst voor offshore boren blijft bestaan UA-voorspelling:orkaanactiviteit onder het gemiddelde
UA-voorspelling:orkaanactiviteit onder het gemiddelde Regen heeft het droge verzacht, maar er is meer nodig om de droogte te doorbreken
Regen heeft het droge verzacht, maar er is meer nodig om de droogte te doorbreken Nieuw onderzoek biedt oplossing voor de Dust Bowl-paradox
Nieuw onderzoek biedt oplossing voor de Dust Bowl-paradox Onderzoek vindt dat transformatiefouten een actieve rol spelen bij het vormgeven van oceaanbodems
Onderzoek vindt dat transformatiefouten een actieve rol spelen bij het vormgeven van oceaanbodems
Hoofdlijnen
- Ingenieurs hacken celbiologie om 3D-vormen te maken van levend weefsel
- Hoe soorten versteend hout te identificeren
- Tientallen nieuwe natuurcorridors geïdentificeerd voor Afrikaanse zoogdieren
- Is er een zaak tegen geluk?
- Geofysicus vindt leermogelijkheden in filmfouten
- Mieren offeren hun koloniegenoten op als onderdeel van een dodelijke desinfectie
- Waar ontwikkelt een Zygote in planten zich in?
- Hoe geel en blauw groen maken bij papegaaien
- Verschil tussen Homozygoot en Heterozygoot
- Onderzoekers gebruiken elektronenmicroscoop om te onthullen hoe halfgeleider nanodraden groeien

- Flexibele piëzo-elektrische akoestische sensoren voor luidsprekerherkenning
- NRL behaalt hoogste nullastspanning voor quantum dot-zonnecellen

- Onderzoekers bedenken zijwaartse benadering van 2D-hybride

- AD gelegeerde nanoantennes voor temperatuur-feedback identificatie van virussen en explosieven
 Chemici brachten gevouwen eiwitten tot leven
Chemici brachten gevouwen eiwitten tot leven Nieuwe toepassing van blauw licht ziet door vuur
Nieuwe toepassing van blauw licht ziet door vuur Voorbij Netflix:Disney Plus voegt zich bij de streamingstrijd
Voorbij Netflix:Disney Plus voegt zich bij de streamingstrijd VN zegt dat de wereld stikt in plastic terwijl de milieucrisis groeit
VN zegt dat de wereld stikt in plastic terwijl de milieucrisis groeit Test voor halogeen
Test voor halogeen  Wetenschapsprojecten met azijn- en eierstokken
Wetenschapsprojecten met azijn- en eierstokken  Onderzoekers ontwikkelen microbellenwasser om gevaarlijke biofilms te vernietigen
Onderzoekers ontwikkelen microbellenwasser om gevaarlijke biofilms te vernietigen De uitvoer van een kwantumcomputer verifiëren door deze te vergelijken met de uitvoer van een andere kwantumcomputer
De uitvoer van een kwantumcomputer verifiëren door deze te vergelijken met de uitvoer van een andere kwantumcomputer
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

