
Wetenschap
Hoe zuren zich gedragen in de ultrakoude interstellaire ruimte

Het team van Cluster of Excellence Resolv heeft chemie in de interstellaire ruimte onderzocht. Tegoed: RUB, Lehrstuhl für Astrophysik
Een onderzoeksgroep van de Ruhr-Universität Bochum heeft onderzocht hoe zuren bij extreem lage temperaturen interageren met watermoleculen. Met behulp van spectroscopische analyses en computersimulaties, ze onderzochten de vraag of zoutzuur (HCl) zijn proton wel of niet afgeeft in omstandigheden zoals die in de interstellaire ruimte worden aangetroffen. Het antwoord hangt af van de volgorde waarin de water- en zoutzuurmoleculen samenkomen.
De groep onder leiding van professor Martina Havenith, Leerstoel Fysische Chemie II, en professor Dominik Marx, Leerstoel Theoretische Chemie, van Ruhr-Universität Bochum, samen met het team onder leiding van dr. Britta Redlich van de Radboud Universiteit, Nijmegen, beschrijft de resultaten in het tijdschrift wetenschappelijke vooruitgang , vooraf online gepubliceerd op 7 juni 2019.
Begrijpen hoe complexe moleculen werden gevormd
Als zoutzuur onder normale omstandigheden in contact komt met watermoleculen, zoals bij kamertemperatuur, het zuur dissocieert onmiddellijk, het vrijgeven van zijn proton (H+); één chloride-ion (Cl-) blijft. Het onderzoeksteam wilde weten of hetzelfde proces ook plaatsvindt bij extreem lage temperaturen onder de 10 Kelvin, d.w.z., onder min 263,15 graden Celsius. "We zouden graag willen weten of dezelfde zuur-alkalichemie zoals we die op aarde kennen ook bestaat in de extreme omstandigheden in de interstellaire ruimte, " legt Martina Havenith uit, spreker voor de Cluster of Excellence Resolv. "De resultaten zijn cruciaal om te begrijpen hoe complexere chemische moleculen in de ruimte werden gevormd - lang voordat de eerste voorlopers van het leven ontstonden."
Om de extreem lage temperaturen in het laboratorium na te bootsen, de onderzoekers voerden de chemische reacties uit in een druppel supervloeibaar helium. Ze bewaakten de processen met behulp van een speciaal type infraroodspectroscopie, die moleculaire trillingen met lage frequenties kan detecteren. Hiervoor gebruikten de onderzoekers een laser met een bijzonder hoge lichtsterkte in Nijmegen. Computersimulaties stelden de wetenschappers in staat de experimentele resultaten te interpreteren.
Eerst, de onderzoekers voegden vier watermoleculen toe, de een na de ander, aan het zoutzuurmolecuul. Het zoutzuur dissocieerde tijdens dit proces, het doneren van zijn proton aan een watermolecuul, resulterend in een hydroniumion. Het resterende chloride-ion, het hydroniumion en de drie andere watermoleculen vormden een cluster.
Echter, als de onderzoekers eerst een ijsachtige cluster van de vier watermoleculen maakten en vervolgens het zoutzuur toevoegden, ze gaven een ander resultaat:het zoutzuurmolecuul dissocieerde niet; het proton bleef gebonden aan het chloride-ion.
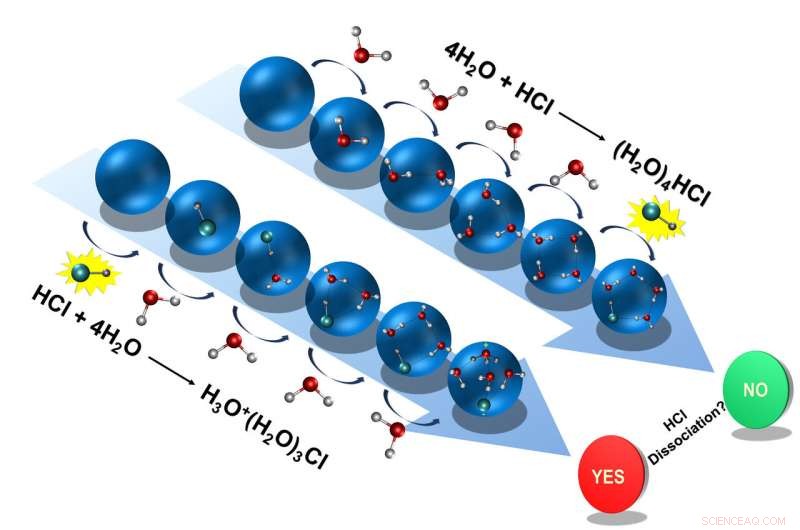
De twee mogelijke routes die zoutzuur kan volgen in omstandigheden zoals die in de interstellaire ruimte:Dissociëren of absorberen in ijskoud water. Krediet:D. Manic
"Onder de omstandigheden die kunnen worden gevonden in de interstellaire ruimte, de zuren kunnen dus dissociëren, maar dit hoeft niet per se te gebeuren - beide processen zijn twee kanten van dezelfde medaille, bij wijze van spreken, ’ zegt Martina Havenith.
Chemie in de ruimte is niet eenvoudig
De onderzoekers gingen ervan uit dat het resultaat ook toepasbaar is op andere zuren, omdat het het basisprincipe van de chemie onder ultrakoude omstandigheden vertegenwoordigt.
"Chemie in de ruimte is geenszins eenvoudig; het kan zelfs complexer zijn dan chemie onder planetaire omstandigheden, " zegt Dominik Marx. Immers, het hangt niet alleen af van de mengverhoudingen van de reagerende stoffen, maar ook van de volgorde waarin ze aan elkaar worden toegevoegd. "Met dit fenomeen moet rekening worden gehouden in toekomstige experimenten en simulaties onder ultrakoude omstandigheden, ", zegt de onderzoeker.
 Nieuwe op palladium gebaseerde initiatiesystemen voor C1-polymerisatie van diazoacetaten
Nieuwe op palladium gebaseerde initiatiesystemen voor C1-polymerisatie van diazoacetaten Moleculen maken die fonkelen
Moleculen maken die fonkelen Het opruwen van een platina-elektrode
Het opruwen van een platina-elektrode Collageenvezels groeien als een zonnebloem
Collageenvezels groeien als een zonnebloem Wetenschappers bevestigen verschillende regio's in het populaire oplosmiddel voor het opvangen en synthetiseren van koolstof
Wetenschappers bevestigen verschillende regio's in het populaire oplosmiddel voor het opvangen en synthetiseren van koolstof
 De toekomst van fracking vereist een sociale licentie
De toekomst van fracking vereist een sociale licentie Nog twee doden door record zware regen in Japan
Nog twee doden door record zware regen in Japan Nieuw hulpmiddel om de optische hygroscopiciteit van aerosolen te meten
Nieuw hulpmiddel om de optische hygroscopiciteit van aerosolen te meten Vier terug te schalen Amerikaanse monumenten bevatten artefacten, belangrijke habitat
Vier terug te schalen Amerikaanse monumenten bevatten artefacten, belangrijke habitat Mysterieuze geomagnetische spike 3, 000 jaar geleden stelt ons begrip van het binnenste van de aarde op de proef
Mysterieuze geomagnetische spike 3, 000 jaar geleden stelt ons begrip van het binnenste van de aarde op de proef
Hoofdlijnen
- Menselijke resten gevonden in grote Australische krokodil
- Verschillen tussen Protista & Monera
- 7 soorten bindweefsel
- Kunstmatige selectie (selectieve fokkerij): definitie & voorbeelden
- Hoe wordt water gevormd tijdens cellulaire ademhaling?
- Wat zijn de vier belangrijkste methoden voor het produceren van ATP?
- Herintroductie van inheemse zoogdieren helpt dorre landschappen te herstellen
- Nieuwe vissoorten vertonen opvallend kleurverschil tussen mannetjes en vrouwtjes
- Eerste levensvormen op aarde onthuld in hete lente
- De effecten van cadmiumplateren 304 roestvrij staal

- Een beter duurzaam maandverband

- Nieuwe synthetische eiwitten wedijveren met hun natuurlijke tegenhangers in protonentransport

- Onderzoekers realiseren de ideale elektronische structuur van kagome-metaal

- Wetenschappers maken waterfiltratiemembranen die zichzelf kunnen reinigen

 Rapport belicht de gevaren van de digitale gig-economie
Rapport belicht de gevaren van de digitale gig-economie Studie richt zich op de bron van arseen in diepe putten van Bengalen Basins
Studie richt zich op de bron van arseen in diepe putten van Bengalen Basins Een onmerkbare dunnefilmsensor om beweging en tastzin vast te leggen
Een onmerkbare dunnefilmsensor om beweging en tastzin vast te leggen Onderzoekers ontdekken belangrijke aanwijzingen over de geschiedenis van het zonnestelsel
Onderzoekers ontdekken belangrijke aanwijzingen over de geschiedenis van het zonnestelsel err http://u1.0
err http://u1.0 Nieuw poreus materiaal veelbelovend voor het maken van duurzame energie uit water
Nieuw poreus materiaal veelbelovend voor het maken van duurzame energie uit water Beperkingen van modellen in Science
Beperkingen van modellen in Science 2040:Hoop en actie in de klimaatcrisis
2040:Hoop en actie in de klimaatcrisis
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

