
Wetenschap
Circulatie van water in het diepe binnenste van de aarde

Water wordt naar het diepe binnenste van de aarde getransporteerd door dichte waterhoudende magnesiumsilicaten (DHMS's). Krediet:Ehime University
Fase H is een waterhoudend mineraal dat wordt beschouwd als een belangrijke drager van water naar de diepe aarde. We hebben de dissociatieconditie van fase H bepaald door een theoretische berekening op basis van kwantummechanica. Fase H ontleedt bij ongeveer 60 GPa bij 1000 K. Dit geeft aan dat het transport van water door fase H op een diepte van ongeveer 1 kan worden beëindigd. 500 km in het midden van de lagere mantel.
Het bestaan van water in de diepe aarde wordt beschouwd als een belangrijke rol in de geodynamica, omdat water de fysieke eigenschappen van mantelgesteente drastisch verandert, zoals smelttemperatuur, elektrische geleidbaarheid, en reologische eigenschappen. Water wordt diep in de aarde getransporteerd door de waterhoudende mineralen in de zinkende koude platen. waterhoudende mineralen, zoals serpentijn, mica en kleimineralen, bevatten H 2 O in de vorm van hydroxyl (-OH) in de kristalstructuur. De meeste waterhoudende mineralen vallen uiteen in watervrije mineralen en water (H 2 O) wanneer ze naar de diepe aarde worden getransporteerd, op 40-100 km diepte, vanwege de hoge temperatuur en drukomstandigheden.
Echter, er is ook gemeld dat sommige waterhoudende mineralen, zogenaamde dichte waterhoudende magnesiumsilicaten (DHMS's), kan overleven in het diepere deel van het binnenste van de aarde als de subductieplaat aanzienlijk kouder is dan de omringende mantel. DHMS is een reeks waterhoudende mineralen die een hoge stabiliteit hebben onder de druk van het diepe binnenste van de aarde. DHMS wordt ook wel "alfabetfasen" genoemd:fase A, fase B, fase D, enzovoort.
Tot voor kort fase D (chemische samenstelling:MgSi 2 O 6 H 2 ) stond bekend als de fase met de hoogste druk van DHMS's. Echter, Tsuchiya 2013 voerde eerste principes berekening uit (een theoretische berekeningsmethode gebaseerd op kwantummechanica) om de stabiliteit van fase D onder druk te onderzoeken en ontdekte dat deze fase transformeert naar een nieuwe fase met een chemische samenstelling van MgSiO 4 H 2 (plus stishoviet, een hogedrukvorm van SiO 2 , als het systeem dezelfde chemische samenstelling behoudt) boven 40 GPa (GPa=109 Pa). Deze voorspelde fase is experimenteel bevestigd door Nishi et al. 2014 en genoemd als "fase H" (Figuur 1). De theoretische berekening door Tsuchiya 2013 suggereert ook dat fase H uiteindelijk ontleedt in het watervrije mineraal MgSiO 3 door H . los te laten 2 O door verdere compressie.
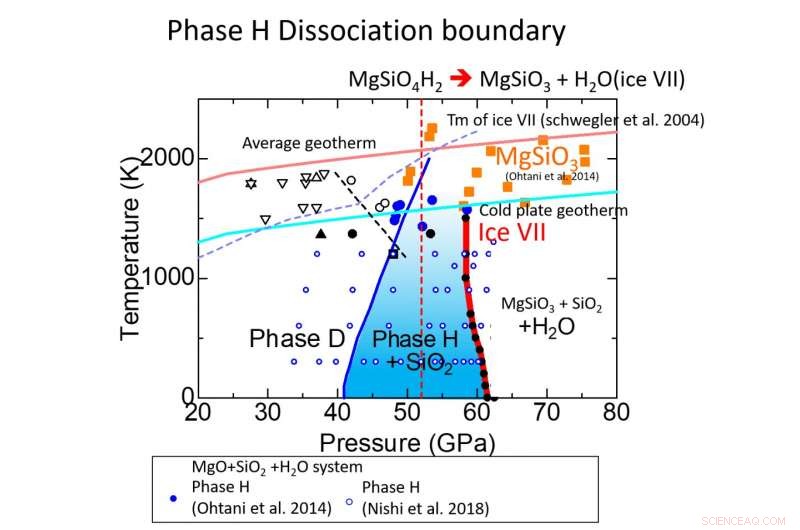
De dikke rode lijn geeft de berekende dissociatiefasegrens van fase H aan. Ehime University
Hoewel de theoretische berekening de ontledingsdruk van fase H rond het midden van de onderste mantel schatte (van 660 km tot 2900 km diepte), een gedetailleerde bepaling is nog niet bereikt, omdat de schatting van de Gibbs vrije energie van H 2 O was nodig om de ontledingsdruk van fase H te bepalen. De Gibbs-vrije energie is een thermodynamisch potentieel dat de stabiliteit van een systeem kan bepalen. Bij lagere mantelomstandigheden, de H 2 O-fase heeft een kristalstructuur met ongeordende waterstofposities, d.w.z. waterstofposities zijn statistisch verdeeld over verschillende posities. Om de ongeordende toestand van waterstof te berekenen, Tsuchiya en Umemoto 2019 berekenden verschillende waterstofposities en schatten de Gibbs-vrije energie van H 2 O met behulp van een techniek gebaseerd op statistische mechanica.
Als resultaat, ze schatten de ontledingsdruk van fase H op ongeveer 62 GPa bij 1000 K, overeenkomend met de ~ 1500 km diepte (Figuur 2). Dit resultaat geeft aan dat het transport van water door een subductieplaat eindigt in het midden van de onderste mantel in het Mg-Si-O-systeem. Tsuchiya en Umemoto 2019 suggereerden ook dat superionisch ijs kan worden gestabiliseerd door de ontleding van fase H in de subductieplaat. In superionisch ijs, zuurstofatomen kristalliseren op roosterpunten, terwijl waterstofatomen vrij mobiel zijn. De chemische reacties tussen superionisch ijs en omringende mineralen zijn nog niet geïdentificeerd, maar hoge diffusiviteit van waterstof in superionisch ijs kan snellere reacties veroorzaken dan die in vast ijs, maar anders dan water, de vloeibare fase van H 2 O.
 Bomen en gazons verslaan de hitte
Bomen en gazons verslaan de hitte Studie toont nieuw wereldwijd bewijs van de rol van mensen, verstedelijking in snelle evolutie
Studie toont nieuw wereldwijd bewijs van de rol van mensen, verstedelijking in snelle evolutie De wetenschap van droogte is complex, maar de boodschap over klimaatverandering is duidelijk
De wetenschap van droogte is complex, maar de boodschap over klimaatverandering is duidelijk Australiër breekt wereldrecord met Everest-top
Australiër breekt wereldrecord met Everest-top Nieuw systeem belooft een snellere en nauwkeurigere voorspelling van regenval
Nieuw systeem belooft een snellere en nauwkeurigere voorspelling van regenval
Hoofdlijnen
- Het is wiskundig onmogelijk om veroudering te verslaan, wetenschappers zeggen:
- Wat zijn de leefgebieden van de zes koninkrijken?
- Een vogel in de bush is $223 waard, 851 in de hand
- Een konijn ontleden
- Cellen geprogrammeerd als computers om ziekten te bestrijden
- Structurele niveaus van organisatie van het menselijk lichaam
- Hoge opbrengst, eiwit met sojabonengen
- Waarom planten spruiten vormen in het donker
- Dennen kappen:eerder vroeger dan later doen is beter voor fynbos
- Het Great Barrier Reef heeft de helft van zijn koralen verloren

- Meer voorspelde zeespiegelstijging voor elke vertraging in piekemissies

- Project gebruikt drones om de gezondheid van de Amazone te bewaken

- Pulsen van zinkende koolstof die de diepzee bereiken, worden niet vastgelegd in wereldwijde klimaatmodellen

- NASA ziet Systeem 91P samenkomen ten oosten van Queensland

 Sensing voor augmented en virtual reality en voor geavanceerde productie
Sensing voor augmented en virtual reality en voor geavanceerde productie Hoe nanogrammen naar milligrammen om te zetten
Hoe nanogrammen naar milligrammen om te zetten  Laat me de cadeaubonnen zien! Beloningstypen hebben invloed op de effectiviteit van wellnessprogramma's
Laat me de cadeaubonnen zien! Beloningstypen hebben invloed op de effectiviteit van wellnessprogramma's Grootste politiemacht in de VS stapt het dronetijdperk in
Grootste politiemacht in de VS stapt het dronetijdperk in De nieuwe Apple Watch is een legit Medical Device - maar er is een vangst
De nieuwe Apple Watch is een legit Medical Device - maar er is een vangst  Is er CO2-uitstoot van aardgas?
Is er CO2-uitstoot van aardgas?  Hoe oplosbaarheid te berekenen op basis van KSP
Hoe oplosbaarheid te berekenen op basis van KSP  Boomzaden identificeren met afbeeldingen
Boomzaden identificeren met afbeeldingen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

