
Wetenschap
Hoe fosfaat- en bicarbonaatbuffers ons lichaam in balans houden
Door Marie‑Luise Blue, bijgewerkt op 24 maart 2022
Wat is pH?
De pH-schaal kwantificeert de zuurgraad of alkaliteit van een oplossing door de logaritme van de waterstofionenconcentratie te meten. Een hogere concentratie H⁺-ionen verlaagt de pH, terwijl een lagere concentratie deze verhoogt. Op een schaal van 0 tot 14 duidt een pH van 7 op neutraliteit, waarden onder de 7 zijn zuur en waarden boven de 7 zijn alkalisch.
Hoe buffers werken
Buffers stabiliseren de pH door een zwak zuur en zijn geconjugeerde zwakke base in evenwicht te brengen. Wanneer overtollige H⁺-ionen verschijnen, sekwestreert de zwakke base ze, zet ze om in de zure vorm en handhaaft de pH. Omgekeerd, wanneer een base wordt toegevoegd, doneert het zwakke zuur H⁺-ionen, waardoor het terugkeert naar neutraliteit.
Het fosfaatbuffersysteem
In de cellen houdt de fosfaatbuffer, bestaande uit diwaterstoffosfaat (H₂PO₄⁻) en waterstoffosfaat (HPO₄²⁻), de intracellulaire pH dichtbij fysiologische waarden. Met een dissociatieconstante (pKa) van 7,21 komt het evenwicht van dit paar nauw overeen met de typische cytosolische pH van 7,2–7,4, waardoor het zeer effectief is voor intracellulaire homeostase (standaard biochemische referenties).
Als het fosfaatbuffersysteem onvoldoende is
In de bloedsomloop kunnen de beperkte concentraties diwaterstof en waterstoffosfaat het bloed niet effectief bufferen. Hier zorgt de bicarbonaatbuffer, gevormd uit opgelost CO₂ als bicarbonaat (HCO₃⁻) en koolzuur (H₂CO₃), ervoor dat de pH van het bloed op ongeveer 7,4 blijft. Door uitademing van CO₂ via de luchtwegen wordt overtollig koolzuur verwijderd, waardoor het bicarbonaatsysteem efficiënt kan werken.
 Wat gebeurt er als een base wordt toegevoegd aan een bufferoplossing?
Wat gebeurt er als een base wordt toegevoegd aan een bufferoplossing?  Waterstofopslagreacties vertonen een complexe dans naar snellere opname
Waterstofopslagreacties vertonen een complexe dans naar snellere opname De lagen waardoor de ademhalingsgassen diffunderen, staan bekend als de?
De lagen waardoor de ademhalingsgassen diffunderen, staan bekend als de?  Nieuw celmembraanmodel kan de sleutel zijn tot het ontdekken van nieuwe eiwiteigenschappen
Nieuw celmembraanmodel kan de sleutel zijn tot het ontdekken van nieuwe eiwiteigenschappen Is een zuur met de molariteit van 0,0094 zwak of sterk en zou het schadelijk zijn?
Is een zuur met de molariteit van 0,0094 zwak of sterk en zou het schadelijk zijn?
 Kustduinen trekken zich terug naarmate de zeespiegel stijgt. Uit onderzoek blijkt dat de snelheid van de veranderingen steeds sneller gaat
Kustduinen trekken zich terug naarmate de zeespiegel stijgt. Uit onderzoek blijkt dat de snelheid van de veranderingen steeds sneller gaat  Hoe brandganzen hun trekgewoonten aanpassen in het licht van de klimaatverandering
Hoe brandganzen hun trekgewoonten aanpassen in het licht van de klimaatverandering  Tribale stem verwerpt plannen voor ondergrondse opslag van radioactief afval nabij Lake Huron
Tribale stem verwerpt plannen voor ondergrondse opslag van radioactief afval nabij Lake Huron Onderzoek toont aan dat het opvoeren van koolstofafvang de sleutel kan zijn tot het verminderen van klimaatverandering
Onderzoek toont aan dat het opvoeren van koolstofafvang de sleutel kan zijn tot het verminderen van klimaatverandering Luchtvervuiling terugdringen
Luchtvervuiling terugdringen
Hoofdlijnen
- Difference Between Mutation & Genetic Drift
- Vluchtpatronen onthullen hoe muggen gastheren vinden om dodelijke ziekten over te brengen
- Wereldwijde explosie van wegenbouw kan rampzalig zijn voor mens en natuur, zeggen wetenschappers
- In welk systeem helpt merg bij de productie van rode bloedcellen en sommige witte cellen?
- De componenten van een organisme begrijpen:cellen, weefsels en organen
- Wat is celcompartimentering en waarom gebeurt het?
- Knuckle Cracking:wat de wetenschap zegt over de impact ervan op de gezondheid
- Hoe onthult vorm en functie identiteit (wetenschap)?
- Wat is een Hyocaust -systeem?
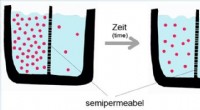
- Diffusie begrijpen:hoe moleculen van hoge naar lage concentratie gaan
- Cement, zout en water:een nieuw opslagmateriaal voor groene warmte

- De opkomst, val en heropleving van gentherapie

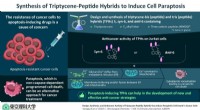
- Geprogrammeerde celdood in kankercellen:weerstand overwinnen door paraptose-inducerende verbindingen
- Aanpassingen aan niet-fullereen acceptor voor kleine moleculen in organische dunne film voor zonnecellen verbeteren de efficiëntie

 Grondwatervoorraden in Afrika bestand tegen klimaatverandering
Grondwatervoorraden in Afrika bestand tegen klimaatverandering Verschillende ruimtesondes en hun missie?
Verschillende ruimtesondes en hun missie?  Hoe gevormd zijn orgels?
Hoe gevormd zijn orgels?  Een ruimteschip heeft een momentum van 20000 kg-ms links en massa 500 kg. Wat is magnitude zijn snelheid?
Een ruimteschip heeft een momentum van 20000 kg-ms links en massa 500 kg. Wat is magnitude zijn snelheid?  Vervormde meteorenregens treffen de aarde vanuit alle hoeken
Vervormde meteorenregens treffen de aarde vanuit alle hoeken Welke landvormen vormen windenerosie en depositie in woestijnen?
Welke landvormen vormen windenerosie en depositie in woestijnen?  Samenwerkende wetenschappers bieden inzichten over het verbeteren van de blauwe OLED-prestaties voor beeldschermen en verlichting
Samenwerkende wetenschappers bieden inzichten over het verbeteren van de blauwe OLED-prestaties voor beeldschermen en verlichting  Wanneer de informatie uit DNA wordt doorgegeven aan RNA dit proces?
Wanneer de informatie uit DNA wordt doorgegeven aan RNA dit proces?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

