
Wetenschap
Hoe materie overgaat tussen vast, vloeibaar en gas:de wetenschap van faseveranderingen
Door John Papiewski | Bijgewerkt op 24 maart 2022
Elk materiaal op aarde ondergaat voorspelbare faseveranderingen naarmate temperatuur en druk variëren. De kern van deze transities is het evenwicht tussen thermische energie en intermoleculaire krachten. Wanneer warmte voldoende energie levert om deze krachten te overwinnen, beweegt een substantie van vast naar vloeibaar naar gas, waarbij elke toestand verschillende fysieke eigenschappen vertoont.
Faseovergang
In wetenschappelijke termen worden vaste stoffen, vloeistoffen en gassen de drie primaire fasen van materie genoemd. Een faseovergang, zoals smelten, bevriezen, koken of condenseren, vindt plaats wanneer een materiaal van de ene fase naar de andere verschuift. Elke stof heeft zijn eigen karakteristieke smelt- en kookpunten, die afhankelijk zijn van de moleculaire structuur en de omgevingsdruk. Kooldioxidedamp wordt bijvoorbeeld droogijs (vaste CO₂) bij -109°F onder standaard atmosferische druk, en vormt alleen een vloeistof onder hoge druk.
Warmte en temperatuur
Wanneer een vaste stof wordt verwarmd, stijgt de temperatuur totdat deze het smeltpunt bereikt. Bij deze temperatuur verhoogt de extra warmte de temperatuur niet, maar wordt deze in plaats daarvan gebruikt als fusiewarmte om het rooster van de vaste stof te breken en om te zetten in vloeistof. De temperatuur blijft constant totdat het gehele monster is gesmolten. Tijdens het koken vindt een soortgelijk proces plaats:de verdampingswarmte is nodig om vloeistof in gas om te zetten, waarbij de temperatuur stabiel blijft totdat de faseverandering is voltooid.
Smelten
Het smelten wordt bepaald door de kracht van intermoleculaire krachten, zoals de Londense dispersiekrachten en waterstofbruggen, die moleculen bij elkaar houden in een kristalrooster. Materialen met zwakkere krachten hebben lagere smeltpunten; degenen met sterkere krachten hebben hogere temperaturen nodig om het rooster te verstoren. Wanneer er voldoende thermische energie wordt geleverd, overwinnen alle moleculen deze krachten en gaan ze over naar de vloeibare fase.
Koken
Koken is de overgang van vloeistof naar gas die plaatsvindt wanneer de dampdruk van een vloeistof gelijk is aan de omringende atmosferische druk. Op dit punt verkrijgen moleculen voldoende kinetische energie om aan het vloeistofoppervlak te ontsnappen, waardoor dampbellen door de vloeistof worden gevormd. Naarmate de temperatuur stijgt, bereiken meer moleculen de energiedrempel, waardoor de snelheid van dampvorming toeneemt totdat de vloeistof volledig is verdampt.
 Onderzoek toont aan dat kosteneffectieve polymeerkit het verlies van irrigatiewater wereldwijd aanzienlijk kan verminderen
Onderzoek toont aan dat kosteneffectieve polymeerkit het verlies van irrigatiewater wereldwijd aanzienlijk kan verminderen Wat zijn de subtakken van de aardewetenschap?
Wat zijn de subtakken van de aardewetenschap?  Bosbranden kunnen giftig drinkwater achterlaten – zo bescherm je het publiek
Bosbranden kunnen giftig drinkwater achterlaten – zo bescherm je het publiek Hoe Twitter – nu X – helpt bij het begrijpen van de Canadese waarden en houding ten opzichte van asielzoekers
Hoe Twitter – nu X – helpt bij het begrijpen van de Canadese waarden en houding ten opzichte van asielzoekers  Plastic in zee kost de samenleving miljarden dollars
Plastic in zee kost de samenleving miljarden dollars
Hoofdlijnen
- Wanneer een kloon wordt gemaakt Welk type cel dat wordt gebruikt om te laten groeien .haploïde of diploïde?
- Mutualisme (biologie): definitie, types, feiten en voorbeelden
- Wat is etiolaat?
- Wat is de naam van cel waaruito -cellen afkomstig zijn?
- Hoe kan een bioloog bepalen of mutatie heeft plaatsgevonden?
- Nieuwe structuren bieden inzicht in hoe een bacteriële motor bacteriële chemotaxis aandrijft, een belangrijk infectieus proces
- Welke chemische stof wordt soms gebruikt om cellulair plastic te maken?
- Wat zijn enkele voorbeelden van aanpassingsdieren en planten?
- Waarom cellen enorme hoeveelheden rRNA produceren uit slechts één enkele rRNA-genkopie per cel
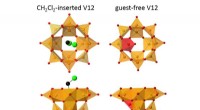
- Omgedraaide metaaloxide kooi kan kooldioxide scheiden van koolmonoxide
- Onderzoekers creëren vloeistofafstotende substantie die op alle oppervlakken werkt

- Natuurkunde versus astma

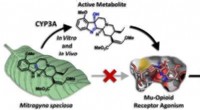
- Kratoms befaamde pijnstillende voordelen kunnen afkomstig zijn van een van zijn metabolieten
- Chemici maken kunstmatige eiwitten die in het chemische verleden van de aarde kijken

 Hoe beïnvloedt de massa van een object de uitkomst wanneer er een onevenwichtige kracht op inwerkt?
Hoe beïnvloedt de massa van een object de uitkomst wanneer er een onevenwichtige kracht op inwerkt?  Beschrijf de kracht die ervoor zorgt dat planeten in een baan rond de zon blijven?
Beschrijf de kracht die ervoor zorgt dat planeten in een baan rond de zon blijven?  Prokaryotische cellen:belangrijkste verschillen met eukaryoten
Prokaryotische cellen:belangrijkste verschillen met eukaryoten  Sunspot -activiteit en magnetische stormen zijn gerelateerd hoe?
Sunspot -activiteit en magnetische stormen zijn gerelateerd hoe?  De stijgende zeespiegel slokt de stranden van Outer Banks op, nieuw rapport zegt:
De stijgende zeespiegel slokt de stranden van Outer Banks op, nieuw rapport zegt: All-nitride supergeleidende qubit gemaakt op een siliciumsubstraat
All-nitride supergeleidende qubit gemaakt op een siliciumsubstraat Redt energiebesparing het klimaat?
Redt energiebesparing het klimaat? Leg uit hoe wetenschappers seismische golven gebruiken om het interieur in kaart te brengen?
Leg uit hoe wetenschappers seismische golven gebruiken om het interieur in kaart te brengen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

