
Wetenschap
Hoe niet-polaire moleculen zich in water gedragen:de wetenschap van hydrofobiciteit
Door Allison Horky
Bijgewerkt op 24 maart 2022
Eigenschappen van water
Water is een polair molecuul dat bestaat uit één zuurstofatoom en twee waterstofatomen. De ongelijke verdeling van elektronen geeft het zuurstofuiteinde een lichte negatieve lading en het waterstofuiteinde een lichte positieve lading. Door deze polariteit kan water uitgebreide waterstofbruggen vormen en is het een uitstekend oplosmiddel voor ionische en polaire soorten, zoals natriumchloride, waarbij de positieve ionen worden aangetrokken door zuurstof en de negatieve ionen door waterstof.
Hydrofobe (niet-polaire) moleculen
Niet-polaire moleculen missen een ongelijkmatige ladingsverdeling; hun elektronen worden gelijkelijk verdeeld over covalente bindingen. Als gevolg hiervan hebben ze geen gunstige wisselwerking met de gedeeltelijke ladingen in water. Deze “watervreesende” aard, of hydrofobiciteit, zorgt ervoor dat niet-polaire moleculen samenklonteren in plaats van zich te verspreiden.
Waterstofbinding en membraanvorming
Omdat de waterstofbruggen van water een netwerk creëren dat polaire interacties bevordert, worden niet-polaire moleculen effectief uitgesloten. Wanneer ze in water worden verspreid, aggregeren ze en vormen ze een strak, vaak bolvormig membraan dat hun hydrofobe interieur beschermt tegen contact met water. Dit principe ligt ten grondslag aan biologische structuren zoals celmembranen, waar de hydrofobe staarten van fosfolipiden naar binnen gericht zijn, terwijl hydrofiele koppen in aanraking komen met de waterige omgeving.
Praktisch voorbeeld:olie in water
Een gezamenlijke keukendemonstratie illustreert dit fenomeen. Wanneer plantaardige olie, gemengd met een scheutje kleurstof, in een doorzichtige beker op water wordt gegoten, vormt de olie duidelijke druppels op het oppervlak. De druppeltjes verspreiden zich niet omdat de niet-polaire koolwaterstofketens de polaire watermoleculen afstoten. Na verloop van tijd diffundeert de voedselkleuring langzaam in het water, wat aantoont dat polaire moleculen het grensvlak kunnen passeren, terwijl de niet-polaire kern geïsoleerd blijft.
Deze waarnemingen bevestigen dat de polariteit van water, de waterstofbinding en de intrinsieke stabiliteit van niet-polaire covalente bindingen gezamenlijk bepalen hoe niet-polaire stoffen zich gedragen in waterige omgevingen.
 EU krijgt zware last van vervuiling:eerste normen voor vrachtwagens
EU krijgt zware last van vervuiling:eerste normen voor vrachtwagens Diepe duik in het binnenste van de aarde laat zien dat verandering niet diep in de huid zit
Diepe duik in het binnenste van de aarde laat zien dat verandering niet diep in de huid zit Wat gebeurt er als je een blad van onkruidplant snijdt?
Wat gebeurt er als je een blad van onkruidplant snijdt?  Opgelost barium als nieuwe kwantitatieve indicator voor Kuroshio-inval in de Oost-Chinese Zee
Opgelost barium als nieuwe kwantitatieve indicator voor Kuroshio-inval in de Oost-Chinese Zee Welke aanpassingen moeten de bevers overleven?
Welke aanpassingen moeten de bevers overleven?
Hoofdlijnen
- Hoe de evolutie de optimale botstructuur bij hoppende knaagdieren voorbijschoot
- Wie heeft natuurlijke vezels ontdekt?
- Explosie van ratten, klaverblaadjes, bedmijt, muggen onbedoeld evolutionair gevolg van verstedelijking
- Wat is Bacillus Typhosa?
- Hoe de gecorrigeerde WBC-telling te berekenen
- Hebben alle levende wezens celwanden als buitengrens?
- Elektroforesetoepassingen:van DNA-analyse tot vaccinontwikkeling
- Welke eiwitstructuur verplaatst chromosomen?
- Een gen is recessief wanneer?
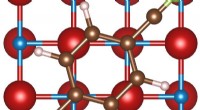
- Solid-ion-geleiders voor veiligere batterijen
- Hoe het stabiliseren van ongeordende eiwitten kan leiden tot de volgende generatie medische toepassingen

- Forensische wetenschappers ontsluiten unieke chemische handtekeningen in banden

- Beoordeling van de impact van verliesmechanismen in zonnecelkandidaat-antimoonsulfideselenide

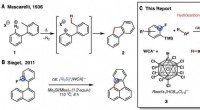
- Functionaliseren van niet-geactiveerde alkanen met behulp van reacties op basis van katalysatoren gemaakt van meer overvloedige materialen
 Als de aardmaan en de zon in de rij staan, wat kan er dan gebeuren?
Als de aardmaan en de zon in de rij staan, wat kan er dan gebeuren?  Hoe gebruikt een raket de bewegingswetten van Newtons?
Hoe gebruikt een raket de bewegingswetten van Newtons?  Ethiopische bemanning volgde procedure maar kon jet niet besturen:onderzoek
Ethiopische bemanning volgde procedure maar kon jet niet besturen:onderzoek Zou 'Oumuamua een buitenaards zonnezeil kunnen zijn?
Zou 'Oumuamua een buitenaards zonnezeil kunnen zijn?  Hoe heeft de Astrolabe het leven gemakkelijker gemaakt?
Hoe heeft de Astrolabe het leven gemakkelijker gemaakt?  Zijn sterren met een hogere oppervlaktetemperatuur ouder in leeftijd?
Zijn sterren met een hogere oppervlaktetemperatuur ouder in leeftijd?  Waarom de aarde rond de zon draait
Waarom de aarde rond de zon draait  Zijn de sterren verder dan de maan?
Zijn de sterren verder dan de maan?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

