
Wetenschap
Natuurkunde versus astma
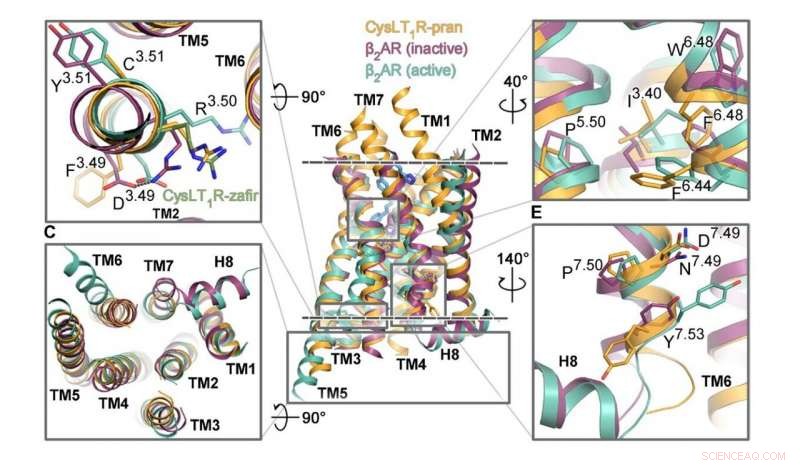
De segmenten van de CysLT1-receptor die verantwoordelijk zijn voor de activering worden weergegeven in oranje, naast andere aan G-eiwit gekoppelde receptoren. Krediet:Luginina et al./Science Advances
Een onderzoeksteam van het MIPT Center for Molecular Mechanisms of Aging and Age-Related Diseases heeft samengewerkt met collega's uit de VS, Canada, Frankrijk, en Duitsland om de ruimtelijke structuur van de CysLT1-receptor te bepalen. De krant is gepubliceerd in wetenschappelijke vooruitgang .
G-eiwit-gekoppelde receptoren, of GPCR's, zijn moleculaire machines ingebouwd in celmembranen. Deze receptoren pikken specifieke signalen aan de buitenkant van een cel op en geven deze door aan de cel. De signalen komen uit verschillende bronnen, inclusief fotonen van licht, vet moleculen, kleine eiwitten, en DNA-fragmenten. Een GPCR kan verschillende gebeurtenissen in de cel veroorzaken, zoals verdeeldheid, verhuizing, of zelfs de dood.
De GPCR-gemedieerde cellulaire "communicatie" is cruciaal voor het functioneren van een organisme. Geen wonder dat deze receptoren op de een of andere manier betrokken zijn bij alle processen in ons lichaam. Ze zijn het doelwit van ongeveer 40% van de bestaande medicijnen, te. Dus, het is interessant voor structurele biologen om het werkingsmechanisme van deze biologische machines te begrijpen en een manier te vinden om ze te beïnvloeden, door nieuwe medicijnen te ontwikkelen met meer specificiteit en minder bijwerkingen.
Structurele biologie is een interdisciplinair veld op het snijvlak van natuurkunde en biologie, bezig met het bestuderen van de 3D-rangschikking van biologische macromoleculen, zoals eiwitten. Structurele studies omvatten genetische manipulatie, kunstmatige eiwitproductie, zuivering, en kristallisatie. Zodra het eiwitkristal is verkregen, de fysica komt binnen:onderzoekers stellen het eiwitkristal bloot aan krachtige röntgenstralen om diffractiepatronen te genereren. De resulterende gegevens kunnen wiskundig worden verwerkt om een gedetailleerde 3D-atoomstructuur van een bepaald eiwitmolecuul te herstellen, met een precisie tot enkele angstroms.
Structurele studies zijn gebaseerd op krachtige röntgenbronnen. Deze zijn er meestal in twee soorten:synchrotrons en de meer recent ontwikkelde vrije-elektronenlasers. In beide gevallen, elektronen worden versneld tot bijna de lichtsnelheid. Ze worden dan gedwongen om hun snelheid of bewegingsrichting te veranderen, wat leidt tot röntgenstraling. In een synchrotron, de elektronen bewegen langs een gekromde, bijna cirkelvormige baan. In een vrije elektronenlaser, ze reizen door een doorgang tussen twee rijen afwisselend tegengesteld gerichte magneten, bekend als een undulator.
Hoewel structurele biologen al sinds de jaren zeventig synchrotrons gebruiken, vrije-elektronenlasers zijn een relatief recente toevoeging aan de toolkit voor eiwitkristallografie. Geïntroduceerd in de vroege jaren 2010, ze genereren extreem krachtige straling en maken röntgendiffractieanalyse mogelijk van minuscule kristallen van 1 micrometer. Dit nieuwe instrument heeft al geleid tot de ontdekking van enkele honderden structuren.
Onderzoekers van het MIPT hebben de structuur onderzocht van een GPCR die bekend staat als CysLT1. Het is betrokken bij ontstekingsprocessen en speelt een belangrijke rol bij allergische aandoeningen, inclusief astma, die ongeveer 10% van de wereldbevolking treft. Het team van biofysici verkreeg de gedetailleerde 3D-structuur van de receptor met de moleculen van zafirlukast en pranlukast. Dit zijn twee medicijnen die worden voorgeschreven aan patiënten met astma, allergische rhinitis, en netelroos.
Hoewel relatief groot, 0,3 millimeter kristallen met pranlukast werden in het onderzoek gekweekt, de kristallen met zafirlukast bereikten slechts de grootte van enkele micrometers. De voormalige monsters zijn onderzocht in de ESRF-synchrotron in Grenoble, Frankrijk. Deze laatste werden onderzocht met behulp van de door Stanford University beheerde Linac Coherent Light Source, een vrije elektronenlaser. De collega's van de onderzoekers uit Canada hielpen de mechanismen van signaaloverdracht via CysLT1 te onderzoeken.
"Dit zijn ongetwijfeld unieke structuren, en we zijn dol op ze geworden, " zei co-auteur van de studie Aleksandra Luginina van het MIPT Laboratory of Structural Biology of G Protein-Coupled Receptors. "Het werkingsmechanisme van de CysLT1-receptor actualiseert hoe we de werking van GPCR-eiwitsubgroepen zien. Ook, door de bindingsplaatsen voor de zafirlukast- en pranlukast-moleculen te identificeren, we leggen de basis voor het verbeteren van astmamedicatie - het verhogen van hun efficiëntie en het verminderen van bijwerkingen."
GPCR's zijn notoir moeilijke objecten voor structurele studies. Slechts een handvol labs wereldwijd is erin geslaagd om dit soort onderzoeksprojecten af te ronden. Het MIPT-team is blij dat er nu een laboratorium van het Instituut bij is.
 Wetenschappers ontdekken pad naar verbetering van baanbrekende batterij-elektrode
Wetenschappers ontdekken pad naar verbetering van baanbrekende batterij-elektrode Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken
Ingenieurs pionieren met het vormingsproces van platinagranaten, eerste waarneming ooit bereiken Chemici lossen de oorsprong van perovskietinstabiliteit op
Chemici lossen de oorsprong van perovskietinstabiliteit op Vloeibare schokdempers
Vloeibare schokdempers De optimale temperatuur van alkalische fosfatase
De optimale temperatuur van alkalische fosfatase
 Gebonden voor de EU, Biomassa van Amerikaanse makelij controleert de juiste vakjes
Gebonden voor de EU, Biomassa van Amerikaanse makelij controleert de juiste vakjes Sla laat zien hoe je met olie doordrenkte grond kunt herstellen
Sla laat zien hoe je met olie doordrenkte grond kunt herstellen Vervuiling van producten:CO2-concurrentie gaat laatste ronde in
Vervuiling van producten:CO2-concurrentie gaat laatste ronde in Ondersteuning van de particuliere sector is essentieel om de uitstoot in het Midden-Oosten en Noord-Afrika te verminderen, deskundigen zeggen
Ondersteuning van de particuliere sector is essentieel om de uitstoot in het Midden-Oosten en Noord-Afrika te verminderen, deskundigen zeggen Ondanks een tragere groei van de uitstoot, kooldioxidegehalte blijft hoog
Ondanks een tragere groei van de uitstoot, kooldioxidegehalte blijft hoog
Hoofdlijnen
- Zelfbevruchtende vissen hebben een verrassende hoeveelheid genetische diversiteit
- Transformatief onderzoek onrealistisch om te voorspellen, wetenschappers vertellen subsidieverstrekkers
- Microbiële ziekten en mutaties: wat is het ?, Lijsten & Oorzaken
- Hoe Charles Darwin werkte
- Twee neuropeptiden in zebravissen geven aanwijzingen voor de complexe neurale mechanismen die ten grondslag liggen aan slaap
- Onderzoekers ontsluiten mogelijk pad om vleesetende bacteriën te behandelen
- Eerste levensvormen op aarde onthuld in hete lente
- Wetenschappers stellen universele wetten voor over de grootte en biologie van plantenzaden
- Natuurlijke selectie: definitie, Darwins-theorie, voorbeelden en feiten
- Hoe effectieve nucleaire lading te berekenen

- Statistische gevolgtrekking om de werkwijze van een zeer ervaren kristallograaf na te bootsen
- Haaibestendig materiaal voor wetsuits kan levens helpen redden

- E-waste transformeren in een sterk, beschermende coating voor metaal

- Infraroodsensor als nieuwe methode voor medicijnontdekking

 Wiskundige onthult oudste voorbeeld van toegepaste meetkunde ter wereld
Wiskundige onthult oudste voorbeeld van toegepaste meetkunde ter wereld Kijk hoe martiaanse wolken opschieten, dankzij NASA's Curiosity
Kijk hoe martiaanse wolken opschieten, dankzij NASA's Curiosity Nanoseconde laser-geïnduceerde amplificatie van een fotochrome reactie in een diaryletheen nanodeeltje
Nanoseconde laser-geïnduceerde amplificatie van een fotochrome reactie in een diaryletheen nanodeeltje Verschillen tussen HDPE-kunststof en polyetheen
Verschillen tussen HDPE-kunststof en polyetheen  Metaalcomplexen gemaakt van cyclische moleculen
Metaalcomplexen gemaakt van cyclische moleculen Telescopen en satellieten worden gecombineerd om de grondbewegingen van hele planeten in kaart te brengen
Telescopen en satellieten worden gecombineerd om de grondbewegingen van hele planeten in kaart te brengen Instrument bij BESSY II laat zien hoe licht molybdeendisulfidelagen activeert om katalysatoren te worden
Instrument bij BESSY II laat zien hoe licht molybdeendisulfidelagen activeert om katalysatoren te worden Hoe verdampingssnelheden te berekenen
Hoe verdampingssnelheden te berekenen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

