
Wetenschap
Elementen die stabiele elektronenconfiguraties missen:een overzicht
Jupiterimages/Photos.com/Getty Images
Een atoom bestaat uit een kern met daarin positief geladen deeltjes omgeven door een wolk negatief geladen elektronen. Elektronen in atomen zitten in een reeks "schillen" rond de kern, en elke schil kan een vast aantal elektronen bevatten. Van elementen met een volledige buitenschil wordt gezegd dat ze een stabiele elektronenconfiguratie hebben. Elementen met stabiele elektronenconfiguraties komen alleen voor binnen een enkele kolom (groep 8) van het periodiek systeem. Daarom heeft de overgrote meerderheid van de elementen in het periodiek systeem onstabiele elektronenconfiguraties.
Waterstof
Waterstof
Waterstof is het eenvoudigste element in het periodiek systeem en bestaat uit een enkel proton en een enkel elektron. Het enkele elektron bevindt zich in de 1s-schil, die twee elektronen kan bezitten. De waterstofelektronicaconfiguratie is daarom niet stabiel. Om de 1s-schil te vullen, combineren en delen twee waterstofatomen het tweede elektron. Dit staat bekend als covalente binding en leidt in dit geval tot de vorming van een waterstofmolecuul.
Natrium
Natrium
Natrium bevindt zich in groep 1 van het periodiek systeem en elk atoom bevat 11 elektronen. Eén enkel elektron bevindt zich in de buitenste 3s-schil, die twee elektronen kan vasthouden. Omdat dit een onstabiele elektronenconfiguratie is, verliest natrium vaak zijn buitenste 3s-elektron, waardoor een positief geladen ion ontstaat. Positief en negatief geladen ionen combineren zich tot moleculen. Dit staat bekend als een ionische binding en leidt in natrium tot een verscheidenheid aan moleculen, waaronder natriumchloride.
Koolstof
Koolstof
Koolstof bevindt zich in groep 6 van het periodiek systeem en bezit in totaal zes elektronen. De buitenste 2p-elektronenschil wordt ingenomen door twee elektronen. Omdat 2p-schillen zes elektronen kunnen bevatten, bevindt koolstof zich niet in een stabiele elektronenconfiguratie. Om koolstof een stabiele elektronenconfiguratie te laten verkrijgen, moet het nog eens vier elektronen delen via covalente bindingen. Het is dit proces dat leidt tot de grote hoeveelheid koolstofverbindingen, zoals methaan.
Chloor
Chloor
Chloor bevindt zich in groep 7 van het periodiek systeem en bezit 17 elektronen. De buitenste 3p-schil wordt ingenomen door vijf elektronen en heeft daarom nog één elektron nodig om een stabiele configuratie te hebben. Chloor krijgt dit extra elektron vaak ten koste van het feit dat het een negatief geladen ion wordt. Dit betekent dat chloor zich kan verbinden met elk positief geladen ion, waardoor een ionische binding ontstaat. Een goed voorbeeld is natriumchloride, ook wel keukenzout genoemd.
 Dieren in een bosecosysteem
Dieren in een bosecosysteem  Wat betekent het van belang de wetenschapstermijn?
Wat betekent het van belang de wetenschapstermijn?  Orkanen en bosbranden botsen met de COVID-19-pandemie, en het vergroten van de risico's
Orkanen en bosbranden botsen met de COVID-19-pandemie, en het vergroten van de risico's Nieuw-Zeeland investeert in de groei van zijn binnenlandse recyclingindustrie om banen te creëren en minder afval op stortplaatsen te dumpen
Nieuw-Zeeland investeert in de groei van zijn binnenlandse recyclingindustrie om banen te creëren en minder afval op stortplaatsen te dumpen Nieuw onderzoek vindt ongekende verzwakking van Aziatische zomermoesson
Nieuw onderzoek vindt ongekende verzwakking van Aziatische zomermoesson
Hoofdlijnen
- Mitochondria:de krachtpatser van de cel - Functie en rol
- Welke biomoleculen zijn aanwezig in mitochondria?
- Wat is de term die wetenschapper gebruikt om te beschrijven hoe reproductief succesvol een organisme in zijn omgeving?
- Wat is een soort reproductie wanneer een nieuwe organismen soms meer dan één worden geproduceerd die erfelijk materiaal heeft dat identiek is aan het ouderorganisme?
- In welke biome leven schorpianen?
- Wat is een andere naam voor een onrijpe eiercel?
- Welk type bloedcel is verantwoordelijk voor immuniteit?
- Minder herkauwen, meer vergroening van de brandstof
- Is een weefsel georganiseerde groep cellen?
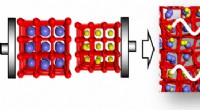
- Gebruikmaken van geometrische frustratie om batterijen af te stemmen voor meer vermogen
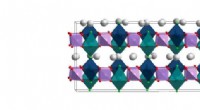
- Nieuwe genomische methode onthult atomaire rangschikkingen van batterijmateriaal
- Een nieuwe betaalbare en gebruiksvriendelijke technologie voor de diagnose van droge ogen

- Zijn kurkuma-folieverpakkingen de toekomst voor het supermarktschap?

- 3D-printen van zetmeel voor gepersonaliseerde medicijnontwikkeling

 Welke wiskundige concepten zijn nodig om klassen op universitair niveau te begrijpen?
Welke wiskundige concepten zijn nodig om klassen op universitair niveau te begrijpen?  Hoe werkt een mierenkolonie?
Hoe werkt een mierenkolonie?  Astronomen zijn getuige van David versus Goliath-gevecht tussen sterrenstelsels
Astronomen zijn getuige van David versus Goliath-gevecht tussen sterrenstelsels De Rode Zee is vernoemd naar de algenbloei van wat?
De Rode Zee is vernoemd naar de algenbloei van wat?  Klopt het dat kern elektronen en protonen bevat?
Klopt het dat kern elektronen en protonen bevat?  Is Wax Harding een chemische verandering?
Is Wax Harding een chemische verandering?  Waar zijn enkele van 's werelds meest vruchtbare grond die dichtbij wordt gevonden?
Waar zijn enkele van 's werelds meest vruchtbare grond die dichtbij wordt gevonden?  Zijn organische verbindingen die een belangrijke energiebron zijn.
Zijn organische verbindingen die een belangrijke energiebron zijn.
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

