
Wetenschap
Osmolariteit berekenen:een stapsgewijze handleiding voor nauwkeurige oplossingen
kunstenaar/iStock/GettyImages
Osmolariteit is de maat voor de concentratie van een opgeloste stof in een oplossing. Het is specifiek een maatstaf voor het aantal mol opgeloste deeltjes in een bepaald volume oplossing en is vergelijkbaar met de molariteit, die het aantal mol opgeloste stof in een bepaald volume oplossing meet. De osmolariteit kan worden berekend op basis van de osmotische coëfficiënt, het aantal deeltjes waarin de opgeloste stof dissocieert, en de molariteit van de opgeloste stof.
De stappen
Stap 1
Beschrijf het verschil tussen osmolariteit en molariteit. Dit onderscheid is te wijten aan het feit dat sommige opgeloste stoffen dissociëren wanneer ze oplossen, terwijl andere dat niet doen. Keukenzout (NaCl) valt bijvoorbeeld uiteen in de samenstellende ionen (Na+ en Cl-) wanneer het oplost. Aan de andere kant dissocieert glucose niet in kleinere deeltjes wanneer het oplost.
Stap 2
Definieer de eenheden van osmolariteit. Osmolariteit wordt gemeten in osmol opgeloste stof per liter oplossing (osmol/l). Een osmol kan informeel worden omschreven als het aantal mol opgeloste componenten in een oplossing.
Stap 3
Beschrijf de osmotische coëfficiënt. Deze waarde is de afwijking van een testoplossing van de ideale oplossing. De volledige berekening van de osmotische coëfficiënt is complex, maar voor eenvoudige gevallen is het de mate van dissociatie van de opgeloste stof. De osmotische coëfficiënt zal in deze gevallen daarom een bereik van 0 tot 1 hebben, zodat de osmotische coëfficiënt 1 zal zijn wanneer de opgeloste stof volledig is opgelost.
Stap 4
Bereken de osmolariteit op basis van waargenomen waarden. De osmolariteit van een oplossing kan worden gegeven als de som van (yi)(ni)(Ci), waarbij yi de osmotische coëfficiënt van opgeloste stof i is, n het aantal deeltjes is waarin opgeloste stof i dissocieert en Ci de molariteit van opgeloste stof i is.
Stap 5
Meet de osmolariteit rechtstreeks met een osmometer. Deze apparaten meten de osmolariteit van specifieke deeltjes, zoals deeltjes die de dampspanning van een oplossing verlagen of het vriespunt van een oplossing verlagen.
 Planten kunnen de uitdagingen van de klimaatverandering weerstaan en herstellen van droogte door de chemische code van lignine aan te passen
Planten kunnen de uitdagingen van de klimaatverandering weerstaan en herstellen van droogte door de chemische code van lignine aan te passen Binnen een haarbreedte - forensische identificatie van enkel geverfde haarstreng nu mogelijk
Binnen een haarbreedte - forensische identificatie van enkel geverfde haarstreng nu mogelijk Een slim idee voor het recyclen van zeldzame aardfosforen uit gebruikte fluorescentielampen
Een slim idee voor het recyclen van zeldzame aardfosforen uit gebruikte fluorescentielampen  Wat is 1 natriumzuurstofwaterstof?
Wat is 1 natriumzuurstofwaterstof?  Standaardiseren en verminderen van kaliumpermanganaat:een praktische gids
Standaardiseren en verminderen van kaliumpermanganaat:een praktische gids
Hoofdlijnen
- Wanneer cellen afbreken welke elektrolyt verloren gaat uit de cel?
- Wat staat ook bekend als celsoep?
- Muizensperma overleeft in de ruimte, maar kunnen menselijke baby's dat ook?
- Wat is een verzameling verschillende organismen die in een ecosysteem leven?
- Welke twee mechanismen worden gebruikt om ATP uit glucosespiercellen te genereren?
- Welk biomolecuul gebruiken levende organismen als energieopslag?
- Hoe libellenvleugels hun patronen krijgen
- Aan welke worm heeft natuurlijke selectie?
- Welke parasiet geeft veel bacteriële virale rickettsiale en protozoale ziekten over?
- Onderzoekers voegen orde toe aan polymeergels

- Een neonatoommodel bouwen:een stapsgewijze handleiding

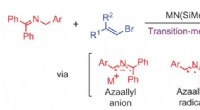
- Overgangsmetaalvrije koolstof-koolstofbindingsvormende reactie:vinylering van azaallyls
- Titratie in de industrie:hoe chemici de precisie meten in farmaceutische producten, wijnen en meer

- Zonnetoren stelt materialen bloot aan intense hitte om thermische respons te testen

 Hoe wordt cederzaad verspreid?
Hoe wordt cederzaad verspreid?  Laat u overdag de zonneschermen aanstaan om de warmte op te vangen of alleen 's nachts om te ontsnappen?
Laat u overdag de zonneschermen aanstaan om de warmte op te vangen of alleen 's nachts om te ontsnappen?  Waarom duren planeten verder van de zon langer om een baan om een baan?
Waarom duren planeten verder van de zon langer om een baan om een baan?  Hoe een baas te dicht bij werknemers kan komen
Hoe een baas te dicht bij werknemers kan komen Hoe verandert energie van de ene vorm andere, maar nooit opgebruikt?
Hoe verandert energie van de ene vorm andere, maar nooit opgebruikt?  Zouden stikstof en fosfor een covalente binding vormen?
Zouden stikstof en fosfor een covalente binding vormen?  Wat zijn Plaisade -cellen?
Wat zijn Plaisade -cellen?  Krill geeft inzicht in hoe mariene soorten zich kunnen aanpassen aan warmere wateren
Krill geeft inzicht in hoe mariene soorten zich kunnen aanpassen aan warmere wateren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

