
Wetenschap
De polariteit van water:waarom moleculen zich gedragen als kleine magneten
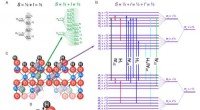
Stel je voor dat je een enkel watermolecuul van dichtbij observeert. De vorm lijkt op een gebogen ‘V’, met het zuurstofatoom aan de top en de twee waterstofatomen in een hoek van 104,5 graden, net als een kleine, asymmetrische magneet.
Waarom de vorm ertoe doet
De hoekige geometrie geeft water een permanent elektrisch dipoolmoment:de zuurstofzijde is gedeeltelijk negatief geladen, terwijl de waterstofzijde een gedeeltelijk positieve lading heeft. Deze polariteit vormt de basis van waterstofbinding, de subtiele maar krachtige aantrekkingskracht tussen aangrenzende moleculen.
Waterstofbruggen en hun gevolgen
In tegenstelling tot covalente bindingen die atomen aan elkaar verbinden, zijn waterstofbruggen relatief zwak maar persistent. Ze zorgen ervoor dat water verschillende afwijkende gedragingen kan vertonen die cruciaal zijn voor het leven.
Vier belangrijke afwijkingen
Cohesie en oppervlaktespanning
Watermoleculen trekken elkaar aan, waardoor oppervlaktespanning ontstaat waardoor insecten over water kunnen lopen en plantenwortels vloeistof door haarvaten naar boven kunnen trekken.
Verhoogd kookpunt
Het verbreken van waterstofbruggen vergt veel energie, waardoor het kookpunt van water stijgt tot 100 °C – veel hoger dan voor vergelijkbare moleculen als H₂Se of H₂S, die onder nul koken. Zonder dit zou de aarde geen stabiel vloeibaar water hebben.
IJs drijft
Wanneer water bevriest, vormen waterstofbruggen een open rooster, waardoor de structuur uitzet en de dichtheid afneemt. IJs heeft daarom een lagere dichtheid dan vloeibaar water, waardoor watermassa’s niet vastvriezen en het waterleven in de winter in stand wordt gehouden.
Universeel oplosmiddel
De polariteit van water lost een breed scala aan stoffen op, van elektrolyten tot organische verbindingen, waardoor het onmisbaar wordt voor biochemische reacties en het transport van voedingsstoffen in levende organismen.
Praktische implicaties
Magnetrons maken gebruik van het dipoolmoment van water:hoogfrequente straling brengt de dipolen op één lijn en brengt ze in beroering, waardoor warmte ontstaat die voedsel efficiënt kookt. Dit is een directe toepassing van hetzelfde magnetische gedrag dat de natuurlijke eigenschappen van water aanstuurt.
Deze verschijnselen onderstrepen waarom water vaak wordt beschreven als het ‘universele oplosmiddel’ en het ‘levensbloed’ van ecosystemen.
 Verwoesting door bosbranden kan aanhouden lang nadat de rook is opgetrokken
Verwoesting door bosbranden kan aanhouden lang nadat de rook is opgetrokken Kan het Arctische ‘ijsbeheer’ de klimaatverandering tegengaan?
Kan het Arctische ‘ijsbeheer’ de klimaatverandering tegengaan?  De natuur redden van vitaal belang om de klimaatcrisis te verslaan, zegt WWF-rapport
De natuur redden van vitaal belang om de klimaatcrisis te verslaan, zegt WWF-rapport Broeikasgasemissies van internationale scheepvaart nemen toe
Broeikasgasemissies van internationale scheepvaart nemen toe Satellietmetingen laten zien dat de mondiale CO2-uitstoot nog steeds stijgt
Satellietmetingen laten zien dat de mondiale CO2-uitstoot nog steeds stijgt
Hoofdlijnen
- Kan prokaryotisch reageren op hun omgeving?
- Welk stadium in de celcyclus speelt de belangrijkste rollen?
- Welke evolutionaire mechanismen kunnen de oorsprong en persistentie van cel-tot-cel signaleringssystemen in eencellige prokaryoten verklaren?
- Wat is DNA en waar het is gevonden?
- Onderzoekers onderzoeken hoe de cellulaire omgeving de conformationele dynamiek van eiwitten beïnvloedt
- Het ontsluiten van de genetische blauwdruk van appels:vorm- en maatkenmerken onthuld
- Wat is de functie van een basis op microscoop?
- Wat is sterker geërfd?
- Wat is het bijvoeglijk naamwoord voor organisme?
- Bevorderen van materiaalwetenschap voor supergeleidende kwantumcircuits
- Nieuw effectief en veilig antischimmelmiddel geïsoleerd uit het microbioom van de waterpijp

- Onderzoekers ontwerpen afstembare, zelfherstellende kleurstoffen voor gebruik in slimme apparaten van de volgende generatie

- Bouw een macroscopisch model van een booratoom – een stapsgewijze handleiding

- Verkenning van sojasausen zoutversterkende peptiden

 Celmuursamenstelling van de zes koninkrijken
Celmuursamenstelling van de zes koninkrijken  Waarom wetenschappers Alfred Wegener geloven?
Waarom wetenschappers Alfred Wegener geloven?  Hoe dragen ATP en NADPH bij aan fotosynthese?
Hoe dragen ATP en NADPH bij aan fotosynthese?  Tesla komt wanneer hij wordt gebeld, maar kan zenuwen rafelen
Tesla komt wanneer hij wordt gebeld, maar kan zenuwen rafelen Onderzoekers ontwikkelen een protocol voor snelle detectie van antibioticaresistente bacteriën
Onderzoekers ontwikkelen een protocol voor snelle detectie van antibioticaresistente bacteriën  Cycloon treft India, Bangladesh; 6 doden, 1.1M geëvacueerd
Cycloon treft India, Bangladesh; 6 doden, 1.1M geëvacueerd Hoe stopt kinetische energie?
Hoe stopt kinetische energie?  Hoe klimaat en waterbeheer de seizoensinvloeden van de stroom beïnvloeden
Hoe klimaat en waterbeheer de seizoensinvloeden van de stroom beïnvloeden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

