
Wetenschap
Hoe u een chemische formule schrijft – een praktische gids
Door Karen G. Blaettler
Bijgewerkt op 30 augustus 2022
RapidEye/iStock/GettyImages
Begrijpen hoe je een chemische formule schrijft, is essentieel voor het communiceren van de samenstelling van welke verbinding dan ook. Met een duidelijk begrip van de chemische basisterminologie kunt u vol vertrouwen formules lezen en schrijven.
Sleuteldefinities
Nauwkeurige taal is de ruggengraat van de wetenschap. Hieronder vindt u essentiële termen die u zullen helpen bij het interpreteren en maken van chemische formules.
- Atoom – De kleinste eenheid van een element, bestaande uit een kern (protonen en neutronen) en omringende elektronen.
- Element – Een stof gemaakt van één type atoom, geïdentificeerd door een uniek symbool op het periodiek systeem.
- Verbinding – Een stof die wordt gevormd wanneer twee of meer verschillende atomen chemisch aan elkaar binden.
- Molecuul – De kleinste eenheid van een verbinding die zijn chemische eigenschappen behoudt; moleculen zijn elektrisch neutraal.
- Ionen – Atomen of groepen atomen die elektronen hebben gewonnen of verloren, wat resulteert in een netto positieve of negatieve lading.
- Chemische formule – Een beknopte weergave van de samenstelling van een stof, met vermelding van de soorten en aantallen aanwezige atomen.
Elementsymbolen
Elk element heeft een symbool van één of twee letters, afgeleid van de Engelse of Latijnse naam (bijvoorbeeld Pb van *plumbum* voor lood). Als een symbool twee letters bevat, is de eerste een hoofdletter en de tweede een kleine letter.
Getallen gebruiken in formules
Getallen in een formule geven specifieke informatie weer:
- Pre-symboolnummers geef aan om hoeveel atomen of moleculen van die soort het gaat (bijvoorbeeld 2O in C + 2O → CO₂).
- Abonnementen toon het aantal atomen direct na het symbool; de afwezigheid van een subscript impliceert één atoom (CO₂ heeft bijvoorbeeld één C en twee O).
- Superscript geven de lading van een ion aan (bijvoorbeeld Mg²⁺, NO₃⁻).
- Wanneer een polyatomair ion meer dan eens voorkomt, omsluiten haakjes het ion en volgt een subscript het sluitende haakje (bijvoorbeeld Mg(NO₃)₂).
Voorbeeld:In magnesiumnitraat is de gebalanceerde vergelijkingMg²⁺ + 2(NO₃)⁻ → Mg(NO₃)₂ , wat aantoont dat de 2+ lading op Mg twee 1-negatieve nitraationen in evenwicht brengt om een neutrale verbinding te produceren.
Latijnse en Griekse voorvoegsels
Voorvoegsels helpen bij het identificeren van het aantal atomen of ionen in een verbinding:
- mono (1), bi/di (2), tri (3), tetra (4), penta (5), hexa (6), hepta (7)
Koolmonoxide (CO) bevat bijvoorbeeld één C en één O, terwijl kooldioxide (CO₂) één C- en twee O-atomen bevat.
Gemeenschappelijke polyatomaire ionen
- hydroxide – OH⁻
- carbonaat – CO₃²⁻
- fosfaat – PO₄³⁻
- nitraat – NO₃⁻
- sulfaat – SO₄²⁻
Praktisch formuleren van formules
Wanneer u een formule schrijft, noteer dan eerst het kation (positief ion), gevolgd door het anion (negatief ion).
- Natriumchloride (tafelzout):NaCl
- Tetrachloorkoolstof (oplosmiddel voor stomerij):CCl₄
- Natriumbicarbonaat (zuiveringszout):Na₂CO₃ (let op:het bicarbonaat-ion is CO₃²⁻; de formule is Na₂CO₃)
- Distikstofheptachloride :N₂Cl₇
- Ammoniumhydroxide (NH₃OH):NH₄OH – het ammoniumion (NH₄⁺) en het hydroxide-ion (OH⁻) vormen samen een neutraal molecuul.
Overgangsmetalen en Romeinse cijfers
Overgangsmetalen vormen vaak ionen met meerdere ladingen. De lading wordt in de naam van de verbinding aangegeven met een Romeins cijfer:
- CuF₂ is koper(II)fluoride omdat fluoride 1⁻ is; koper moet dus 2⁺ zijn.
- FeCl₃ is ijzer(III)chloride, waarbij ijzer(III) (3⁺) in evenwicht is met drie chloride-ionen (elk 1⁻).
- SnF₂ (stannofluoride) en SnF₄ (stannofluoride) illustreren het gebruik van "stanno" voor Sn²⁺ en "stanno" voor Sn⁴⁺.
Als u deze conventies begrijpt, zorgt u ervoor dat uw formules de chemische realiteit van elke verbinding nauwkeurig weerspiegelen.
 NASA analyseert tropische storm Wukongs aardbeivorm
NASA analyseert tropische storm Wukongs aardbeivorm GOES Satellite ziet tropische depressie 09E vorm
GOES Satellite ziet tropische depressie 09E vorm Onderzoek ondersteunt de zorgen van demonstranten over de toekomst van Llobregat Delta
Onderzoek ondersteunt de zorgen van demonstranten over de toekomst van Llobregat Delta Hoe is winderosie anders dan watererosie?
Hoe is winderosie anders dan watererosie?  Wetenschappers vinden boosdoeners voor extreme regenval boven de Yangtze-rivier in mei 2016
Wetenschappers vinden boosdoeners voor extreme regenval boven de Yangtze-rivier in mei 2016
Hoofdlijnen
- Wat zijn vier theorieën die de oorsprong van een staat verklaren?
- Wat zijn 4 dingen die alle cellen hebben?
- Wat zijn twee voorbeelden van aminozuren?
- Welk kenmerk binnen populaties zorgt ervoor dat de natuurlijke selectie opkomt?
- Hoe LEGO DNA-modellen te maken
- Wat uw urinekleur onthult over uw gezondheid
- Wat zijn enkele cellen organismen met stijve silica -celwanden in veel verschillende vormen?
- Welke RNA- en DNA -nucleotiden zijn purines?
- Ontbinding begrijpen:de stadia van organisch verval
- Nieuwe beeldvormingstechniek onthult hoe mechanische schade begint op moleculaire schaal
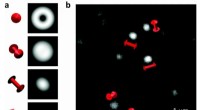
- Hyper-CEST NMR-techniek onthult ontbrekende structuur van een nieuw containermolecuul
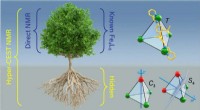
- Polyproline beschermt celmonolagen tegen vorstschade
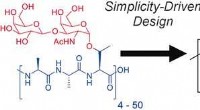
- Hoe we de vroegste glasproductie ten zuiden van de Sahara vonden, en wat het betekent

- Gecombineerde databenadering kan de ontwikkeling van nieuwe materialen versnellen
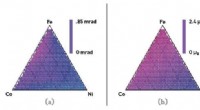
 Hoeveel moleculen van koolstofdioxide worden door de plant opgebruikt bij het produceren van elke zuurstof van molecuul?
Hoeveel moleculen van koolstofdioxide worden door de plant opgebruikt bij het produceren van elke zuurstof van molecuul?  Chemische formule voor barium(II)- en nitride-ionen (Ba2+ en N3-)
Chemische formule voor barium(II)- en nitride-ionen (Ba2+ en N3-)  Is het altijd gemakkelijk om verspilde energie te verzamelen en te gebruiken?
Is het altijd gemakkelijk om verspilde energie te verzamelen en te gebruiken?  Regulering van de atomaire Fe-Rh-plaatsafstand voor een efficiënte zuurstofreductiereactie
Regulering van de atomaire Fe-Rh-plaatsafstand voor een efficiënte zuurstofreductiereactie  Hoe is het mogelijk voor witte dwergen van een lagere helderheid dan de zon, hoewel veel koelere dwergen?
Hoe is het mogelijk voor witte dwergen van een lagere helderheid dan de zon, hoewel veel koelere dwergen?  Door neutronen en röntgenbeelden te combineren, bestuderen wetenschappers meteorieten om te onderzoeken hoe de aarde aan haar water kwam
Door neutronen en röntgenbeelden te combineren, bestuderen wetenschappers meteorieten om te onderzoeken hoe de aarde aan haar water kwam  Als een resulterende kracht wordt uitgeoefend op een object in de richting van de vermelde richting, bijvoorbeeld Noord, past de verhuizing erin de tweede wet van beweging toe, waarom dan?
Als een resulterende kracht wordt uitgeoefend op een object in de richting van de vermelde richting, bijvoorbeeld Noord, past de verhuizing erin de tweede wet van beweging toe, waarom dan?  Massa van 4,00 mol natrium berekenen?
Massa van 4,00 mol natrium berekenen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

