
Wetenschap
Hoe u de alkaliteit van water in CaCO₃-eenheden kunt berekenen – een praktische gids
Door Karen G. Blaettler – Bijgewerkt op 24 maart 2022
Zuiver water bestaat in de natuur nooit. Zelfs in gecontroleerde omgevingen gaat de zuiverheid ervan achteruit zodra deze wordt geopend. Het vermogen van water om een breed scala aan stoffen op te lossen is cruciaal voor het leven, en de opgeloste chemicaliën bepalen de belangrijkste fysieke omstandigheden in ecosystemen. Twee onderling verbonden parameters voor de waterkwaliteit zijn de zuurgraad en de alkaliteit.
Waarom alkaliteit belangrijk is
Alkaliteit is het vermogen van het water om pH-veranderingen te weerstaan, met name de verschuiving naar zuurgraad. Een hogere alkaliteit betekent een grotere buffercapaciteit, waardoor het waterleven dat gedijt binnen nauwe pH-bereiken wordt beschermd. Alkaliteit heeft ook invloed op de afvalwaterzuivering, de geschiktheid van irrigatie en huishoudelijke watersystemen, waar het kan bijdragen aan de vorming van kalkaanslag en het schuimen van zeep kan beïnvloeden.
Meeteenheden
De alkaliteit wordt gewoonlijk uitgedrukt als de calciumcarbonaatconcentratie (CaCO₃), weergegeven in delen per miljoen (ppm) of milligram per liter (mg/l). De conversiefactor is 1ppm=1mg/L.
Uw monster voorbereiden
Gebruik een aliquot van 50 ml voor typische alkaliteitsbereiken; voor water met een lage alkaliteit verbetert een monster van 100 ml de nauwkeurigheid. Filter het water door een membraan van 0,45 µm om zwevende deeltjes te verwijderen. Houd het monster op de oorspronkelijke temperatuur en bescherm het tegen licht en verontreinigingen. Controleer vóór titratie de zwavelzuuroplossing (doorgaans 0,01639N) aan de hand van een natriumcarbonaatstandaard.
Titratiemethode
De voorkeurstechniek is buigpunttitratie (IPT) met een glazen buret of een gekalibreerde digitale titrator. Voer de titratie zorgvuldig uit rond pH8,3 en het equivalentiepunt nabij pH4,5. Schone, droge apparatuur is essentieel om verdunning van het zuur te voorkomen.
Alkaliteit berekenen
- Bepaal de variabelen:
B– Gebruikt volume zuur (ml)Ca– Zuurconcentratie (meq/ml). Voor 0,01639N zwavelzuur,Ca = 0.01639.Vs– Monstervolume (ml)CF– Correctiefactor. Gebruik1.01voor digitale titratorcartridges van Hach; anders1.0.
- Alkaliteit in milli-equivalenten per liter (meq/L):
Alk(meq/L) = (1000 × B × Ca × CF) ÷ Vs - Alkaliteit als CaCO₃ (mg/L):
Alk(mg/L CaCO₃) = (50044 × B × Ca × CF) ÷ Vs
Voorbeeldberekening
Stel dat bij een titratie 12 ml 0,01639meq/ml zwavelzuur werd gebruikt op een watermonster van 50 ml met een standaardburet (CF = 1.0 ).
- Alk(meq/L) =(1000 × 12 × 0,01639 × 1,0) ÷ 50 =3,94meq/L
- Alk(mg/L CaCO₃) =(50044 × 12 × 0,01639 × 1,0) ÷ 50 =196,8 mg/L
De resultaten interpreteren
De alkaliteitswaarden worden uitgedrukt in mg/l, wat overeenkomt met ppm. Algemene richtlijnen:
- Zacht water:<17 ppm
- Hard water:17–180 ppm
- Zeer hard water:> 180 ppm
 Snelle vouwing voor synthetische peptiden en microproteïnen
Snelle vouwing voor synthetische peptiden en microproteïnen  Wat is het product van de reactie Tetraline met heet basisch kaliumpermanganaat?
Wat is het product van de reactie Tetraline met heet basisch kaliumpermanganaat?  Wat is latente warmteoverdracht?
Wat is latente warmteoverdracht?  Wat bevat een gecoördineerde covalente binding KCl HF H2O F2?
Wat bevat een gecoördineerde covalente binding KCl HF H2O F2?  Hoe verschilt het metaal magnesium van calcium in hun reactie met water?
Hoe verschilt het metaal magnesium van calcium in hun reactie met water?
Hoofdlijnen
- Wat eten diep watervissen?
- Waarom is het voordelig voor organismen zoals schimmels en algen om mutualistische relatie te vormen?
- Welke seksuele reproductie kan zijn ontstaan als een manier voor cellen?
- Groeien of delen de hartcellen gedurende het leven van een personen?
- Kan een menselijk organisme?
- Welke planten slaan voedsel op in hun stengel?
- Inzicht in de verspreiding van gedrag:hoe langdurige verbindingen de snelheid van sociale besmetting versnellen
- Introducties voor eigenschappen die van ouders worden doorgegeven aan nakomelingen die bekend staan als?
- Wat is de ORF van een gen?
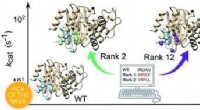
- Oude enzymen kunnen bijdragen aan groenere chemie
- Onderzoekers creëren een effectievere hydrogel voor het genezen van wonden

- Schone waterstof maken is moeilijk, maar onderzoekers hebben zojuist een grote hindernis opgelost

- Biofysici verhelderen de mechanismen van neutrale dragers van opgeloste stoffen

- Inzicht in enzymcascades die de sleutel zijn tot het begrijpen van het metabolisme
 Welk lichaamssysteem produceert hormonen om orgelactiviteit te reguleren?
Welk lichaamssysteem produceert hormonen om orgelactiviteit te reguleren?  Hoeveel atomen zijn er in CUSO4?
Hoeveel atomen zijn er in CUSO4?  Welke SD -kaart moet u gebruiken voor een Garmin Nuvi 1310?
Welke SD -kaart moet u gebruiken voor een Garmin Nuvi 1310?  Waarom community college-studenten stoppen ondanks dat ze bijna klaar zijn
Waarom community college-studenten stoppen ondanks dat ze bijna klaar zijn  Is fenylalanine een zuur of een base?
Is fenylalanine een zuur of een base?  Onderzoekers ontwikkelen computermodel van ferrofluïde beweging
Onderzoekers ontwikkelen computermodel van ferrofluïde beweging Wat zijn de verschillen tussen de dood van een enorme ster en gigantische ster?
Wat zijn de verschillen tussen de dood van een enorme ster en gigantische ster?  Wormen op nanoschaal bieden nieuwe route naar nanokettingstructuren
Wormen op nanoschaal bieden nieuwe route naar nanokettingstructuren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

