
Wetenschap
Rode oxideverf:chemie, toepassingen en veiligheid
Door Vincent Summers – Bijgewerkt op 24 maart 2022
Wat is roodoxide?
Rood oxide, ook wel minium of rood lood genoemd, is het loodtetraoxide (PbO₂). Hoewel het niet van nature voorkomt, kan het worden geproduceerd door het gewone lood(II)oxide, litharge, te oxideren:
6 PbO + O₂ → 2 PbO₂
Gemengde Valence-staten
PbO₂ kan worden weergegeven als 2PbO ↔ PbO₂, wat duidt op een mengsel van lood in +2 en +4 oxidatietoestanden. Deze gemengde valentie draagt bij aan het chemische gedrag.
Gebruik in verven en primers
In de coatingindustrie fungeert rood oxide als roestpreventiemiddel. Wanneer het wordt aangebracht op ijzeroppervlakken met lichte oxidatie, hecht het sterk door chemische bindingen te vormen met ijzeroxiden, waardoor een beschermende barrière ontstaat.
Chemische reacties met ijzer
Rood oxide reageert met ijzer en zijn oxiden en produceert onoplosbare plumbaten, waarbij lood onderdeel wordt van het anionische complex. Ferro-plumbaat (Fe(PbO₂)) bevat bijvoorbeeld Fe²⁺-kationen gebonden aan het PbO₂-anion.
Gezondheids- en milieuoverwegingen
Door de toxiciteit van lood is het gebruik van rode oxideverf sterk afgenomen. Moderne veiligheidsvoorschriften en het bewustzijn van de risico's van loodvergiftiging hebben fabrikanten ertoe aangezet op zoek te gaan naar alternatieve roestwerende coatings.
Toepassingen bij de glasproductie
Rood oxide wordt ook gebruikt in bepaalde glasformuleringen. In deze contexten bevindt het zich in de glasmatrix, wat een minimaal gezondheidsrisico voor de consument met zich meebrengt.
Raadpleeg de nieuwste ASTM- en OSHA-normen voor meer gedetailleerde veiligheidsrichtlijnen.
 Australië keurt nieuw steenkoolproject goed naarmate klimaatwaarschuwingen toenemen
Australië keurt nieuw steenkoolproject goed naarmate klimaatwaarschuwingen toenemen Nieuwe studie werpt licht op hoe en wanneer visie evolueerde
Nieuwe studie werpt licht op hoe en wanneer visie evolueerde  Door de mens gemaakte vezels en plastic gevonden in de diepste levende organismen
Door de mens gemaakte vezels en plastic gevonden in de diepste levende organismen Licht werpen op koraalriffen
Licht werpen op koraalriffen Ecologische doemloops:waarom het instorten van ecosystemen veel eerder kan plaatsvinden dan verwacht
Ecologische doemloops:waarom het instorten van ecosystemen veel eerder kan plaatsvinden dan verwacht
Hoofdlijnen
- Welke term wordt aan elk chromosoom gegeven in een dubbel of gerepliceerd paar?
- Nieuw onderzoek laat zien hoe sommige kippen gestreepte veren kregen
- Nieuwe studie laat zien hoe mierenkolonies zich anders gedragen in verschillende omgevingen
- Wat zijn drie belangrijkste delen van de celtheorie?
- Welke chromosomen draagt het minste aantal genen?
- Chemische cocktail in de huid roept ziekteverspreidende muggen op
- Welke plant groeit van sporen?
- Is het verschil tussen glycogeen en zetmeel?
- Wat zijn enzymen die de hydrolyse van vetten versnellen?
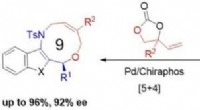
- Synthese van middelgrote ringstructuren
- Hoe u een weerstandstemperatuurdetector (RTD) kunt testen op nauwkeurige prestaties

- Tumbleweeds of fibrillen:Tau-eiwitten moeten kiezen
- Hoe efficiënte organische zonnecellen te bouwen?

- Hoe u de verbrandingswarmte van paraffinewas kunt meten:een stapsgewijze handleiding voor calorimetrie

 Vooruitgang in de wetenschap is een stap in de richting van zelfvernietiging?
Vooruitgang in de wetenschap is een stap in de richting van zelfvernietiging?  Snel en continu 3D-printen met licht
Snel en continu 3D-printen met licht Koolstofverwijdering:waarom ambitieuze 'no-nonsense'-plannen van cruciaal belang zijn om de opwarming van de aarde met 2℃ te beperken
Koolstofverwijdering:waarom ambitieuze 'no-nonsense'-plannen van cruciaal belang zijn om de opwarming van de aarde met 2℃ te beperken  Verrassende langzame elektronen worden geproduceerd wanneer intense lasers clusters van atomen raken
Verrassende langzame elektronen worden geproduceerd wanneer intense lasers clusters van atomen raken Onderzoek naar menselijke factoren versnelt missieplanning
Onderzoek naar menselijke factoren versnelt missieplanning Cling-film zonnecellen kunnen leiden tot vooruitgang in hernieuwbare energie
Cling-film zonnecellen kunnen leiden tot vooruitgang in hernieuwbare energie Wat is absolute waarde in de natuurkunde?
Wat is absolute waarde in de natuurkunde?  Zijn CH3CH2CH2CH2CH3 en CH3CH2CH2CH2CH2CH3 MILIJBABEL CBR4 H20 CL2 MILBABEL?
Zijn CH3CH2CH2CH2CH3 en CH3CH2CH2CH2CH2CH3 MILIJBABEL CBR4 H20 CL2 MILBABEL?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

