
Wetenschap
Hoe u de verbrandingswarmte van paraffinewas kunt meten:een stapsgewijze handleiding voor calorimetrie
Door Amber Webb | Bijgewerkt op 30 augustus 2022
MrDamien/iStock/GettyImages
In de scheikunde is dit de verbrandingswarmte kwantificeert de energie die vrijkomt wanneer een stof volledige oxidatie ondergaat. Het bepalen van deze waarde voor gewone brandstoffen, zoals paraffinewas, geeft inzicht in energieconversieprocessen, van voertuigmotoren tot de calorieën in onze voeding. Dit praktische experiment maakt gebruik van gemakkelijk verkrijgbare materialen om de verbrandingswarmte van een paraffinekaars te meten, waardoor je hands-on inzicht krijgt in thermochemische principes.
Experimentele procedure
1. Stel de calorimeter in
Vul een leeg frisdrankblikje met precies 100 ml koud water. Hang een digitale thermometer in het water met een strook Sticky Tack, zodat deze de wanden van het blik niet raakt. Deze opstelling vormt een eenvoudige calorimeter .
2. Bereid de kaars voor
Snijd de bovenkant van een tweede blikje frisdrank af, zodat er een schijf van 2,5 cm breed overblijft. Weeg de schijf en noteer de massa. Weeg de paraffinekaars en plaats de kaars op de schijf in de calorimeter.
3. Start de verbranding
Meet de initiële watertemperatuur. Steek de kaars aan en til vervolgens de calorimeter met een tang op, zodat de vlam zich net boven de kaars bevindt, zodat er voldoende luchtstroom is. Houd een veilige afstand aan om brandwonden te voorkomen.
4. Registreer definitieve gegevens
Wanneer de vlam dooft, noteer dan de maximale watertemperatuur. Verwijder de kaars en de schijf, weeg de resterende kaarsmassa en trek de schijfmassa af om de massa van de verbrande was te verkrijgen.
Gegevensanalyse
1. Massa verbrand en temperatuurstijging
Verbrande massa =initiële kaarsmassa – uiteindelijke kaarsmassa.
ΔT =eindtemperatuur – begintemperatuur.
2. Thermische energieoverdracht
Uitgaande van 1 ml water ≈ 1 g, gebruikt het experiment 100 g water. De specifieke warmtecapaciteit van water is 4,18Jg⁻¹°C⁻¹.
Thermische energie (Q) =100 g × ΔT × 4,18Jg⁻¹°C⁻¹.
3. Verbrandingswarmte
Verbrandingswarmte (ΔH_comb) =Q ÷ verbrande massa (g). Het resultaat wordt uitgedrukt in Jg⁻¹.
Benodigde materialen
- Paraffinewaskaars
- Koel water
- Twee lege frisdrankblikjes
- Tong
- Digitale thermometer (Celsius)
- Kleverige tack
- Precisiebalans
- Lichter
Veiligheidsmededeling
Raak de calorimeter niet aan als deze heet is, of direct daarna. Gebruik een tang en houd een veilige werkafstand aan om brandwonden te voorkomen.
 Waarom vertonen lanthaniden vergelijkbaar chemisch gedrag?
Waarom vertonen lanthaniden vergelijkbaar chemisch gedrag?  Hoeveel pond is gelijk aan 5 kg?
Hoeveel pond is gelijk aan 5 kg?  Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties
Molariteit beheersen:een stapsgewijze handleiding voor het berekenen van initiële concentraties  Nieuwe inzichten in waarom de aardewerkproductie aan het einde van de laatste ijstijd aanzienlijk toenam
Nieuwe inzichten in waarom de aardewerkproductie aan het einde van de laatste ijstijd aanzienlijk toenam  Nieuwe reactie maakt indoline-steigers beschikbaar voor farmaceutische ontwikkeling
Nieuwe reactie maakt indoline-steigers beschikbaar voor farmaceutische ontwikkeling
 Welk thema van geografie bestudeert mensen het klimaat en dieren weer?
Welk thema van geografie bestudeert mensen het klimaat en dieren weer?  Nieuwe tools helpen gemeenschappen hun uitstoot lokaal te meten en te verminderen
Nieuwe tools helpen gemeenschappen hun uitstoot lokaal te meten en te verminderen Orkanen Irma en Jose:wat we weten
Orkanen Irma en Jose:wat we weten NASA's nieuwe koolstofobservatorium wordt gelanceerd, ondanks de inspanningen van Trump om het te stoppen
NASA's nieuwe koolstofobservatorium wordt gelanceerd, ondanks de inspanningen van Trump om het te stoppen Het Westen ruilt water voor geld. Het water raakt op
Het Westen ruilt water voor geld. Het water raakt op
Hoofdlijnen
- Genoom versus gen:genetische informatie begrijpen
- Hebben bacteriën enzymen voor het uitvoeren van metabole activiteiten?
- Welk modelorganisme wordt meestal gebruikt voor studies in menselijke immuniteit?
- Weten hoe cellen groeien en delen kan leiden tot robuustere productieve planten
- Welke verklaring zou waarschijnlijk van een socioloog komen met behulp van de structurele functionele aanpak?
- Wie was de wetenschapper die de evolutie theorie maakt?
- Fluorescentiemicroscopie laat zien hoe levende cellen blaasjes vormen om vrachtachtige groeifactoren te transporteren
- Wat zijn de sublinguale klieren?
- Nieuwe strategie onderdrukt ongewenste verwijderingsgebeurtenissen om het bewerken van genoom veiliger en nauwkeuriger te maken
- Een nieuwe sensor voor licht, warmte en aanraking

- Botdiep:Mineraal gevonden in menselijk bot kan helpen bij het bestrijden van giftige organische stoffen
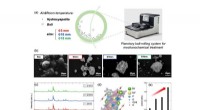
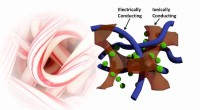
- Snoeprietpolymeerweefsel kan toekomstige functionele stoffen en apparaten van stroom voorzien
- Nieuw begrip van hoe cellen tunnels vormen, kan helpen bij het behandelen van wonden, tumoren

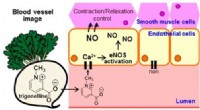
- Verbindingen in monsterradijs kunnen hart- en vaatziekten helpen temmen
 Punnett Squares:genetische resultaten voorspellen met Mendeliaanse principes
Punnett Squares:genetische resultaten voorspellen met Mendeliaanse principes  Het is onwaarschijnlijk dat Californië de historische doelstellingen voor het terugdringen van de uitstoot van broeikasgassen zal halen
Het is onwaarschijnlijk dat Californië de historische doelstellingen voor het terugdringen van de uitstoot van broeikasgassen zal halen  Wat is de naam voor een reactie die monomeren verbindt om een voedselketen te vormen?
Wat is de naam voor een reactie die monomeren verbindt om een voedselketen te vormen?  Hoe beïnvloedt waterwarmte-capaciteit mensen?
Hoe beïnvloedt waterwarmte-capaciteit mensen?  Wat is de chemische formule voor koolstof tri-nitride?
Wat is de chemische formule voor koolstof tri-nitride?  Hoe snel is 450 KNTS in MPH?
Hoe snel is 450 KNTS in MPH?  Een wetenschapper die probeert te bepalen waarom het besprenkelen van zout op een ijzige weg ervoor zorgt dat het ijs smelt zich bezighoudt met proces van?
Een wetenschapper die probeert te bepalen waarom het besprenkelen van zout op een ijzige weg ervoor zorgt dat het ijs smelt zich bezighoudt met proces van?  Wat betekent het om macht uit te oefenen?
Wat betekent het om macht uit te oefenen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

