
Wetenschap
Hoe u de titreerbare zuurgraad in wijn kunt berekenen:een stapsgewijze handleiding
Door bijdragende schrijver
Bijgewerkt op 24 maart 2022
Nauwkeurige titreerbare zuurgraadmetingen zijn essentieel voor wijnmakers, kwaliteitscontrolelaboratoria en voedseltechnologen. Het kwantificeert de totale hoeveelheid zuren in een oplossing door te titreren met een standaard natriumhydroxideoplossing (NaOH), waarbij een pH-gevoelige indicator wordt gebruikt om het eindpunt te bepalen. Het resultaat, uitgedrukt in gram per 100 ml, is een belangrijke parameter bij de wijnevaluatie, vooral waar wijnsteenzuur domineert.
Hieronder vindt u een duidelijke, industriestandaardmethode om de titreerbare zuurgraad te bepalen, geïllustreerd met een voorbeeld van wijnsteenzuur.
Stap 1:Bepaal de molaire massa van het zuur
Bereken de molaire massa door de atoomgewichten van alle samenstellende atomen bij elkaar op te tellen. Voor wijnsteenzuur (C4 H6 O6 ), gebruik de periodieke tabelwaarden:
M(C)=12, M(H)=1, M(O)=16.
Molaire massa =4×12 + 6×1 + 6×16 =150gmol –1 .
Stap 2:Bereken het aantal gebruikte mollen NaOH
Vermenigvuldig het titrantvolume met zijn molariteit:
Volume NaOH =12,6 ml =0,0126 l
Concentratie =0,1molL
–1
Mol NaOH =0,0126 l × 0,1 mol L –1 =0,00126mol.
Stap 3:Schrijf de neutralisatiereactie
C4 H6 O6 + 2NaOH → C4 H4 O6 Na2 + 2H2 O
Stap 4:Bereken het aantal mol zuur
Eén mol wijnsteenzuur reageert met twee mol NaOH. Daarom:
Molzuur =0,00126mol NaOH ÷ 2 =0,00063mol.
Stap 5:Schalen naar 100 ml
Aanpassen voor het aliquotvolume (15 ml):
Zuur in 100 ml =0,00063 mol × (100 ml ÷ 15 ml) =0,0042 mol.
Stap 6:Converteren naar g/100 ml
Vermenigvuldig met de molaire massa:
Titreerbare zuurgraad =0,0042mol × 150gmol –1 =0,63 g/100 ml.
Wat je nodig hebt
- Wetenschappelijke rekenmachine
- Periodiek systeem van elementen (bijvoorbeeld RSC Periodiek Systeem )
 Locals maken zich zorgen dat wind en zonne-energie bossen en boerderijen zullen opslokken
Locals maken zich zorgen dat wind en zonne-energie bossen en boerderijen zullen opslokken Studie onderzoekt hoe ras en cultuur de schooldiscipline en het aantal schooluitval beïnvloeden
Studie onderzoekt hoe ras en cultuur de schooldiscipline en het aantal schooluitval beïnvloeden  Diepvriesgrepen Upper Midwest, er komt nog meer bittere kou aan
Diepvriesgrepen Upper Midwest, er komt nog meer bittere kou aan Verminderde impact houtkap schaadt nog steeds de biodiversiteit in tropische regenwouden
Verminderde impact houtkap schaadt nog steeds de biodiversiteit in tropische regenwouden Bodemgeschiedenis:een oplossing voor oplosbaar fosfor?
Bodemgeschiedenis:een oplossing voor oplosbaar fosfor?
Hoofdlijnen
- Wat is de structuur van een celwand?
- Wat is de naam van een gespecialiseerde cellen van een groep die unieke materialen om hen heen produceren?
- Wie is de vader van bacteriën?
- Welke microscopische structuren van make -up organismen zoals mensen?
- Wat is de voedselketen van een bladdraak?
- Wie bestudeert de relatie tussen organismen en hun omgeving?
- Op welke manier zijn levende organismen op aarde vergelijkbaar?
- Vergelijk het gebruik van chemische en biologische controlepest?
- Freeze frame:Onderzoekers lossen op hoe cellen eiwitten ontvouwen
- Wolachtig materiaal kan zich herinneren en van vorm veranderen

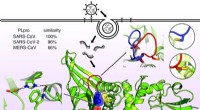
- Informatie over de moleculaire vorm van virussen die COVID-19 veroorzaken, SARS, en MERS onthult structurele overeenkomsten
- Optimalisatie van een nieuwe spuitmethode voor keramische coatings

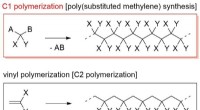
- Ontwikkeling van nieuwe slimme zachte materialen:Synthese van een pH-responsief gedendroniseerd poly(gesubstitueerd methyleen)s
- Video:Waarom wordt kunstmest gebruikt in explosieven?

 Nieuwe ontwerpen voor springende en met vleugels klappende microrobots
Nieuwe ontwerpen voor springende en met vleugels klappende microrobots Rapport identificeert factoren die verband houden met intimidatie, misbruik in academisch veldwerk
Rapport identificeert factoren die verband houden met intimidatie, misbruik in academisch veldwerk Het opruwen van een platina-elektrode
Het opruwen van een platina-elektrode Wat zijn de punten verste noord- en zuiden op aarde?
Wat zijn de punten verste noord- en zuiden op aarde?  Onderzoekers beoordelen hoe de stijging van de zeespiegel de gezondheid van zoetwatermosselen en andere zoutgevoelige soorten zal beïnvloeden
Onderzoekers beoordelen hoe de stijging van de zeespiegel de gezondheid van zoetwatermosselen en andere zoutgevoelige soorten zal beïnvloeden  Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen
Kunstmatige intelligentie kan worden ingesteld om kantelpunten van klimaatverandering te onthullen Zelfassemblerende nanodeeltjesarrays kunnen schakelen tussen een spiegel en een raam
Zelfassemblerende nanodeeltjesarrays kunnen schakelen tussen een spiegel en een raam Reageert waterstofbromide met chloor?
Reageert waterstofbromide met chloor?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

