
Wetenschap
Calorimeters begrijpen:hoe ze warmte meten en hun belangrijkste beperkingen
Door John Brennan
Bijgewerkt op 24 maart 2022
Yurko_Gud/iStock/GettyImages
Voor scheikundigen is het kwantificeren van de warmte die vrijkomt of wordt geabsorbeerd tijdens een reactie essentieel. Calorimeters zijn de hulpmiddelen die deze meting mogelijk maken, waardoor dieper inzicht in reactiemechanismen en betrouwbaardere voorspellingen mogelijk worden.
TL;DR
Calorimeters kwantificeren de warmte van een reactie. Hun belangrijkste nadelen zijn onvermijdelijk warmteverlies naar de omgeving en mogelijke temperatuurgradiënten in het monster.
De functies van een calorimeter
Een calorimeter registreert de temperatuurverandering van zowel de container als de reactanten. Na kalibratie levert het apparaat een calorimeterconstante op, die aangeeft hoeveel de temperatuur stijgt per toegevoegde eenheid warmte. Met deze constante en de massa van de reagerende soorten kunnen scheikundigen de enthalpieverandering van het proces berekenen. Het minimaliseren van warmteverlies naar de omgeving is cruciaal; anders zullen de gegevens vertekend zijn.
Verschillende soorten calorimeters
Terwijl een eenvoudige calorimeter voor koffiekopjes kan worden gebouwd met twee piepschuimbekers en een thermometer, gebruiken academische laboratoria meer geavanceerde apparatuur. De bomcalorimeter plaatst de reactanten bijvoorbeeld in een afgesloten stalen kamer (de ‘bom’). Een elektrische vonk ontsteekt het mengsel, en de daaropvolgende temperatuurstijging onthult de ontwikkelde of geabsorbeerde warmte. Elk ontwerp is afgestemd op specifieke reactietypen en nauwkeurigheidseisen.
Kalibratie van een calorimeter
Bij kalibratie wordt een bekende hoeveelheid warmte naar het systeem overgebracht. Een veelgebruikte methode is het mengwaterexperiment:warm en koud water worden gecombineerd in de calorimeter en het temperatuurverloop wordt geregistreerd. Door lineaire regressie toe te passen wordt de uiteindelijke evenwichtstemperatuur geschat. De warmte die door het koude water wordt gewonnen minus de warmte die door het warme water verloren gaat, is gelijk aan de warmte die door de calorimeter wordt geabsorbeerd. Als je dit cijfer deelt door de totale temperatuurverandering, krijg je de calorimeterconstante, die vervolgens wordt gebruikt voor volgende experimenten.
Beperkingen van calorimetrie
Geen enkele calorimeter is perfect. Zelfs met een uitstekende isolatie ontsnapt er onvermijdelijk een deel van de warmte naar de omgeving, waardoor er fouten ontstaan. Ongelijkmatig mengen kan temperatuurgradiënten veroorzaken, waardoor de nauwkeurigheid verder in gevaar komt. Bovendien zijn niet alle reacties geschikt voor calorimetrisch onderzoek. De snelle, hoogenergetische ontleding van TNT is bijvoorbeeld onpraktisch in een eenvoudige koffiekopjescalorimeter en kan zelfs veiligheidsrisico's opleveren voor een bomcalorimeter. Omgekeerd zorgen zeer langzame reacties, zoals de oxidatie van ijzer tot roest, voor temperatuurveranderingen die te subtiel zijn voor betrouwbare detectie.
 Welk element reageert snel met water om waterstof te produceren?
Welk element reageert snel met water om waterstof te produceren?  Wat is het evenwicht van 6H2O plus 6CO2-C6H12O6 6O2?
Wat is het evenwicht van 6H2O plus 6CO2-C6H12O6 6O2?  Is koolstofdioxide een waterstofbrug?
Is koolstofdioxide een waterstofbrug?  Dalian Coherent Light Source onthult nieuwe dissociatiekanalen in ethaanfotochemie
Dalian Coherent Light Source onthult nieuwe dissociatiekanalen in ethaanfotochemie Organische eutectica met kleine moleculen tonen potentieel voor het vervangen van kunststoffen
Organische eutectica met kleine moleculen tonen potentieel voor het vervangen van kunststoffen
Hoofdlijnen
- Wat is wetenschappelijke therory?
- Wat zit er in een oxyribonucleische cel?
- Biofysici vinden een manier om te kijken hoe membraanreceptoren werken
- Wat is een celstaart?
- Is een manier waarop wetenschappers organismen classificeren, is door reproduceren?
- Wat zijn de drie plantachtige stoffen die hun eigen voedsel produceren?
- Hoe menselijke activiteiten een van 's werelds meest afgelegen walvissoorten beïnvloeden
- Waarom moet de cel erfelijk materiaal kopiëren voordat hij zich verdeelt?
- Walvisliederen weerspiegelen de menselijke taal:een onderzoek toont aan dat de wet van Zipf van toepassing is op bultruggen
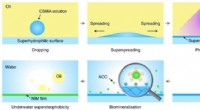
- Onderzoekers maken op parelmoer geïnspireerde superoleofobe onderwaterfilms
- Calorimeters begrijpen:hoe ze warmte meten en hun belangrijkste beperkingen

- Stress in kunststoffen visualiseren

- Wetenschappers pionieren met het maken van programmeerbare kunstmatige weefsels van synthetische cellen

- Spinifex belooft sterkere condooms

 Atoomnummer:protonen en elementidentiteit begrijpen
Atoomnummer:protonen en elementidentiteit begrijpen  EU's Juncker zegt dat er geen heronderhandeling over klimaatakkoorden is in Parijs
EU's Juncker zegt dat er geen heronderhandeling over klimaatakkoorden is in Parijs Is het mogelijk om de politieke polarisatie te verminderen?
Is het mogelijk om de politieke polarisatie te verminderen?  Buttes op Mars kunnen dienen als stralingsschuilplaatsen
Buttes op Mars kunnen dienen als stralingsschuilplaatsen Hoe varieert de viscositeit van vloeistoffen met de druk?
Hoe varieert de viscositeit van vloeistoffen met de druk?  Een soort potentiële energie die is gemaakt van fossiele brandstoffen?
Een soort potentiële energie die is gemaakt van fossiele brandstoffen?  Graven naar artefacten bevestigt neolithische periode in Nieuw-Guinea
Graven naar artefacten bevestigt neolithische periode in Nieuw-Guinea Een regenboog in een fles maken
Een regenboog in een fles maken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

